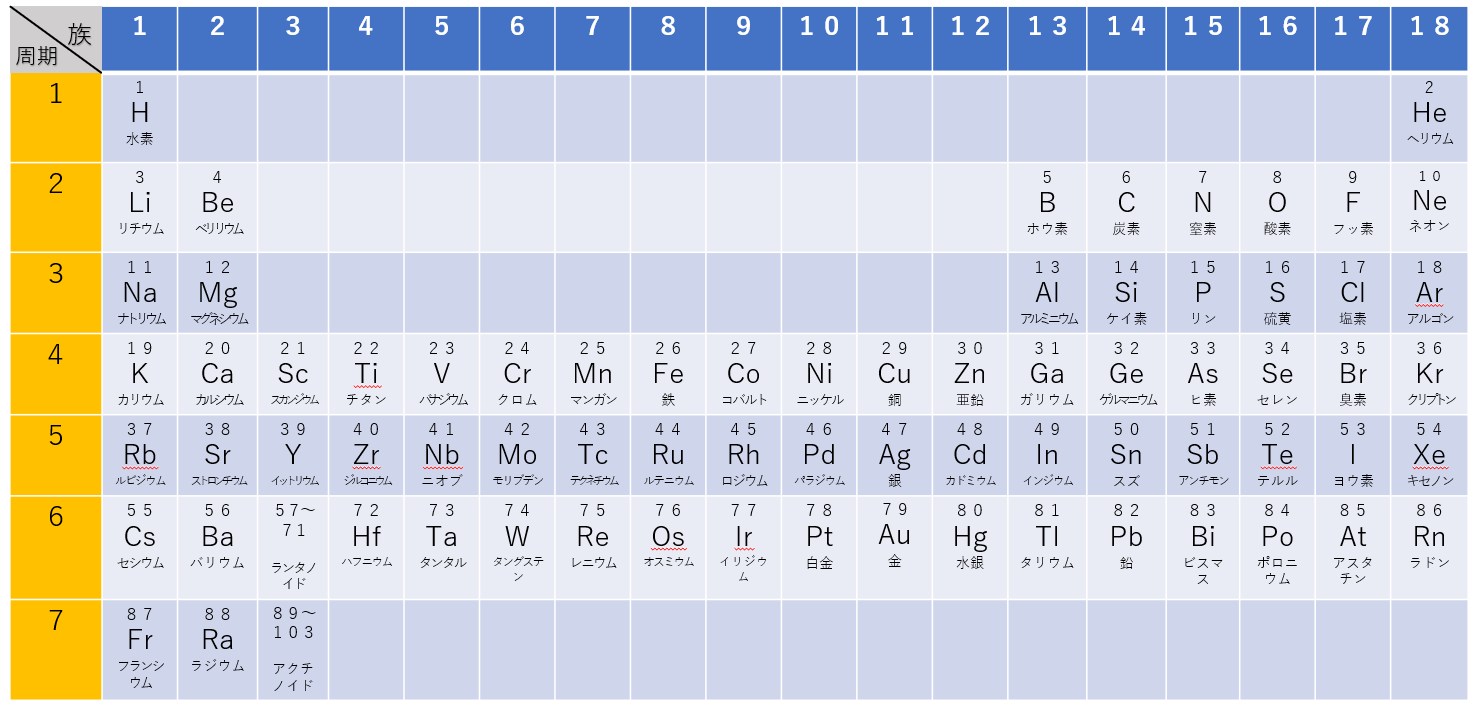
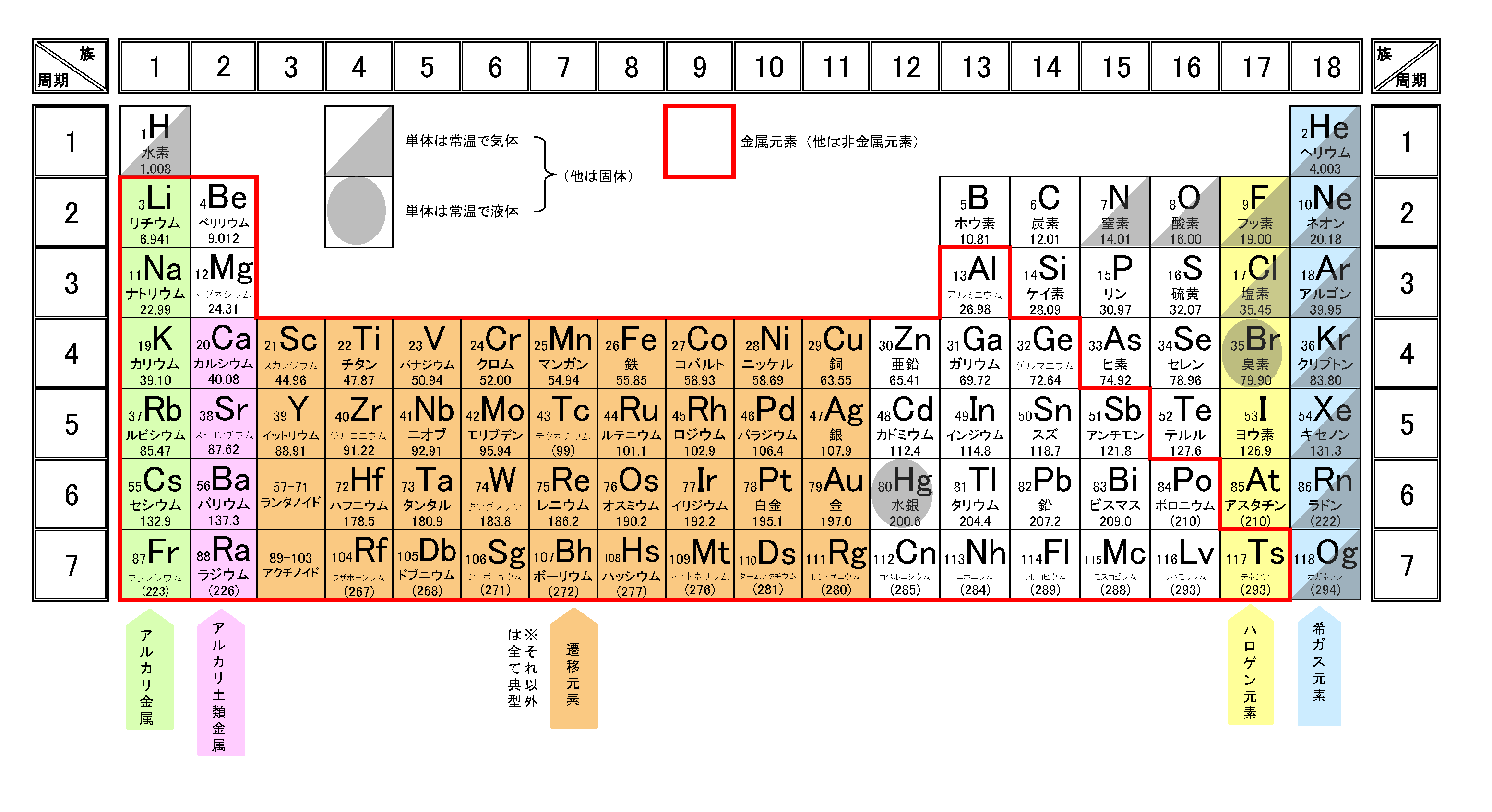
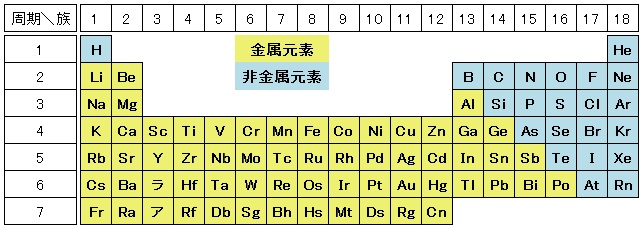
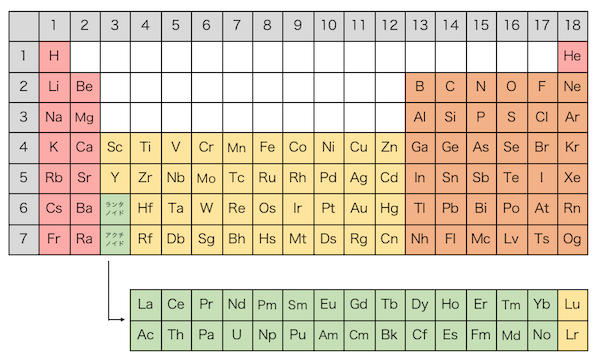
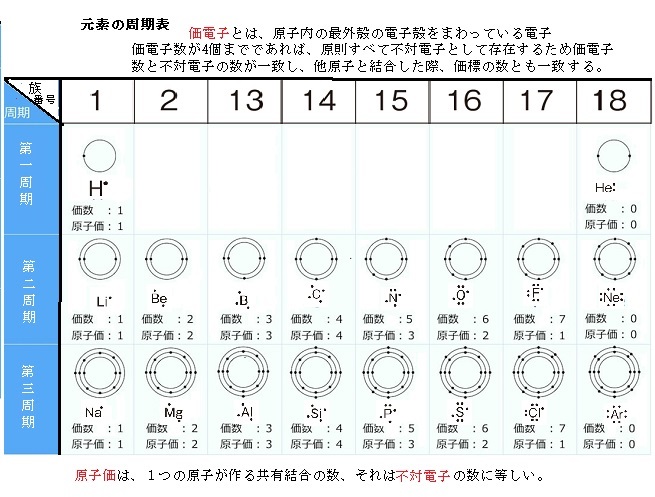
元素のエネルギー的安定性は、その原子の最外層が満たされるにつれて増加します。これは、他の原子への電子の「獲得」または「喪失」によって発生する可能性があります。原子にとってエネルギー的に最も有利なものは何でも起こります。たとえば、電子配置が ns 2 np 5 である元素は 、価電子殻 を完成させるために 1 つの電子を受け取るだけで済みます。この元素は、その原子の価電子殻に多数の電子を持つ非金属として分類されます。 ns 1 で終わる構成を持つ元素の場合、この周囲の電子が失われると、以前の殻が価電子殻になり、その原子の安定性が高まります。この元素は、原子価殻内の電子数が少ない 金属 として分類されます。このような議論では 、希ガス の安定性が考慮されています。

おそらく、化学周期性の最も印象的な例は、特定の元素とその周期の元素の間の原子の組み合わせの関係における 周期表 の周期にわたる変化に見られます。特に、この化学量論的な周期性は、化学者を周期律の発見に導きました。 「化合物中の原子の組み合わせの関係は、化学の周期性を見事に示しています。 表 1 に いくつかの塩素化合物の式を示します。比率は、IA 族 塩化物 の 1:1 から IVA 族塩化物の 1:4 まで変化し、VIIA 族塩化物の 1:1 に戻ります。 (塩素ガス Cl 2 は、化合物ではありませんが、表に含まれています。) この周期性は、当初からメンデリエフとマイヤーの注目を集めていました。 」

表 1. 化合物と塩素の原子の組み合わせの関係1。
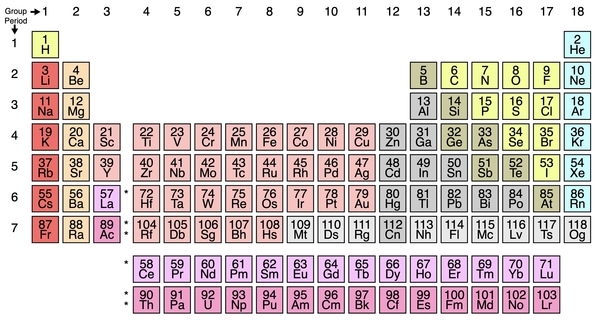
ただし、多くの例外が観察され、元素の割合が異なるさまざまな化合物を形成できる元素が存在するため、周期表内で占める位置は必ずしも元素によって作られる化学結合の数を示すものではありません。
たとえば、化学元素 鉄 (Fe) は +2 および +3 の 酸化数 変動 (NOX) を示し、この変動により塩化第一鉄 (FeCl 2 ) や塩化第二鉄 (FeCl 3 ) などの化合物が生成されます。接尾辞 oso は最小の NOX を示し、接尾辞 ico は 最大の NOX を示します。化学元素銅の NOX は +1 ~ +2 の間で変化し、塩化第一銅 (CuCl) と塩化第二銅 (CuCl 2 ) を形成します。これら 2 つの化学元素 (Fe と Cu) は、多様性と出現率の高い化合物の形成に関する正規性により議論されたことに注意してください。
参考文献:
1. ジョン・B・ラッセル; General Chemistry vol.1、サンパウロ: ブラジルのピアソン教育、マクロンブックス、1994 年。
サルデッラ、アントニオ。マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
マハン、ブルース・M。ローリー・J・マイヤーズ;化学: 大学コース、Edgard Blucher LTDA、サンパウロ/SP – 2002
ギャラリー