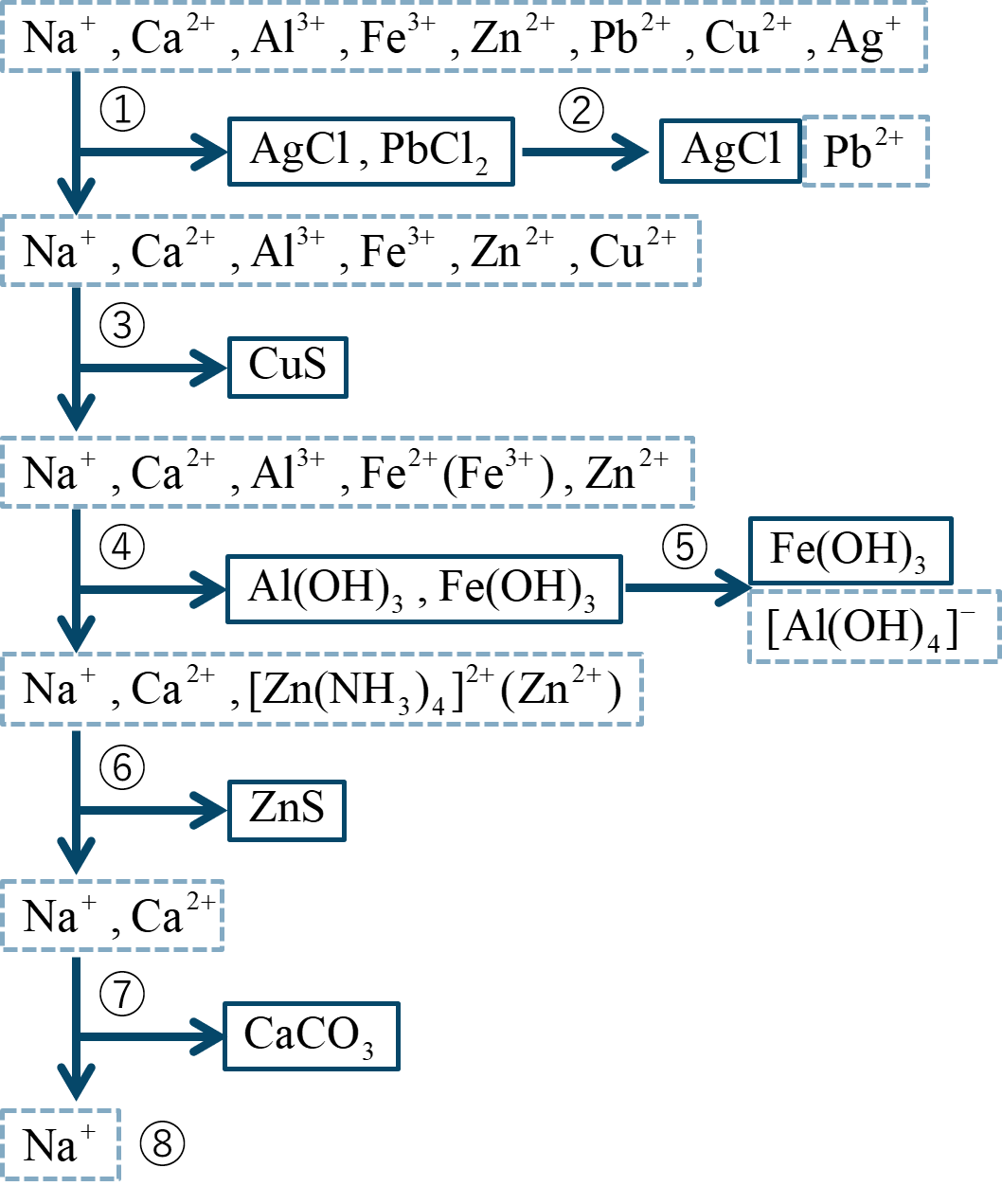
無機化学 で研究される反応は、合成、分析、置換、二重交換反応の 4 つのグループに分類できます。あらゆる無機反応は、これらの異なるグループの 1 つに属するものとして特徴付けることができます。

このテキストでは、中程度の高度な化学実験室で実行できる、これらの各反応の実験を紹介します。この実験の主な目的は、無機化学における主な反応を特定して同等にし、このトピックに関する一般的な質問に対処することです。そのためには、鉄やすり、硫黄、炭酸カルシウム、硫酸銅、金属亜鉛、 水酸化ナトリウム 、硫酸アルミニウムなどの試薬が必要になります。
(1) 合成 反応: 生成物に関連する反応物間の複雑さは大きくなります。
- 鉄やすり1gと硫黄1gを量ります。
- 磁石を使って、硫黄と混合した場合でも鉄の強磁性をテストします。
- 物質を再度混合し、混合物を磁器るつぼ中で加熱します。
- 形成された新しい物質の強磁性をテストします。
式: Fe + S → FeS
読み方: 1 モルの金属鉄は加熱すると固体硫黄と反応し、1 モルの硫化第一鉄が生成されます。
(2) 分析 反応: 反応物に関連して生成物はより複雑になります。
- 試験管に炭酸カルシウム1gを入れます。
- 試験管を加熱し、新しい物質の生成とガスの放出を観察します。
式: CaCO 3 → CaO + CO 2

(3) 置換 反応: あるアニオンと別のアニオンの間、またはあるカチオンと別のカチオンの間の置換が反応物質間で起こります。
- 100mLビーカーに硫酸銅の粗溶液を調製します。
- 亜鉛板を溶液に挿入します。
- 数分以内に、亜鉛シート上に赤みを帯びた銅の堆積物が現れるのを観察します。
式: CuSO 4 + Zn → ZnSO 4 + Cu

読み方: 1 モルの硫酸銅が金属亜鉛と反応し、硫酸亜鉛と金属銅を形成します。
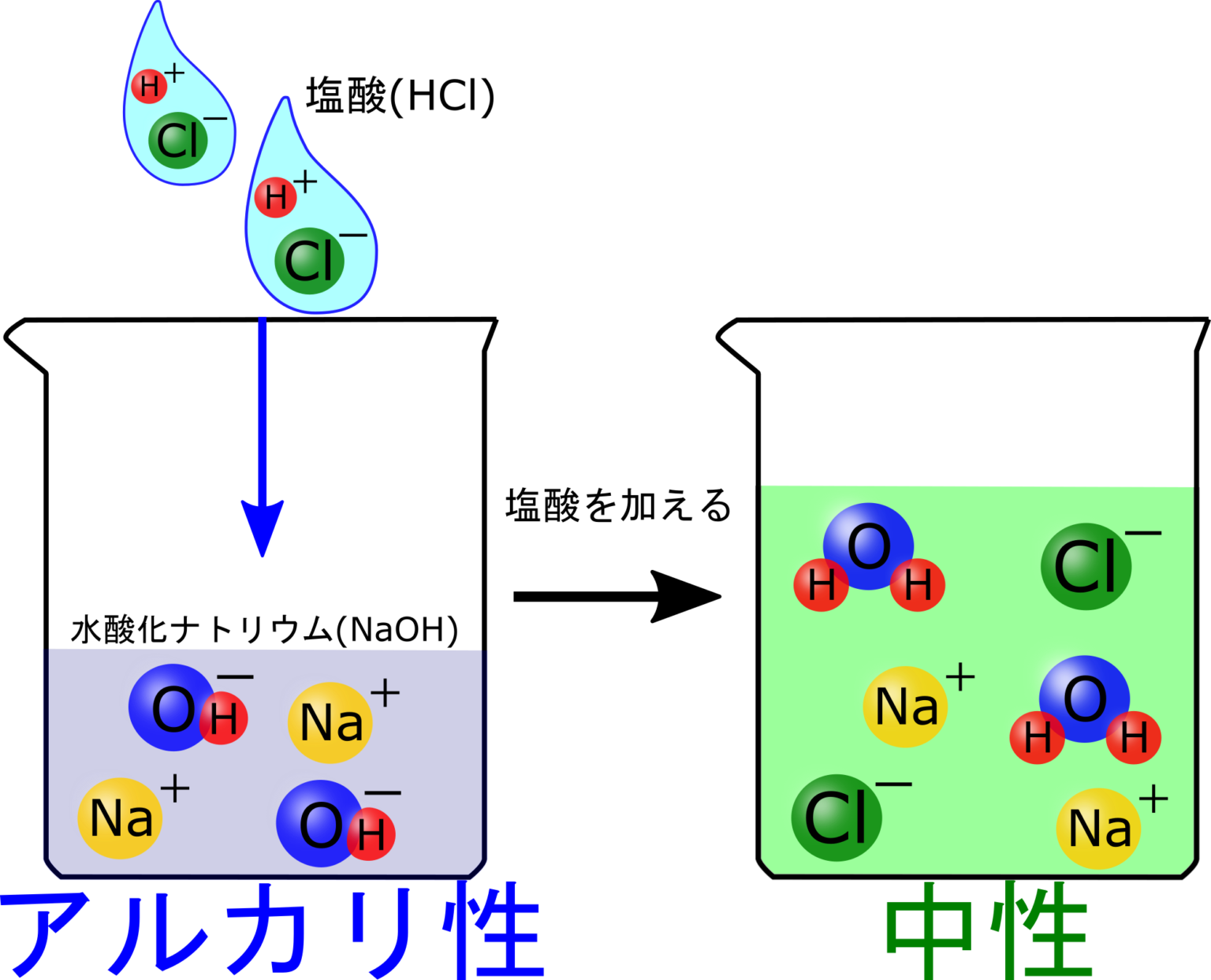
(4) 二重交換 反応: 最初の反応物のカチオンは 2 番目の反応物のアニオンに結合し、2 番目の反応物のカチオンは最初の反応物のアニオンに結合します。
- 試験管に水酸化ナトリウム水溶液 2mL を加えます。
- 別のチューブに硫酸アルミニウム溶液を加えて操作を繰り返します。
- チューブの 1 つで 2 つの溶液を混合し、水酸化アルミニウムの凝集を観察します。
式: 6NaOH + Al 2 (SO 4 ) 3 → 2Al(OH) 3 + 3Na 2 SO 4
読み方: 6 モルの水酸化ナトリウムが 1 モルの硫酸アルミニウムと反応し、2 モルの水酸化アルミニウムと 3 モルの硫酸ナトリウムが生成されます。
参考文献:
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ギャラリー