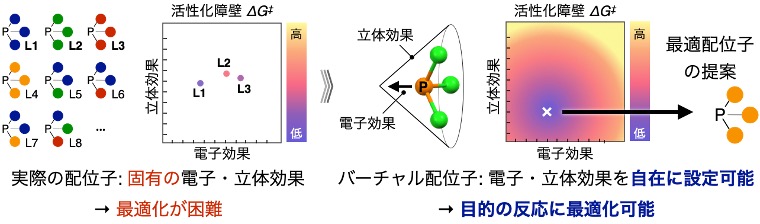
熱化学は 、2 つのシステム間の熱交換を扱う化学の分野です。化学反応は物質の構造の変化を表し、反応物が形成される生成物と化学的に異なるプロセスです。以下では、このトピックに関連する、互いに独立した 5 つのトピックについて説明します。

1 . 以下の表に示されているデータを考慮すると、
| 試薬・製品 | ΔH(標準状態) | |
| 1 | C(gr) → C(d) | +0.5 kcal/mol C |
| 2 | I(g) → 1/2I2(g) | -25 kcal/モルの I |
| 3 | 1/2Cl2(g) → Cl(g) | +30 kcal/mol Cl |
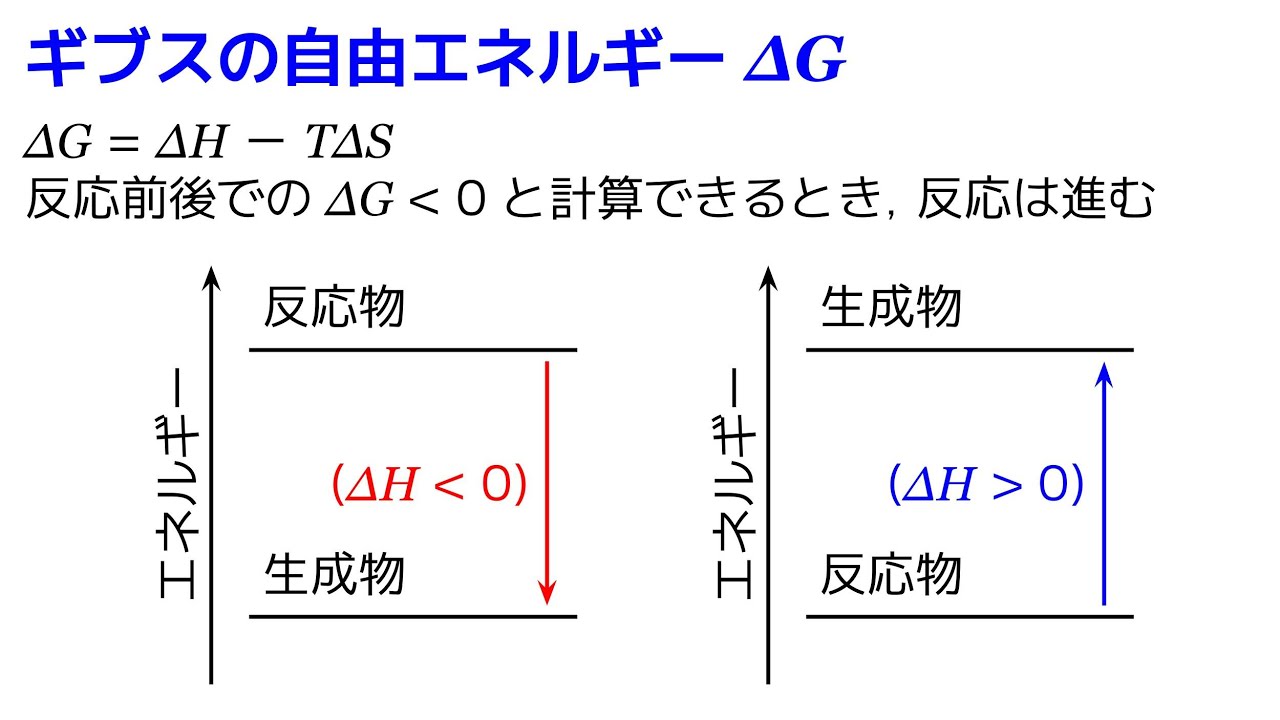
これは発熱プロセスであるため、(2) の場合のみ、反応物が生成物よりも大きなエネルギーを持っていると言えます。 (1) と (3) ではエネルギー吸収があるため、生成物は反応物よりも大きなエネルギーを持っています。

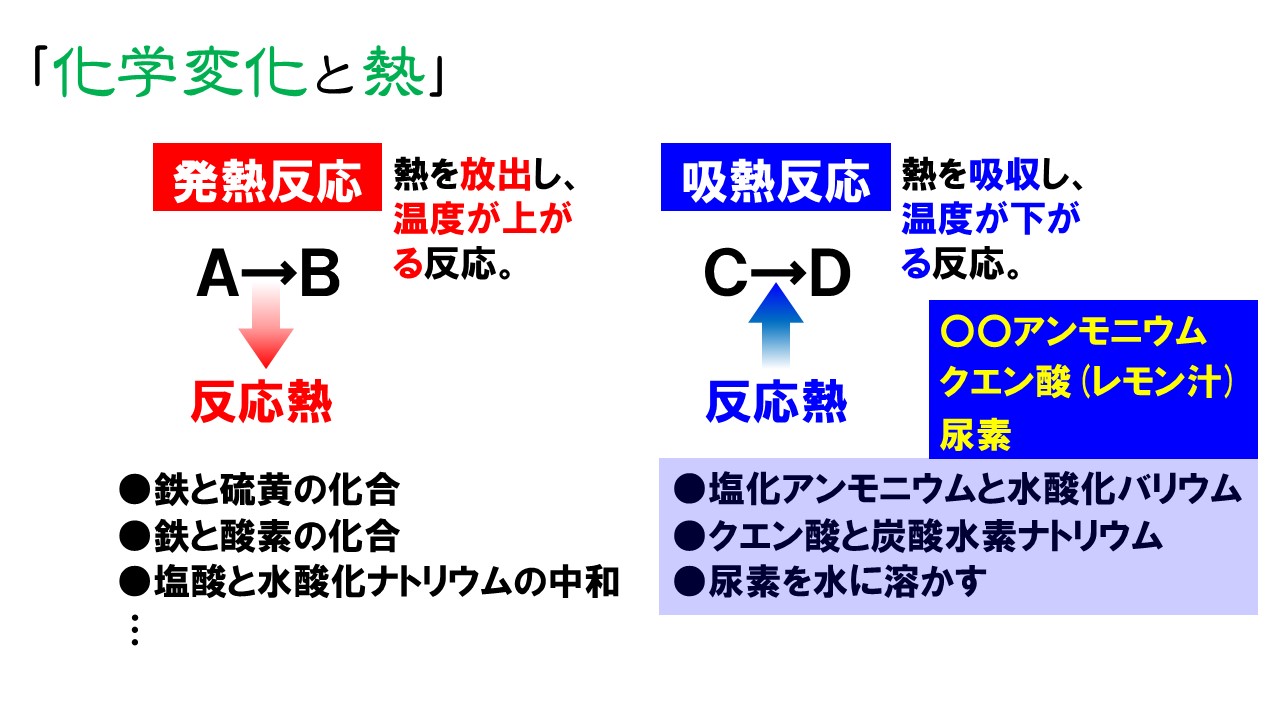
2. 太陽光の作用によるプールの水の 蒸発は 吸熱プロセスの例であり、これはプールの水が環境から熱を吸収する場合にのみ発生します。ろうそくからのパラフィンの燃焼、液体の水への濃硫酸の溶解、車のエンジン内での水和アルコールの燃焼、海水から 氷山 を形成するプロセスは、反応物から生成物への変換中に熱を放出するため、本質的に発熱を伴います。
3. 25 °C および 1 気圧で、1 モルの窒素が 1 モルの気体酸素と反応して、得られた生成物 1 モルあたり 22 kcal の吸収を伴う気体一酸化窒素を生成します。この情報を正確に表す図を以下に示します。

したがって、矢印の位置に従って、プロセスの吸熱特性を観察できます。 44 Kcal という値は、2 モルの生成物である一酸化窒素 (NO) の生成を指します。
4. 物質 A は、下図に示すような 3 つの凝集状態にあります (H = エンタルピー )。
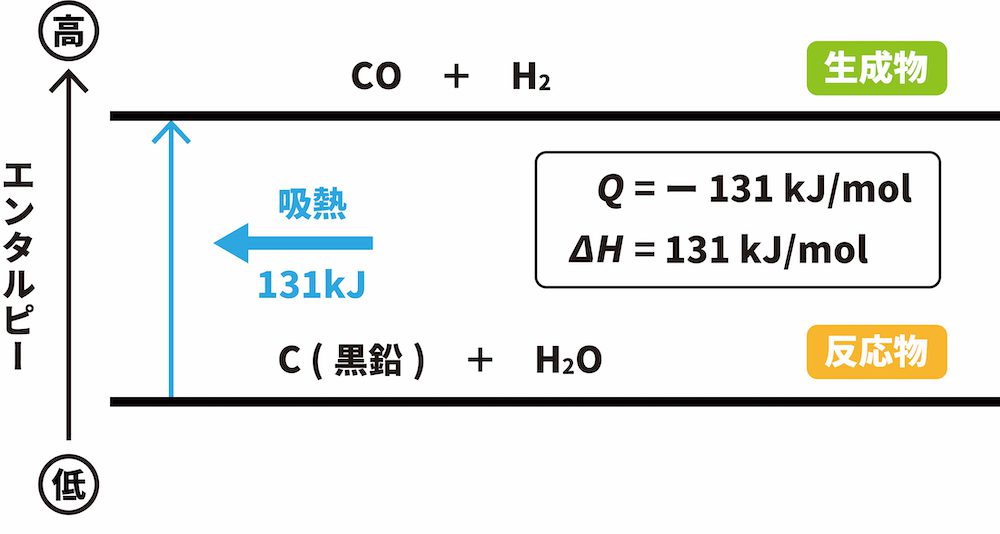
エンタルピーの降順は、H 蒸気 > H 液体 > H 固体になります。これは、蒸気状態では分子のエネルギー含有量 (エンタルピー) が他の物質の凝集状態よりも高いためです。
5. HCl と NaOH の反応は発熱反応、つまり熱を放出します。 0.8 molのHCl + 0.8 molのNaOHの「混合物」の直後は、0.6 molのHCl + 1.0 molのNaOHの「混合物」よりも高い温度が測定されます。これは、最初は反応物の割合が化学量論的にバランスが取れているためです。過剰な反応物や 制限的な反応物 は存在しません。

参考文献:
ラッセル、ジョン B. General Chemistry vol.1、サンパウロ: ブラジルのピアソン教育、マクロンブックス、1994 年。
ギャラリー