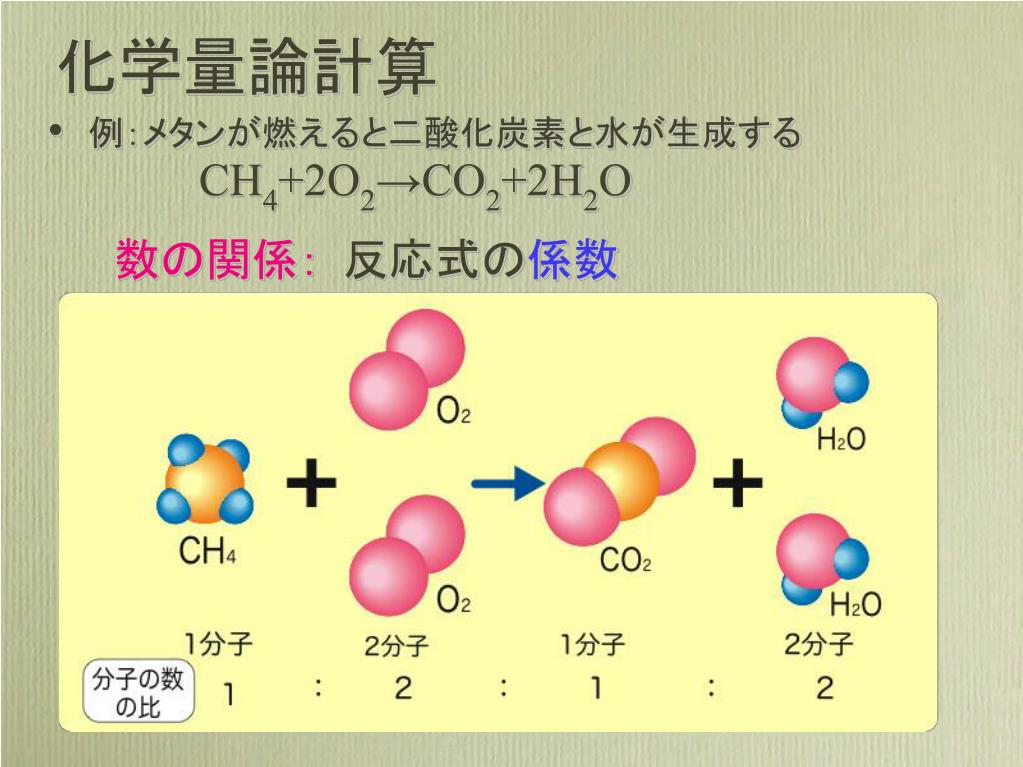
化学量論 は、対応する化学方程式を利用して化学反応に関与する反応物と生成物の量を関連付けることを可能にする計算です。

時間の経過とともに、物質の構成とその変化を説明しようとする無数の試みが行われ、1500年に長寿の秘薬と賢者の石を手に入れる目的でアラブ人とヨーロッパ人の間で錬金術が開発されました。その後、医薬化学が発展し、その主な名前はパラケルススでした。化学が科学的な性格を獲得したのは、18 世紀以降、理論と実践が組み合わされてからです。このとき、 ラヴォアジエは 質量保存則 あるいは自然法則を携えて登場した。
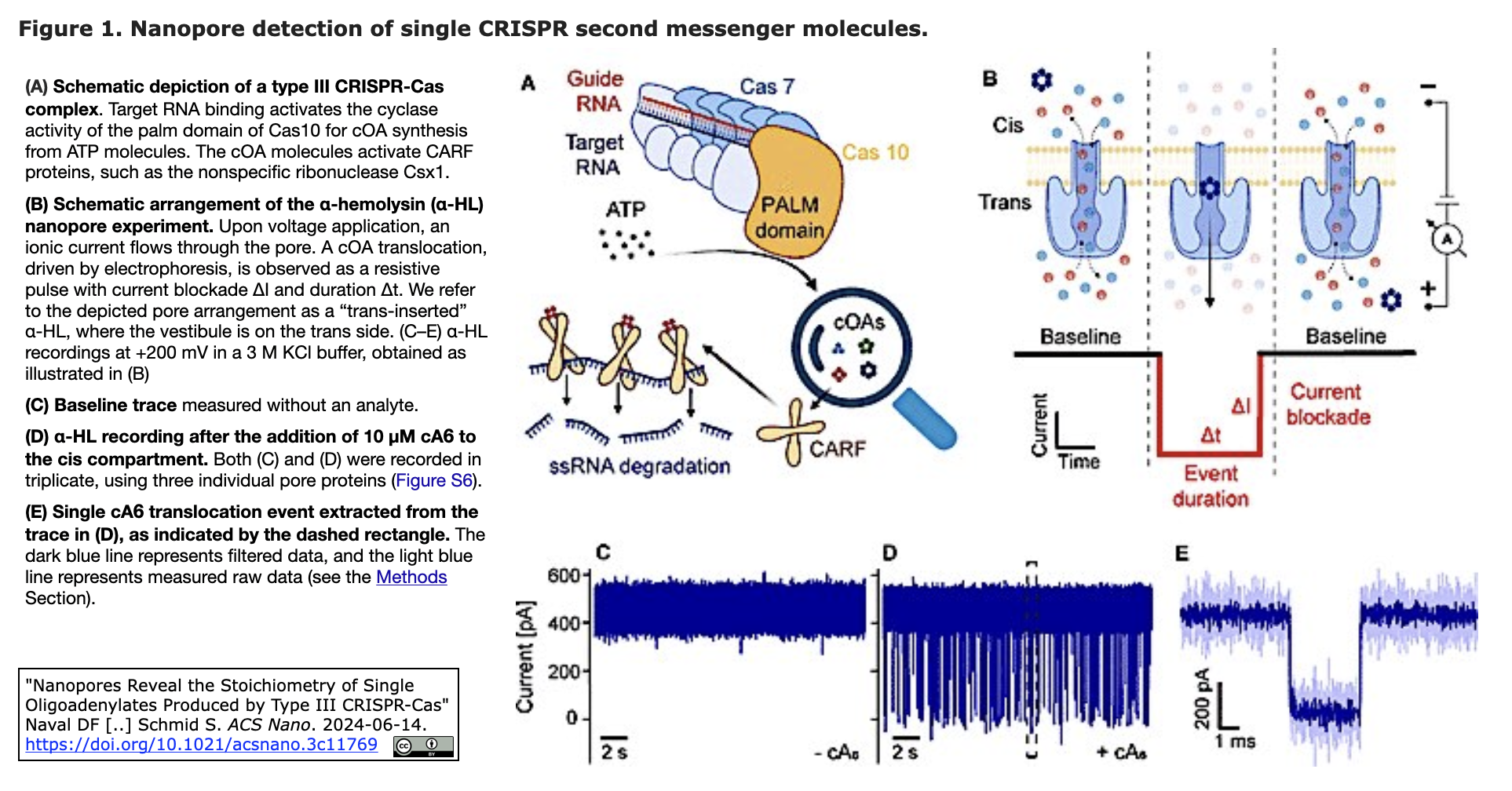
フランスの化学者であり、現代化学の父と考えられているアントワーヌ・ローラン・ド・ラヴォワジエは、密閉された容器内では、たとえ何らかの変換が起こったとしても、総質量は不変であると推測しました。彼の理論は次の理由で有名になりました。
「 自然界では、何も生成されず、何も失われず、すべてが変化します 。」

彼の理論を完成させたのがジョセフ・ルイ・プルーストであり、彼は 純粋な物質 を用いた実験を通じて、物質の質量組成はそれらを得るプロセスに関係なく一定であると結論付けました。つまり、反応物の質量の合計は、生成物の質量の合計と常に同じ値になります。

ラヴォアジエとプルーストの法則は ポンデラルの法則 として知られており、 化学量論 の研究を導くだけでなく、科学としての化学の始まりを示しています。上で説明した法則を例示する例を見てみましょう。
3 グラムの 炭素 が 8 グラムの 酸素 と結合して 二酸化炭素 を形成する場合、9 グラムの炭素は 24 グラムの酸素と結合して同じ化合物を形成します。この場合、反応物質の 1 つの値を 3 倍にするとき、反応によって生成物の量が比例するように、他の反応物質 (存在する場合) の量も 3 倍にする必要があることがわかります。これはプルーストの法則を明確に示しています。
反応物中の炭素が酸素と結合して二酸化炭素を形成することを分析すると、反応中に炭素原子が失われることはなく、単に生成物中に結合した形で存在し、したがって質量が一定に保たれることがわかります。
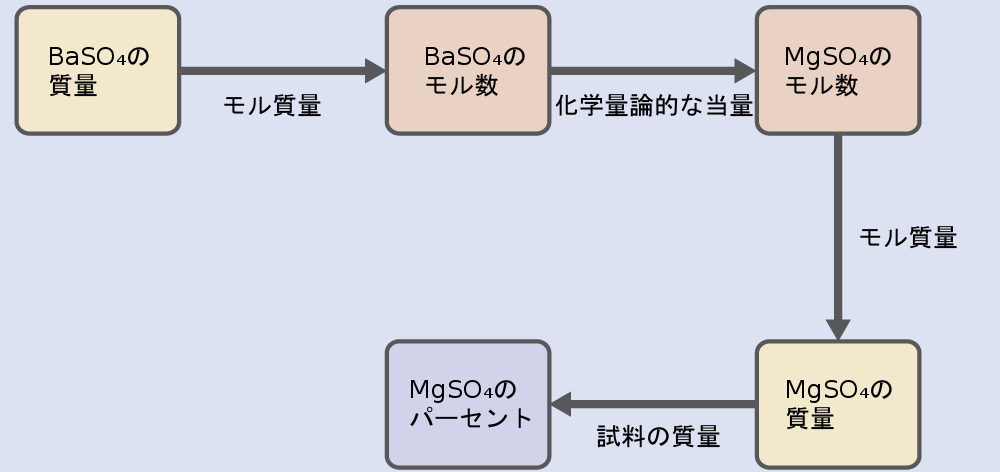
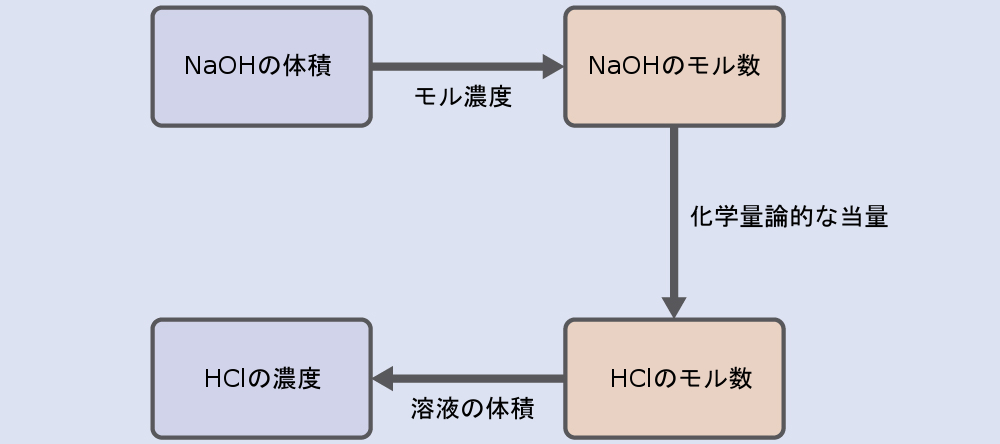
化学量論は、反応媒体中に存在する反応物質と生成物の量を関連付け、形成される生成物の量を事前に決定する計算によって得られます。計算を実行するには、いくつかのルールに従う必要があります。
1. まず、以下の数量の関係を明確にする必要があります。
1 mol – xg (物質表からの質量) – 6.02 x 10 -3 原子/分子 – 22.4L ( CNTP )
2. 反応物と生成物の係数が釣り合うように反応を記述します。バランスのとれたという用語は、反応物と生成物で同じである必要がある特定の化学元素の原子の数を指します。
これらの手順の後、通常は「3 つのルール」を実行して、求める値を見つけます。
このタイプの計算には、次のようないくつかの項を考慮する必要があります。
純度 : 反応物質のどれだけが実際に反応して特定の生成物を形成できるかを指します。たとえば、反応物の質量が 100 g であるとしますが、その純度が 90% であるという情報がある場合、反応するのは 90 g だけであると考えなければならず、したがって計算目的で考慮され、残りは不純物となります。 。
収量 : 収量は特に製品に関係します。反応に全収率がある場合、計算で予測された全量が得られることを意味しますが、実際には反応中に生成する残留物のため、これは一般に起こりません。しかし、計算を実行して、理想的な条件下で特定の反応で 180 グラムが生成され、実際の収率が 50% であることがわかった場合、生成物は 90 グラムしかないと考えなければなりません。
Khan Academy
が制作し、Fundação Lemann がポルトガル語に翻訳した
化学量論
に関する以下のビデオをご覧ください。
ギャラリー