人間の本性は、文化 (「科学」文化、行動文化など) によって示されるように、人間の知識を生み出すために、すべての情報を正当化することを私たちに強います。化学、特に原子学の分野では、何人かの科学者が自然界で観察される現象を正当化する説明モデルを提案しようとしました。この必要性から 原子モデル の理論が生まれ、目に見える宇宙と目に見えない宇宙を支配する「自然法則」の観察に基づいて作成され、覆され、改良されました。
これらの観察から、 ダルトン 、 トムソン 、 ラザフォード などのいくつかの原子モデルが出現しました。現時点では原子模型の進化について議論するつもりはないので、 量子数は シュレディンガーの原子模型 によって証明された基本的な概念であることを認識するだけで十分です。シュレディンガーの原子モデル理論は現在受け入れられており、力学量子に由来する 4 つの特性に基づいて、既知の量子数 (s、p、d、f) と理論的な量子数 (g、h、i…) の存在を前提としています。
これら 4 つの特性は量子数と呼ばれ、次のように列挙できます。
- 主量子数(n)
- 二次または方位量子数 (l)
- 磁気量子数 (m または ml)
- スピン量子数 (S または m s )
主量子数
主量子数 (n) は、 電子 が持つ エネルギー準位 または殻を定義し、原子核に対する軌道の距離と電子が占める軌道のサイズも定義します。この概念は、ニールス ベーアによって採用された層の概念に似ており、次のように例示できます。

主な量子数「n」の可能なレベルを含む表。
二次量子数
二次量子数 (l) は、電子の エネルギー サブレベル を定義するため特徴的です。 l の値の範囲は 0 から無限大ですが、現在、サブレベル (s、p、d、f) はほとんどわかっていません。エネルギーサブレベルは、量子力学では次のように定義されます。 l = n-1;サブレベルを次の表に示します。
| エネルギーレベル (n) | l値 | サブレベル | 理論的なサブレベル | 既知のサブレベル | 最大電子数* |
| 1 | 0 | 1 | s | s | 2 |
| 2 | 0、1 | 2 | s、p | s、p | 2+6 = 8 |
| 3 | 0、1、2 | 3 | s、p、d | s、p、d | 2+6+10 =18 |
| 4 | 0、1、2、3 | 4 | s、p、d、f | s、p、d、f | 2+6+10+14 = 32 |
| 5 | 0、1、2、3、4 | 5 | s、p、d、f、g | s、p、d、f | 2+6+10+14 = 32 |
| 6 | 0、1、2、3、4、5 | 6 | s、p、d、f、g、h | s、p、d | 2+6+10 = 18 |
| 7 | 0、1、2、3、4、5、6 | 7 | s、p、d、f、g、h、i | s、p | 2+6 = 8 |
* サブレベルあたりの電子の数: s = 2; p = 6; d = 10; f = 14。
式 2n 2 を使用すると、各準位が収容できる電子の最大数を計算できますが、この式は最初の 4 準位にのみ適用されます。これは、後続のサブ準位 (g、h、i) に関する知識が不足していることが部分的に原因です。 )。
磁気量子数
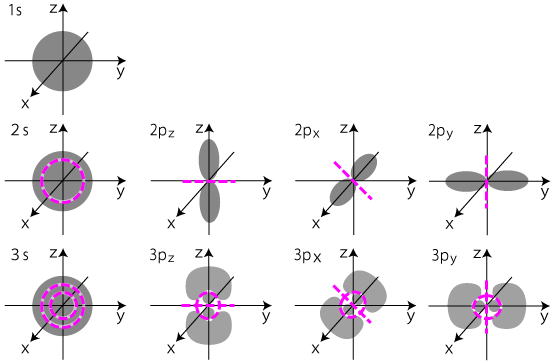
磁気量子数 (ml) は、各サブレベルの軌道数の特徴です。 m の数学的値は、m = ± l で与えられます。この推論を分解すると、 – l … 0 … +l となります。 s、p、d、f 軌道は以下に表されます。

既知のサブレベルの磁気量子数 (ml)。
スピン量子数
スピン量子数 (S または m s ) は、電子の仮想軸の下での電子の可能な回転運動を特徴付けます。

2 つの電子とそれぞれのスピンを記号で表現したもの。
上の画像では、矢印は電子の回転方向を示しており、この動きは最大多重度の原理 (フントの法則) に従ってサブレベルの充填に影響を与えます。この原理によれば、軌道の充填は、可能な限り最大数の不対電子を維持するような方法で実行されなければなりません。次の図では、2 つの完了試行が分析されます。

窒素:N 7 。不正解です。電子をペアで分配することによりフントの法則を無視し、空の軌道を残します。

窒素:N 7 。電子 (すべて不対) の分布におけるフントの法則を考慮しているため、正解です。
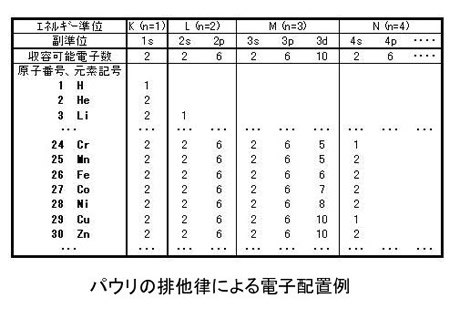
ペアリングは、孤立した電子に利用できる軌道がなくなった場合にのみ発生します。 パウリの排他原理 により、2 つの電子だけが軌道を占有し、反対のスピンを所有することが電子の安定性の基本条件となります。
参考文献:
フェルトレ、R;吉永、S. Atomística – 第 1 版 – サンパウロ: モデルナ、1970。 146~175。
FELTRE、R. 一般化学 – 第 5 版 – サンパウロ: モデルナ、2000。p.110 – 115。
ギャラリー