周期表 に示されている化学元素は、特定の法則に支配された組み合わせを通じて、地球上およびアクセス可能な宇宙のすべての物質を形成するため、私たちの物理世界の構成を表しています。ただし、化学結合の化学という観点から見ると、これらの元素は結合して「独自の生命」を獲得する必要があります。ただし、特殊な種類の化学元素は環境内でこれらの組み合わせが存在する必要はありません。これらの元素は ヘリウム 、 ネオン 、 アルゴン 、 クリプトン 、 キセノン 、 ラドン であり、 希ガス として知られています。

希ガス族は周期表の 18 番目の列 (最後の列) に位置しており、これには今でも族 O または 8A という古い名前が付いています。したがって、希ガスという名前は、これらの元素が 通常の温度および圧力条件下 では気体状態にあり (これらの元素は原子間引力が低い)、他の化学元素に対して不活性な挙動を示すという事実に由来しています。 。
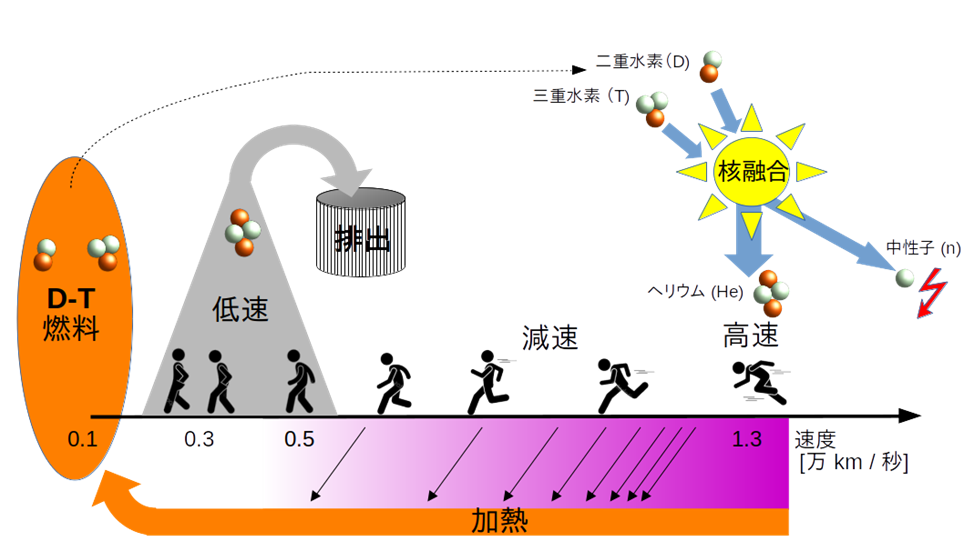
希ガスの安定性について最も受け入れられている説明は、その 原子価殻 が完全に満たされているという事実であり、化学結合に関する化学理論は希ガスのこの特性に基づいており、そのため他の化学元素は結合する際に、最も近い希ガスの構成と同一の構成を求めることになります。

希ガスは 地球 の 大気 中に適度な量で存在しますが、化学反応性が低い (不活性な性質) ため、当初は発見されませんでした。これらの特性を持つ化学元素の最初の証拠は、 太陽 からのヘリウムの発見によって起こりました。これは太陽光の 分光法 によって可能になりました。数年後、ヘリウムは地球の大気から分離されるでしょう。
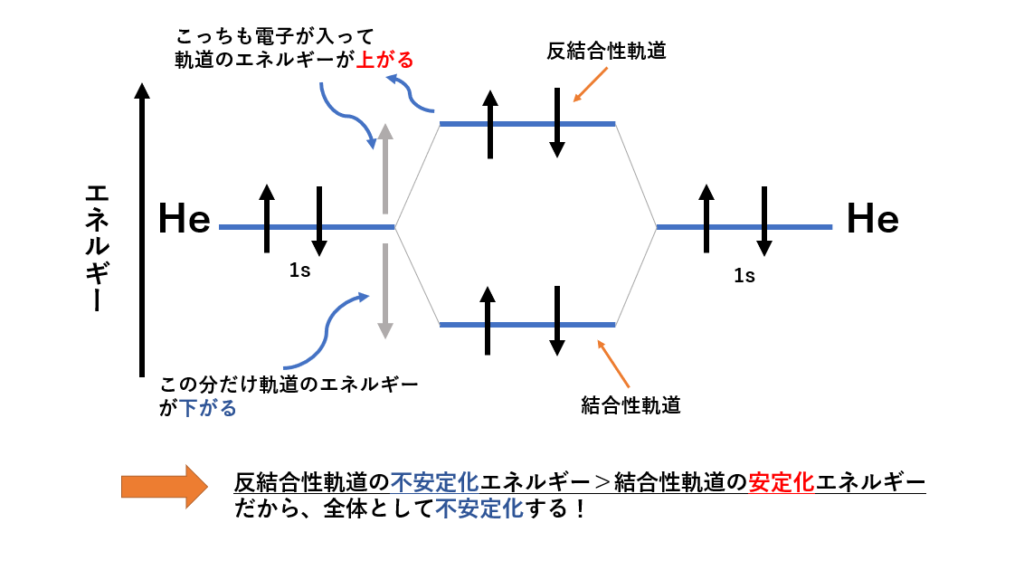
すでに述べたように、希ガス化学元素の原子は完全な外部軌道を持っており、これは化学反応性が低いことを意味します。周期表では、下に行くほど、これらの元素の反応性がわずかに高くなり、元素キセノンと フッ素 の間で化合物が形成される可能性があります。 ウランが ヘリウムを除く他の希ガスと結合を形成した化合物はすでに発見されており、今日ではその安定性と電子配置は、模倣すべきルールというよりも、従うべき傾向として機能しています。
今日、希ガスが比較的多様性に富んだ金属と化合物を形成する可能性があることがわかっており、その実験的挙動に基づくと、 ヘリウムガスは 周期表のすべての化学元素の中で最も不活性であると依然として考えられています。
参考文献:
アトキンス、ピーター。ロレタ・ジョーンズ。化学の原理: 現代生活と環境への疑問、ポルト アレグレ: ブックマン、2001 年。
エプスタイン、ローレンス M.ローゼンバーグ、ジェローム l.一般化学、
(シャウム コレクション)、ポルト アレグレ: ブックマン、2003 年。
ギャラリー











.png?resize=636,418&ssl=1)


