周期表では、 右側にある元素は左側にある元素よりも 電気陰性度 が高くなる傾向があります。電気陰性度の高い元素の中で目立つのは フッ素であり、 この周期性の値が最も高くなります。この元素は ハロゲン のグループ、つまり 17 族に属し、その最大の特徴は、結合を確立するときに 電子を 自分自身に引き付ける傾向があることです。その名前は、「走る」を意味するラテン語の「 fluere 」に由来し、化学記号はFです。1886年、化学者のアンリ・モアッサンは初めてフッ素の単離に成功し、その結果、1906年にノーベル化学賞を受賞しました。原子番号 9 および質量番号 19.00 のこの元素の 電子分布は 次のとおりです。
1秒 2 2秒 2 2p 5
最後の層ではフッ素が 7 個の電子を持っていることに注意してください。これは、 オクテット理論 に従って安定化しようとしているため、電子引力の高い傾向を説明しています。
しかし、この理論は何を言っているのでしょうか?彼女は、18 族の元素または 希ガスは 、 原子 全体に 2 個の電子しか持たない ヘリウム (He) を除いて、最後の殻に 8 個の電子を持つため、大きな反応性を持たないと説明しています。その結果、周期表内の他のすべての元素は、この電子配置を取得するために (何が最もアクセスしやすいかに応じて) 電子を獲得または喪失する傾向があります。プロセスは常にエネルギーを低くし、安定性を高める傾向があることを常に覚えておく必要があります。
フッ素の話に戻ると、次のような基本的な特性を挙げることができます。


蛍石 (CaF 2 ) はフッ素元素の主な供給源です。写真: Cagla Acikgoz / Shutterstock.com
ハロゲンの中で、フッ素は 地球 上で最も豊富な元素であり、主に氷晶石や蛍石などの一部の鉱物に含まれています。フッ素は、あまり一般的ではない方法の中でも、 アルミニウム 製造の副産物として得ることもできます。これは主に産業によって放出される汚染ガスである CFC ( クロロフルオロカーボン ) に含まれており、最終的には オゾン層 に損傷を与え、 温室効果 を増大させます。

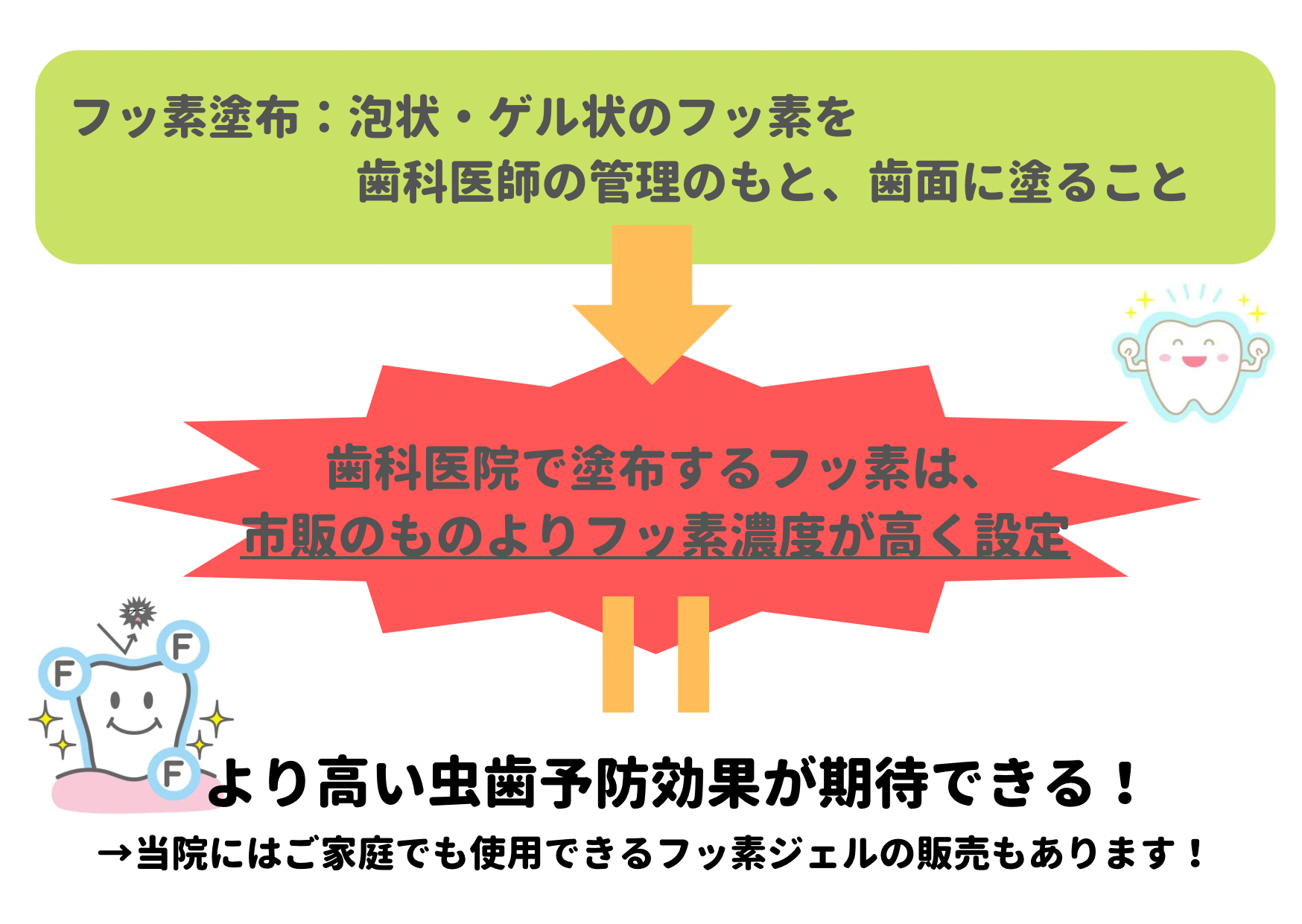
この元素は私たちの体にとって極めて重要ではありませんが、かなりの濃度で摂取すると害を引き起こす可能性があります。通常、口腔の問題を解決する方法として 処理工場 の水に添加されます。いくつかのアプリケーションがあり、その一部を以下に示します。
ギャラリー