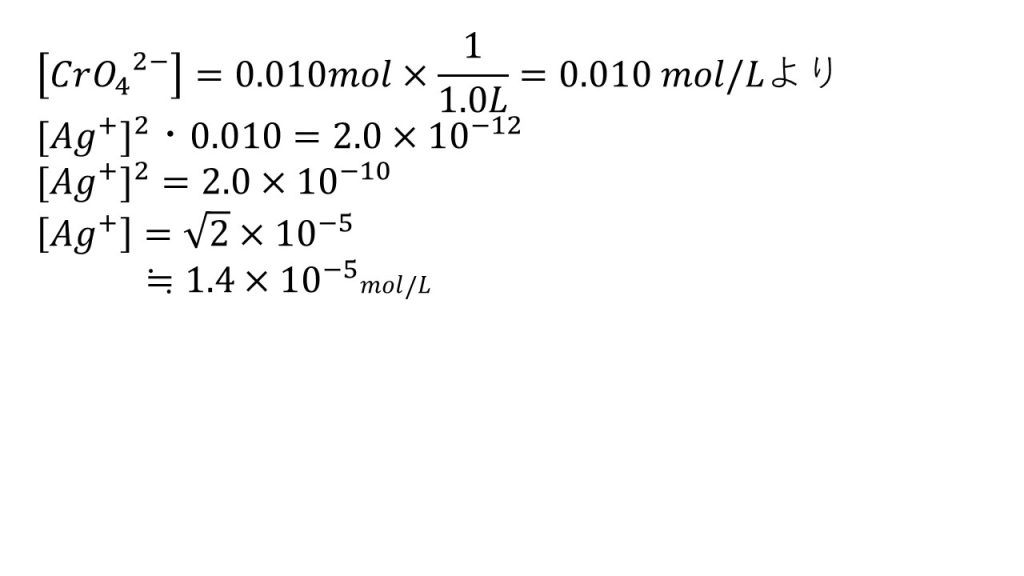NaOH (s) + H 2 O → Na + (aq) + OH – (aq)
元のベース分子にすでに存在するイオンが分離されていることが確認されます。
イオン化 と呼ばれるプロセスは 、共有結合 (電子の共有) の化学結合 からイオンが形成されるプロセスです。以下の塩酸 (HCl) の例を考えてみましょう。

HCl (g) + H 2 O → H + (aq) + Cl – (aq)
これらのイオンは元の酸分子には存在しないため、溶液中でイオンの形成が起こることが確認されています。
推奨される質問:

1. 解離とイオン化を概念化して区別します。
2. 2g の固体 NaOH を完全に 中和する のに十分な 1.5M HCl 水溶液の最小量を決定します。
3. カウンター上にこぼれた 200mL の 3M 硫酸を中和したいと考えています。この場合、 水酸化カルシウム と水酸化アルミニウムが選択肢となります。塩基の解離の程度を無視して、酸を完全に中和するために必要な質量が最も低い塩基を決定します。

4. 250 mL の 2M NaOH 水溶液を中和したいとします。このために、 濃塩酸 サンプルが実験室で見つかりました。一方、化学技術者は、中和に使用するためにこの酸の 1M 溶液を調製することにしました。それでは、どのくらいの量の濃塩酸が使用され、どのような手順が適切なのでしょうか?
6. NaOH の解離係数が 92%、HCl のイオン化度が 98% であることがわかっているので、1M 水溶液の場合、中水溶液中の 100mL の NaOH を完全に中和するのに必要なこの酸の最小体積を決定します。濃度は24g/L。

7. 酢のサンプルには質量で 5% の 酢酸 が含まれています。酢酸のイオン化度が 60% であるとすると、酢 100mL の酸分を中和できる 1M NaOH 溶液 (α = 92%) の最小質量はいくらになります。
8. 12g の金属鉄を完全に腐食できる 1M 塩酸水溶液 (α = 98%) の最小量を決定します。
参考文献:
ラッセル、ジョン B. General Chemistry vol.1、サンパウロ: ブラジルのピアソン教育、マクロンブックス、1994 年。
サルデッラ、アントニオ。マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
マハン、ブルース・M。ローリー・J・マイヤーズ;化学: 大学コース、Edgard Blucher LTDA、サンパウロ/SP – 2002
ギャラリー