無機化合物は、 元素または非金属元素のグループに結合した 金属 または 水素 を有する化合物です。 無機機能 は、 酸 、 塩基 、 塩 、 酸化物 です。 硫酸は、 その構造内にイオン化可能な水素を持ち、分子の唯一の正に荷電した部分が H + カチオンであるため、酸のグループに属します。

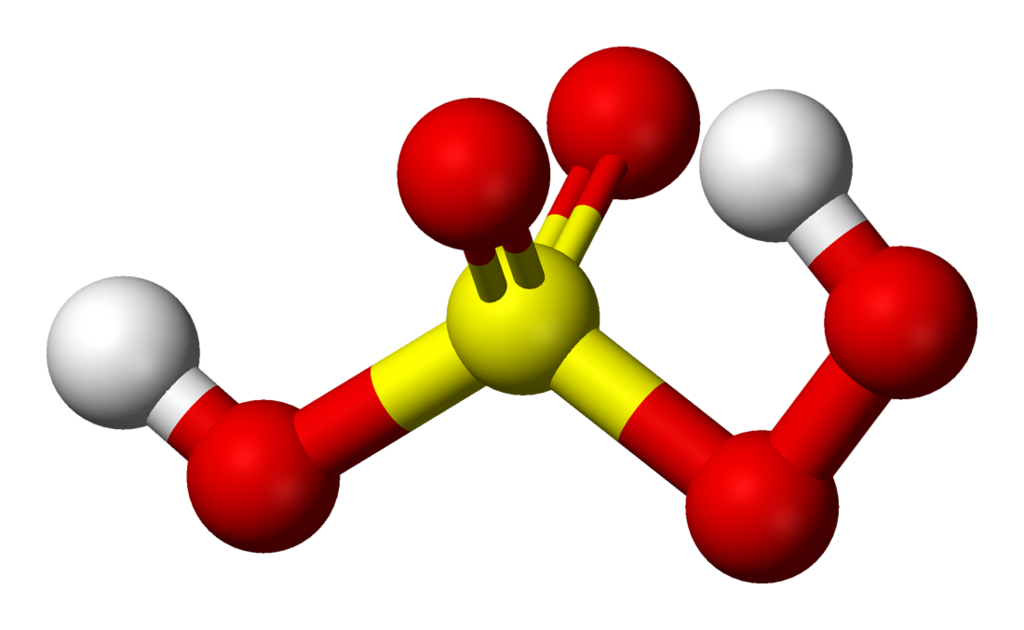
おそらく発見者は中世の 錬金術師 ジャビル・イブン・ハイヤンであり、硫酸の名前は当初ザイト・アル・ザイ、つまりビトリオールの油でした。この酸は分子式 H 2 SO 4 を持ち、 その幾何学的形状は四面体であり、その構造は以下に表されます。
この分子内の結合はすべて極性 の共有結合 です。

酸の強さは水中でイオンを形成する能力と密接に関係しており、その結果、 電流 が伝導します。 酸素酸 (構造中に酸素を含む酸)の強度を分析する方法の 1 つは、 分子 内に存在する酸素の数からイオン化可能な水素の数を引くことです。結果が 2 以上の数値であれば、強酸であることがわかります。結果が 1 に等しい場合、酸は中程度であり、1 未満の場合、酸は弱いと見なされます。
たとえば、硫酸の場合、次の減算があります。

(O 原子の数 – H 原子の数)
(4-2=2)

結果は 2 に等しいため、硫酸を 強い として分類できます。
この広く使用されている物質のいくつかの特徴は、液体、無色、非常に有毒で粘性があることです。一般に純度 97% で販売されており、室温では 蒸発が 非常に遅いです。腐食力が高く、誤って摂取したり、皮膚に吸い込んだりこぼしたりすると、人体に重大な問題を引き起こします。 硫黄 、酸素および水から接触プロセス( バナジウム または白金化合物によって触媒される酸化プロセス)を通じて得られます。

この酸は産業で最も使用されており、この物質の消費が増えるほど産業が発展するため、国の産業指数の指標として機能するため、用途は多岐にわたります。この大規模な使用のマイナス要因は、硫黄化合物の放出量の増加による 酸性雨 プロセスの悪化です。以下にそのアプリケーションの一部を示します。
ギャラリー