無機化合物は 、少なくとも 2 つの異なる元素の原子または分子によって形成され、鎖を形成して 水素 に結合した構造内に 炭素 原子を含まないすべての物質です。状況によっては、化合物の構造に炭素が現れることがありますが、その結合方法により、CO 2 や Na 2 CO 3 の場合と同様に無機とみなされます。
歴史的に、 有機化合物と無機化合物 の区別は、有機化合物がすべて生物由来の物質、つまり有機機能システムであると信じられていたために生まれました。無機化合物は、鉱物や他の無生物などの「死んだ」システムに由来します。
無機化合物は 周期表 上の任意の元素によって形成されますが、一般に 非金属 または水素で構成され、金属原子との結合を持っています。結合に関しては、 イオン結合 、 共有結合 、 配位結合のいずれ かになります。イオン結合によって形成される化合物には、 電気陰性度の 差が 1.7 eV を超える元素 (通常、非金属に結合する金属) が含まれていることを思い出してください。共有結合性化合物は、電気陰性度の差が 1.7 eV 未満の元素 (通常、非金属同士または水素に結合したもの) によって形成されます。 配位化合物は、 1 つまたは複数のルイス塩基に結合した 1 つまたは複数の ルイス酸 で構成される分子です。場合によっては、配位化合物で発生するように、物質は同じ分子内にイオン結合と共有結合を持っています。
無機化合物は、酸、塩基、塩、酸化物に分類されます。
この記事の内容
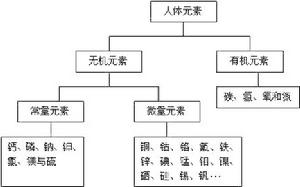
酸
例: HCl、H 2 SO 4 、HCN

塩基または水酸化物
アレニウスによれば、それは水溶液中で唯一の陰イオンとして OH – ( ヒドロキシル ) イオンを放出するあらゆる物質です。
例: NaOH、Ca(OH) 2 、Al(OH) 3
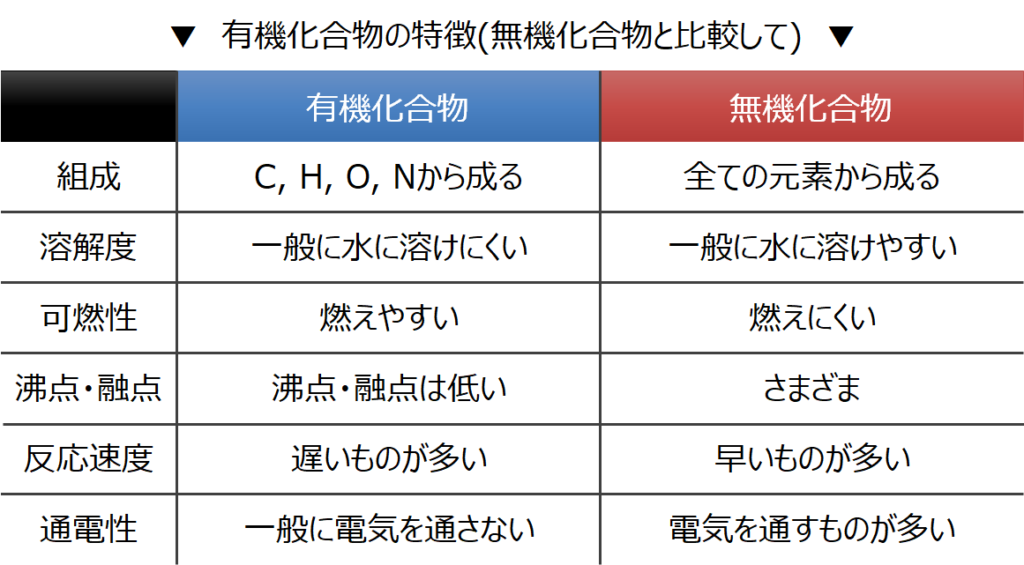
塩
塩は、水溶液中で 解離 を受け、H + 以外の少なくとも 1 つのカチオンと OH – 以外の 1 つのアニオンを放出するあらゆる物質です。
例: NaCl、FeCl 3 、Na 2 SO 4

酸化物
例: CO 2 、SO 3 、Na 2 O

生物学的に重要な無機化合物
水 (H 2 O) : 水は生命を維持するために最も重要な化合物です。さまざまな物質を溶解し、いくつかの化学反応および生物学的反応の基礎となります。
ガス状酸化物 (CO 2 、SO 2 、SO 3 、NO x ) : 化石燃料 の 燃焼 と 呼吸 によって形成され、地球の 大気 中に存在し、 酸性雨を 発生させ、 オゾン層 に悪影響を与える可能性があります。
参考文献:
アトキンス、PW、ジョーンズ、L.、『化学の原理: 現代生活と環境への疑問』第 5 版、ポルト アレグレ: ブックマン編、2012 年。
Usberco J.、Salvador E.、Química Geral、第 12 版、サンパウロ: サライバ、2006 年。
ギャラリー