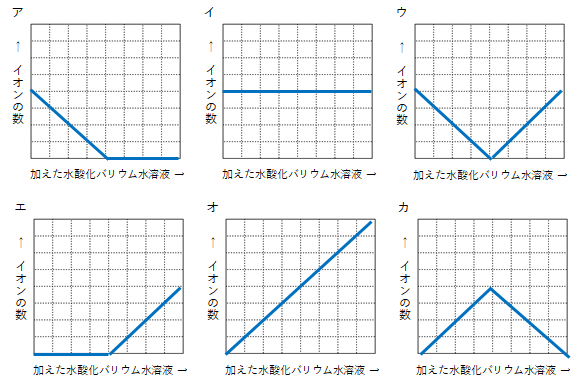
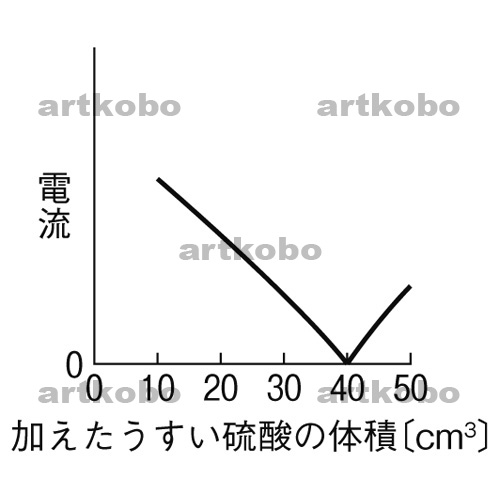
一般に アレニウス塩基 と呼ばれる 水酸化物は 、 カチオン と ヒドロキシル 基 (OH – ) の結合から形成される 無機化合物 です。アレニウスによれば、塩基または水酸化物とは、 水溶液 中で 解離し 、アニオンとしてのみ OH – イオンを放出するあらゆる物質です。これらは、水に溶解すると、高濃度の水酸化物イオンによりアルカリ性の pH を示す化合物です。
NaOH + H 2 O → Na ++ OH –
一般に塩基は有毒で腐食性の化合物であり、その取り扱いには注意が必要です。水中での解離能力が高いため、皮膚に触れると 火傷を 引き起こす可能性があります。
水酸化物の形成中、ヒドロキシルイオンの電荷は-1であるため、それがカチオンと結合すると、基本式中のヒドロキシルイオンの量はカチオンの電荷と等しくなります。
例:バリウム(Ba)元素を使用して水酸化物を生成する場合
Ba 2+ —- OH –
電荷をキャンセルするには、2 つの OH – イオンが必要です。この場合、基本式は Ba(OH) 2 になります。
塩基はいくつかの方法で分類できます。
この記事の内容
水酸基の数による分類
- 一塩基 : ヒドロキシルを 1 つ持ちます。例: NaOH
- 二 塩基 : ヒドロキシルを 2 つ持ちます。例:Ca(OH) 2
- 三塩基 : 3 つのヒドロキシルを持っています。例:Fe(OH) 3
- Polybase : ヒドロキシルが 4 つあります。例:Pt(OH) 4
水への溶解度による分類
- 可溶性 : アルカリ金属および水酸化アンモニウム 。
- わずかに溶ける : マグネシウム を除く、 アルカリ土類金属 の水酸化物。
- 実質的に不溶性 :Mg(OH) 2

強さによる分類
- 強 ( イオン化度 がほぼ100%):アルカリ金属およびアルカリ土類金属の水酸化物。
- 弱い (イオン化度が 5% 未満): その他すべて。
水酸化物の命名法
固定 NOX 金属を含む水酸化物の命名法は、次の一般規則に従います。
________水酸化物
元。:
- KOH – 水酸化カリウム
- Zn(OH) 2 – 水酸化亜鉛
ベースが固定の nox を持たない金属で作られている場合、命名法にこの金属の nox を示す必要があり、これは次の 2 つの方法で行われます。
名前の末尾に金属のNOXをローマ数字で表記。
元。:
- Fe(OH) 2 – 水酸化鉄 II
- Fe(OH) 3 – 水酸化鉄III
物質内の金属の NOX を示す接尾語を使用します。接尾辞 oso は金属の最低 NOX に使用され、接頭辞 ico は 最高 NOX に使用されます。
元。:
- Fe(OH) 2 – 水酸化第一鉄
- Fe(OH) 3 – 水酸化第二鉄

日常生活の大切な拠点

水酸化ナトリウム (NaOH)
苛性ソーダとして知られ、パイプの洗浄や詰まりの解消に国内で広く使用されています。非常に腐食性が高いため、取り扱いには注意が必要です。
水酸化アンモニウム (NH 4 OH)
これは、水に最大 30% の アンモニア を溶解することによって形成される塩基です。息が詰まるような強い臭いがします。この塩基は、金属陽イオンから形成されず、溶液中にのみ存在する唯一の塩基です。
水酸化カルシウム (Ca(OH) 2 )
それは消石灰として知られており、建築のモルタルの準備や砂糖の精製に使用される白色の固体です。
参考文献:
Usberco J.、Salvador E.、Química Geral、第 12 版、サンパウロ: サライバ、2006 年。
ギャラリー