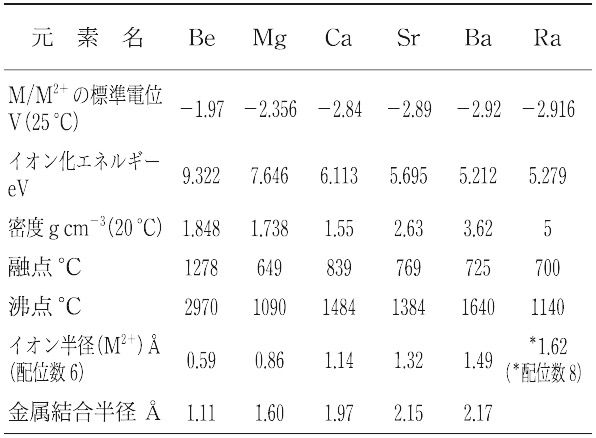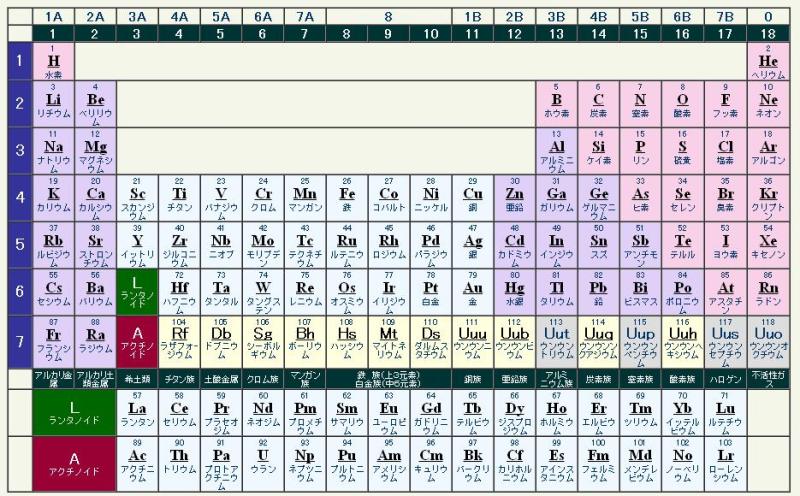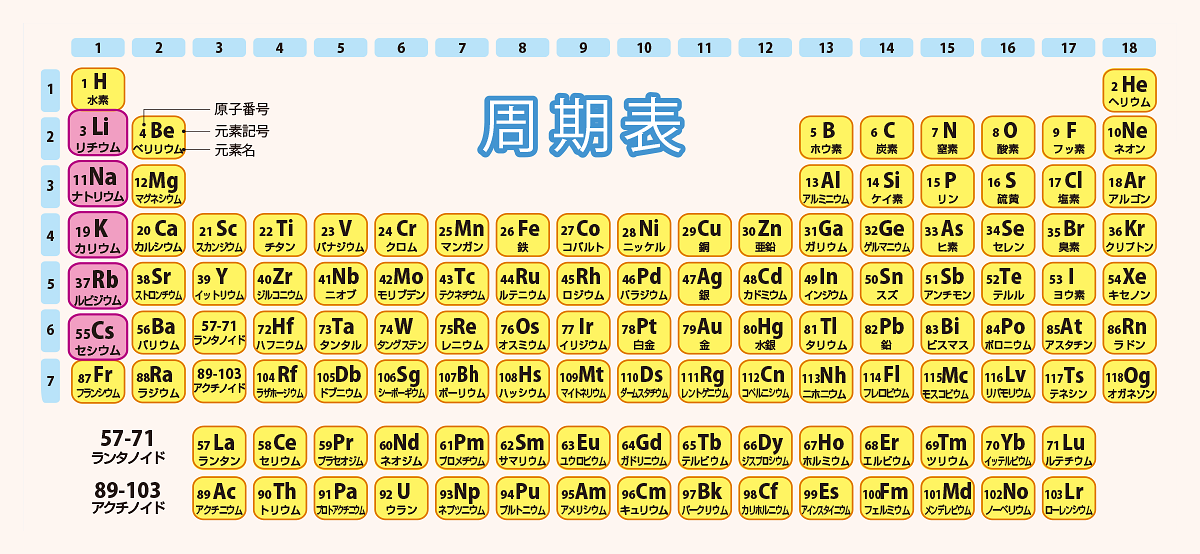
アルカリ土類金属 (アルカリを形成するためアルカリ性、 アレニウス塩基 、その 酸化物が 長い間土と呼ばれていたため土性) は、 周期表 の 2A 族の元素を表し、 電子配置が ns² で終わる、n は対応する数を表します。最後のレイヤー (1 ~ 7 の範囲) まで。
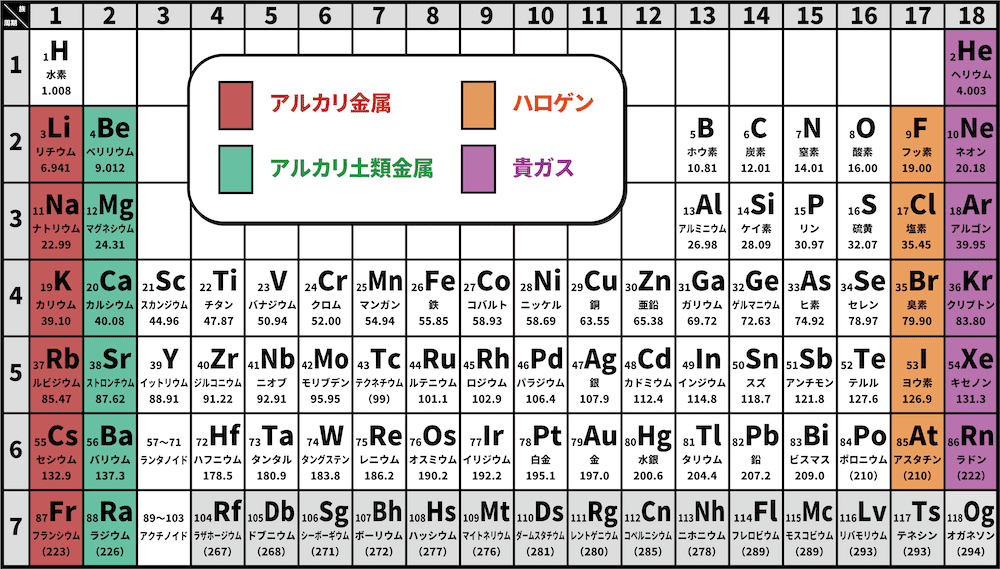
この族は次の元素で構成されています: ベリリウム 、Be (z = 4)。 マグネシウム 、Mg (12); カルシウム 、Ca (z = 20); ストロンチウム 、Sr (z = 38); バリウム 、Ba (z = 56);および ラジウム 、Ra (z = 88)。
反応性
アルカリ土類金属は 価殻 に 2 つの電子を持っているため、自然界では +2 の 酸化状態 でよく見られます (反応性も高く、カルシウム、ストロンチウム、バリウムの場合は、ファミリー 1A) の要素。

ベリリウムとマグネシウムは、それぞれの イオン化エネルギー により、グループ 2A の中で最も高い還元電位値 (したがって、最も低い酸化電位) を持ちます。他の金属の電位は アルカリ 金属に匹敵します。

ベリリウムを除いて、金属は水と接触すると 水酸化物 を形成し、その結果として 水素 ガスが発生する傾向があります。ただし、マグネシウムと水の反応は非常に遅く、不動態化金属酸化膜 (MgO) が形成されるため、プロセスが困難になったり、室温で他の物質と反応したりすることさえ困難になります。
酸素と接触すると、それらは塩基性酸化物を形成します(バリウムは、高圧および高温が維持されると 過酸化 バリウムを生成することもあります)。ハロゲン化物および窒化物(MX 2 、M 3 N 2 )。特にバリウム、カルシウム、ストロンチウムも、MH 2 タイプの 金属水素化物 を形成する傾向があります。

物理化学的性質
アルカリ金属と同様に、アルカリ土類金属は 電気陰性度 の値が低く ( ポーリングスケール によると最大 1.5 eV)、層の数が (下から上に) 減少するにつれて増加し、 イオン化エネルギー 値も低くなります。 (これも下から上に向かって増加します)。
ストロンチウム、バリウム、ラジウムは、最も多くの放射性同位体 (放射性 同位体 ) を含む金属です。ストロンチウムには 4 つの安定な天然同位体 (Sr-88 が最も豊富で約 83%) と 16 の放射性同位体 (Sr-90 はより長い) が含まれています。半減期: 29 年以上);バリウムには 7 つの安定な天然同位体と 15 の放射性同位体 (最も長く持続する Ba-133、半減期は 10.5 年) があります。ラジウムは、天然に安定な同位体を持たない唯一の物質であり、放射性同位体のみを持ちます(半減期が最も長いのは Ra-226 で、約 1600 年です)。
これらはすべて室温では固体であり、密に詰まった六方晶格子 (ベリリウムとマグネシウム)、面心立方構造 (カルシウムとストロンチウム)、および体心構造 (バリウム) を形成します。
ギャラリー