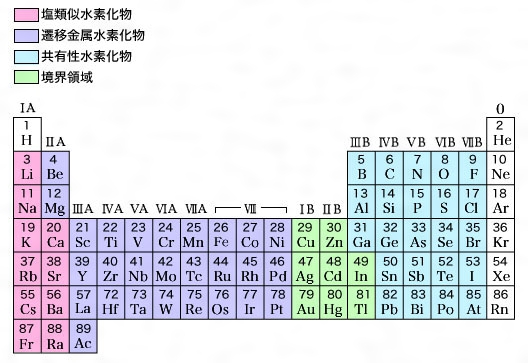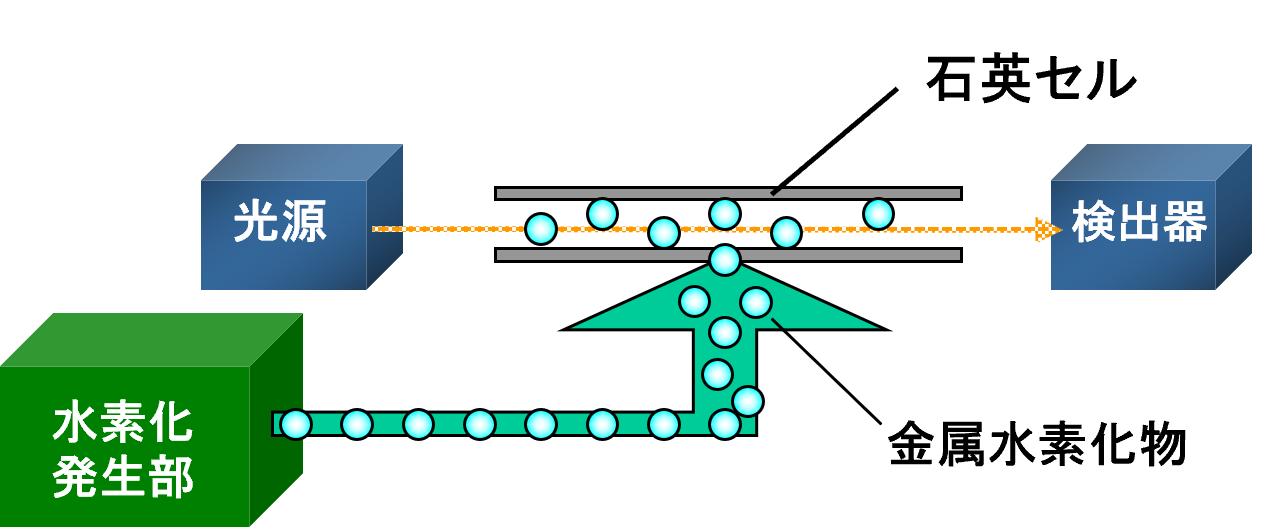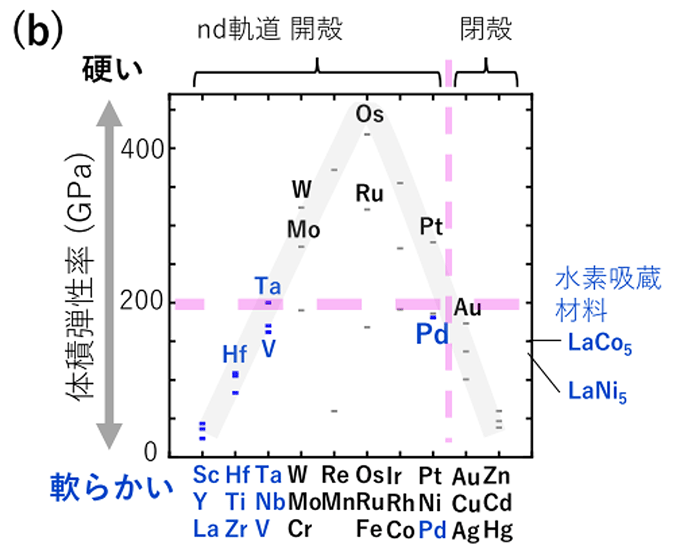
分子 内で最も 電気陰性度の 高い元素が 水素 (H) である 無機化合物 のグループは、 水素化物 と呼ばれます。水素化物は、確立する 化学結合 の種類に応じて、イオン結合、共有結合、金属結合に分類できます。
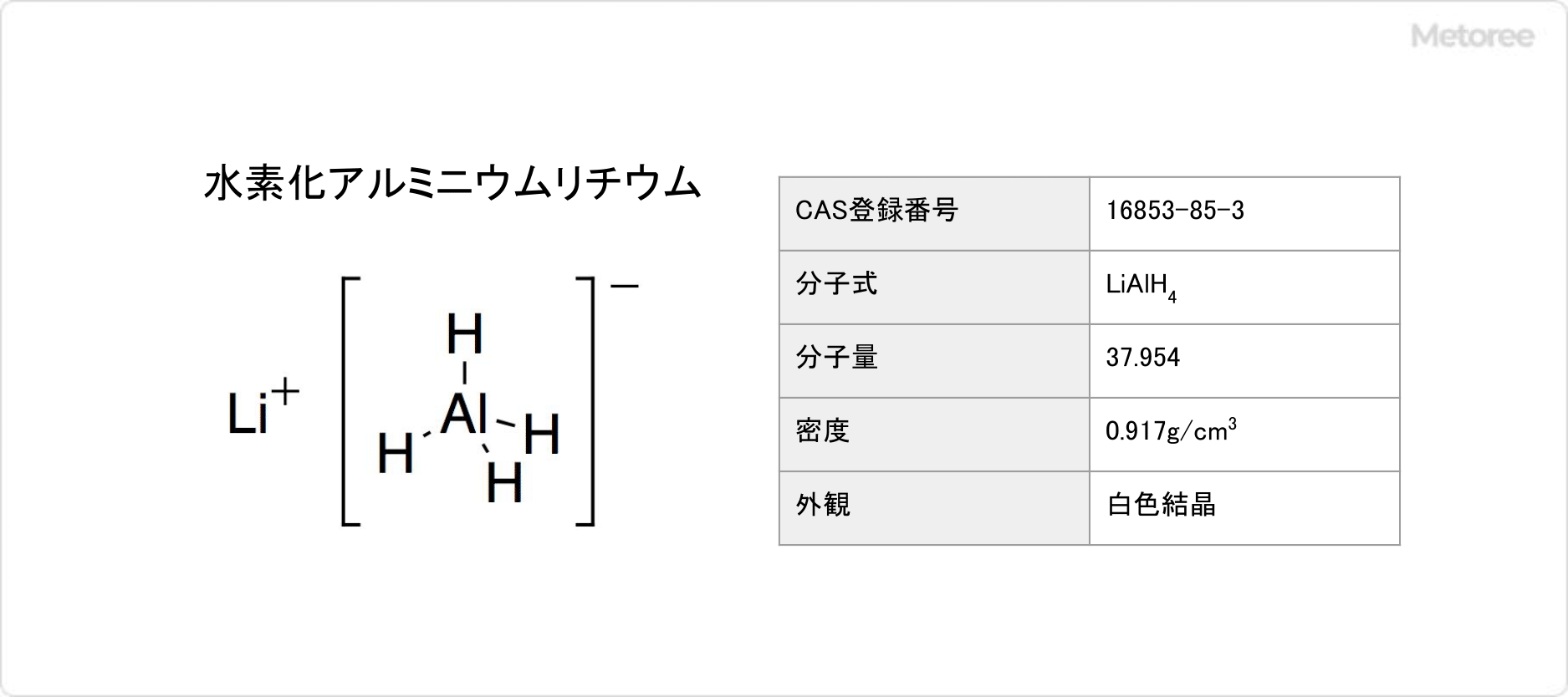

イオン性水素化物

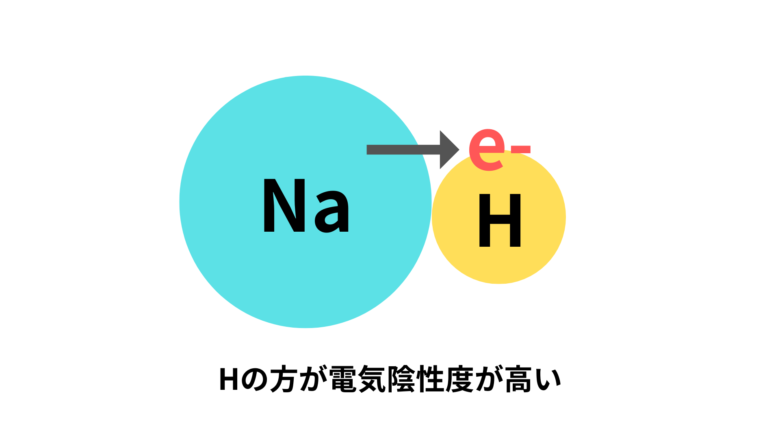
イオン性水素化物は、 アルカリ金属 および アルカリ土類 金属 (それぞれ 周期表 の 1A 族および 2A 族) に結合した水素によって形成されます。これらは固体の結晶性化合物で、融点が高く、 生成エンタルピーが 高く、水と反応して塩基を生成し、有機 溶媒 に不溶で、特に高温では強力な還元剤です。例:
- 水素化ナトリウム (NaH): 有機および無機合成 における還元剤として広く使用されています。
- 水素化カルシウム (CaH 2 ): 水と強く反応して水素ガスを放出します。一部の種類の溶剤の乾燥剤として広く使用されています。
共有結合性水素化物
共有結合(または分子)水素化物は、グループ 3A (13)、4A (14)、5A (15)、6A (16)、および 7A (17) の元素と ベリリウム (Be) に水素を付加することによって形成されます。その分子は共有結合しており、 ファンデルワールス型結合 によって結合されており、揮発性で融点と沸点が低いです。例:
- 水素化ベリリウム (BeH 2 ): ロケット燃料に広く使用されている物質で、 熱分解 (非常に高い温度で起こる分解反応) によって得られます。
- 水素化リン (PH 3 ): ホスフィン、ホスファン、またはホスパミンとも呼ばれます。可燃性ガスで、一般に魚が腐ったような不快な臭いがします。ペースト、錠剤、プレート、錠剤、農産物の製造によく使用されます。
- 水素化硫黄 (H 2 S) – 硫化水素: 特有の臭気 (腐った卵のような) を持つ腐食性ガスで、主に 石油化学産業 で使用されます。
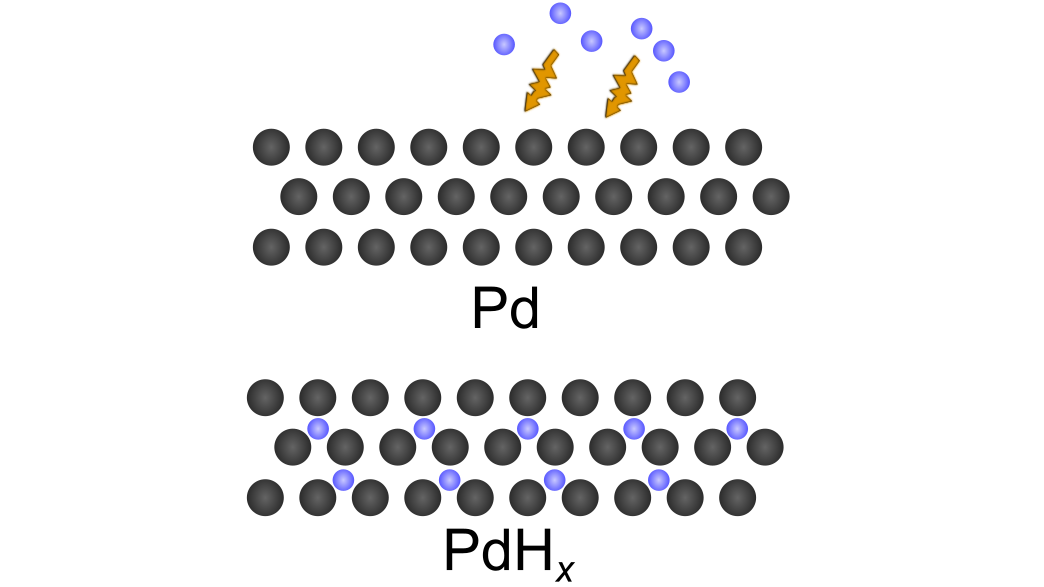
金属水素化物
水素は周期表の def ブロックの元素、 ランタニド および アクチニド と結合して水素化物を形成します。これらの化合物の物理的および化学的特性は一般に、それらを構成する金属の特性に近く、金属光沢、高い硬度、および良好な導電性を持ちます。これらは水と激しく反応し、水素と金属塩基を生成します。例:
- 水素化アンチモン (SbH3): 非常に不安定で有毒なガスで、金属合金の硬化に使用されます。
水素化物の正式な命名法は、式中のカチオンの名前を水素化物という用語に追加することによって与えられます。元。:
NaH – 水素化ナトリウム
非金属で構成される水素化物の中には、水中で非常に酸性の溶液を形成するものがあり、その結果、 塩酸 (HCl) などの別名が付けられます。さらに、水 (水素化酸素)、ボラン (水素化ホウ素)、シラン (水素化ケイ素) など、非メソッド名で知られるものもあります。
ギャラリー