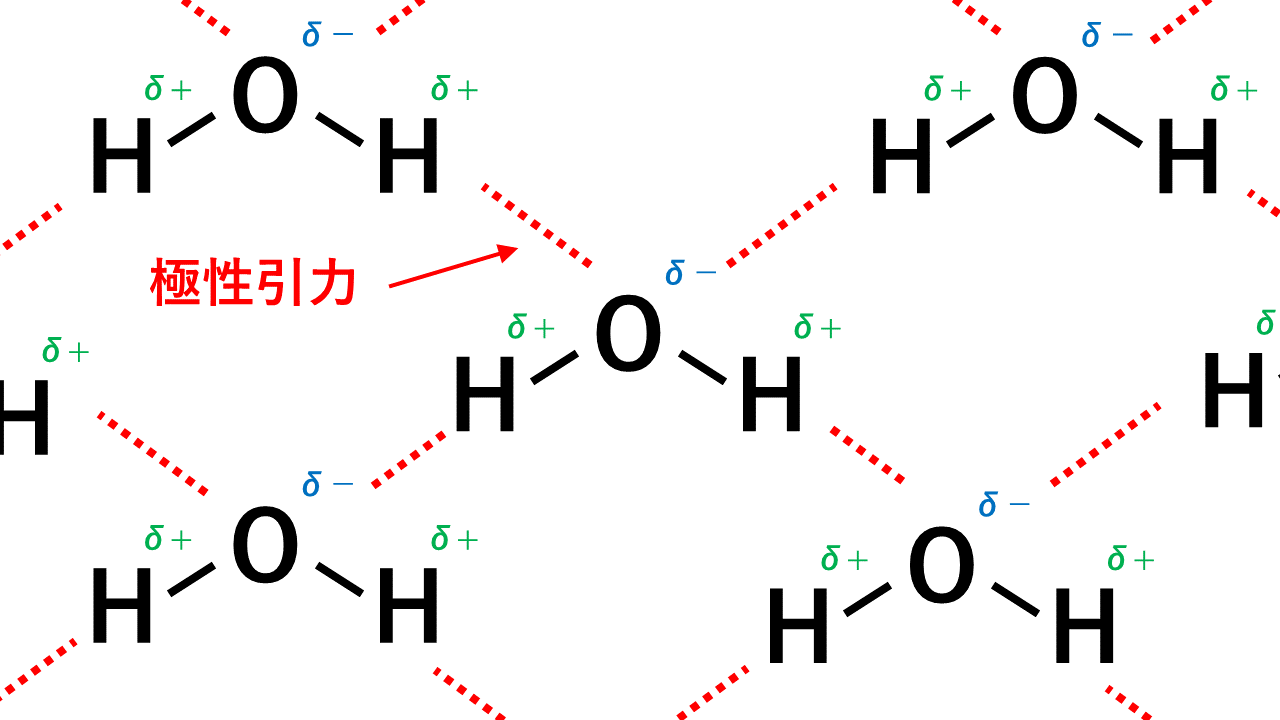
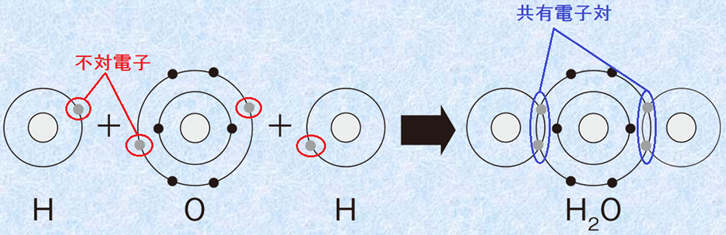
基本的に、物質内では性質の異なる 2 つの力が作用します。それらは 分子間力 、つまり 分子 間に作用し、 分子内力 はこれらの分子内で 2 つ以上の原子間に作用します。分子間力は、 水素結合 または ファンデルワールス 力 として簡潔に説明できます。分子内力は有名な 化学結合 であり、イオン結合、共有結合、金属結合などがあります。このテキストの目的は、分子内力、つまり化学結合に関連する側面を扱うことです。

間違いなく、今日でも原子間に働く力は、化学研究全体の中で最も興味深い側面の 1 つを表しています。これらの力の中で最も強いのは化学結合であり、 原子 の安定した結合に関与し、分子の形成をもたらします。これらは私たちが知っているすべての物質の構成塩基です。
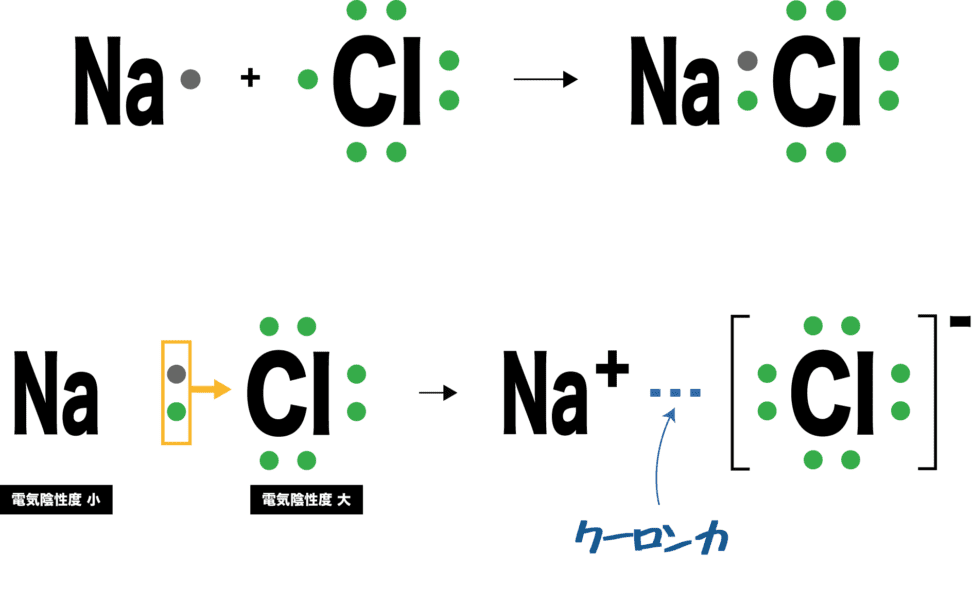
化学結合は、2 つ以上の原子間の相互作用、電子の供与、電子の共有、さらには電子の非局在化によって発生する相互作用を表します。これらの各プロセスは、化学結合の指定によって特徴付けられます。ただし、大部分の接続は特定のグループに 100% 属するために発生するわけではないことを強調することが重要です。何が起こるかというと、与えられた結合が一方のグループと他方のグループに中間的な性質を示すということです。しかし、この中間的な側面は化学文献ではめったに取り上げられず、問題の化学結合の主な分類が使用されます。
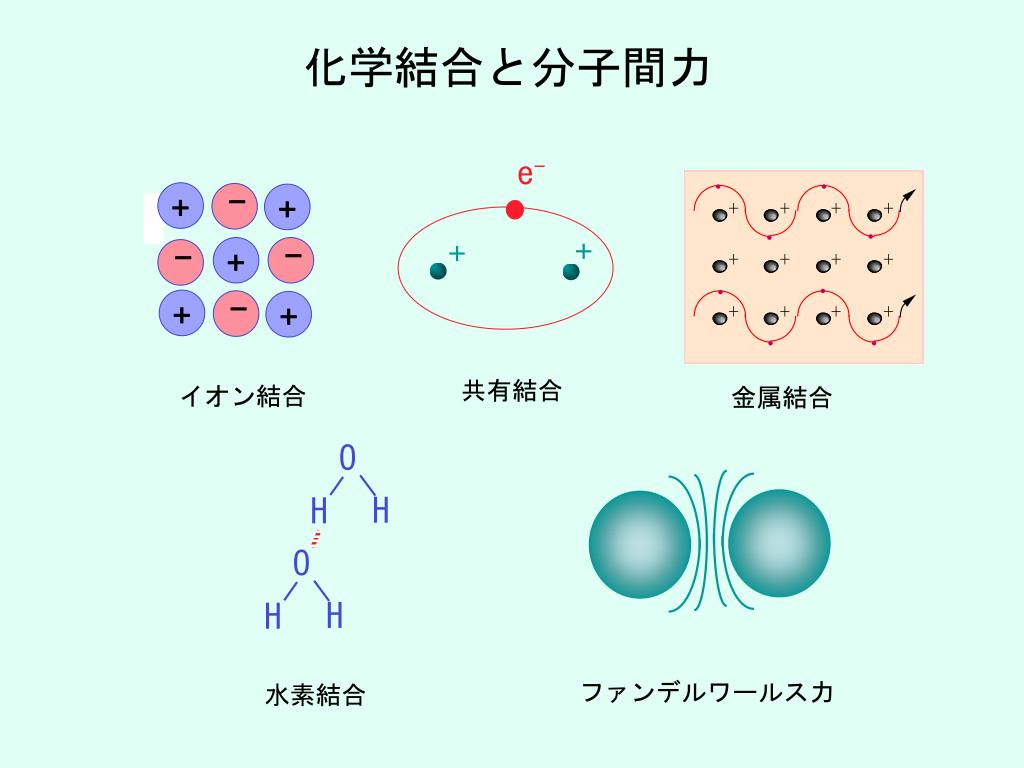
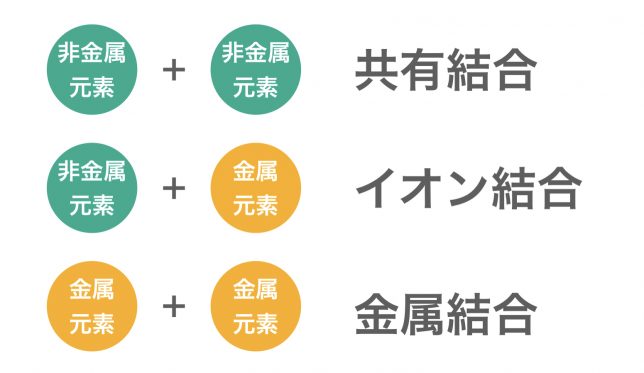
一般に、前述したように、電子の授受は 2 つの原子間で発生し、 イオン結合 と呼ばれる結合を特徴づけます。これに関連して、反対の電荷を持つ イオン を引き付ける静電気力が優勢になります。イオン結合は イオン性化合物 の形成に関与しており、金属原子と非金属原子の間で発生し、最初の原子による 電子 の供与と2番目の原子による電子の受け取りが行われます。

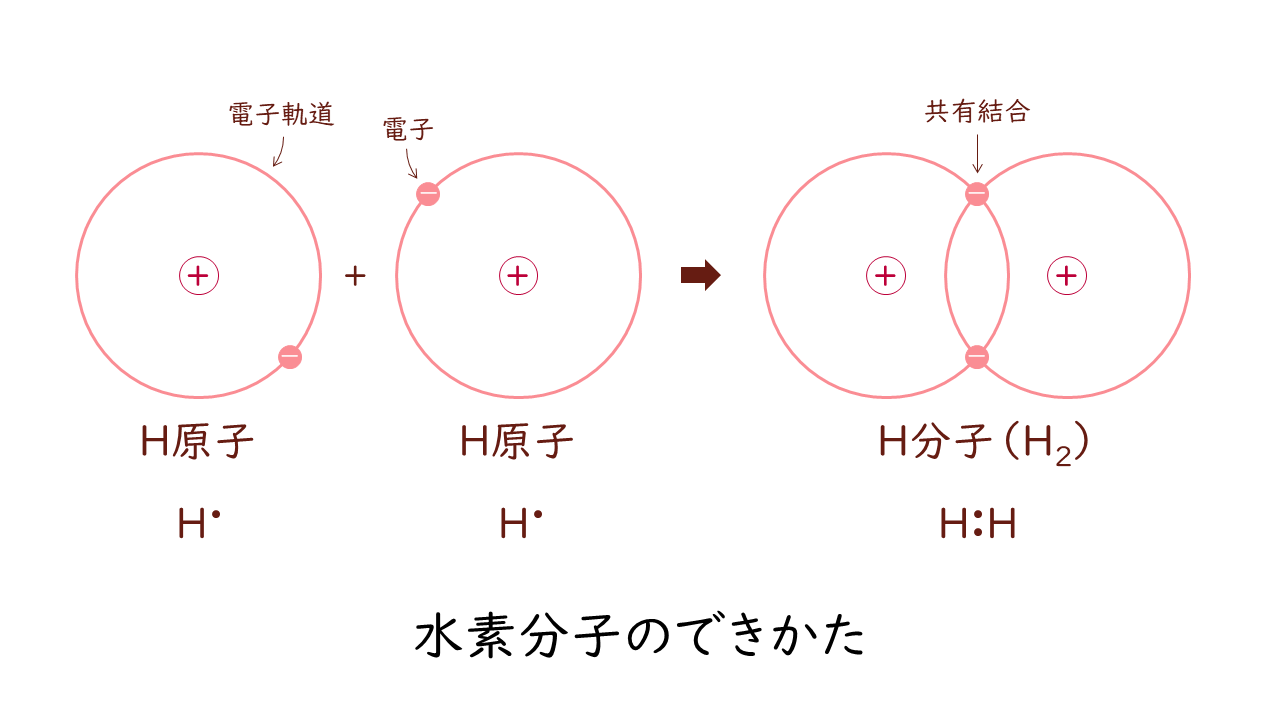
電子を獲得したり失う傾向が同じ 2 つの原子が結合すると、 共有結合が 形成されます。このような条件下では、完全な電子移動は起こりません。このプロセスでは、電子がペアで共有されます。常に 2 つの非金属原子間の共有結合は、極性 (2 つの異なる原子間の結合) または非極性 (2 つの等しい原子間の結合) の分子を構成するために、分子的性質の化合物を形成します。
参考文献:
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
サルデッラ、アントニオ。マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
ギャラリー