バリウム (記号 Ba ) は、第 2 族の アルカリ土類金属 または 希土類 に属する金属元素です。その名前はギリシャ語の「 barys 」に由来し、「重い」を意味します。この元素の原子番号は 56、質量数は 137.33 です。以下の 電子分布 があり、そこから 電子 が占める 6 つの層を持つ 電子圏 があることがわかります。
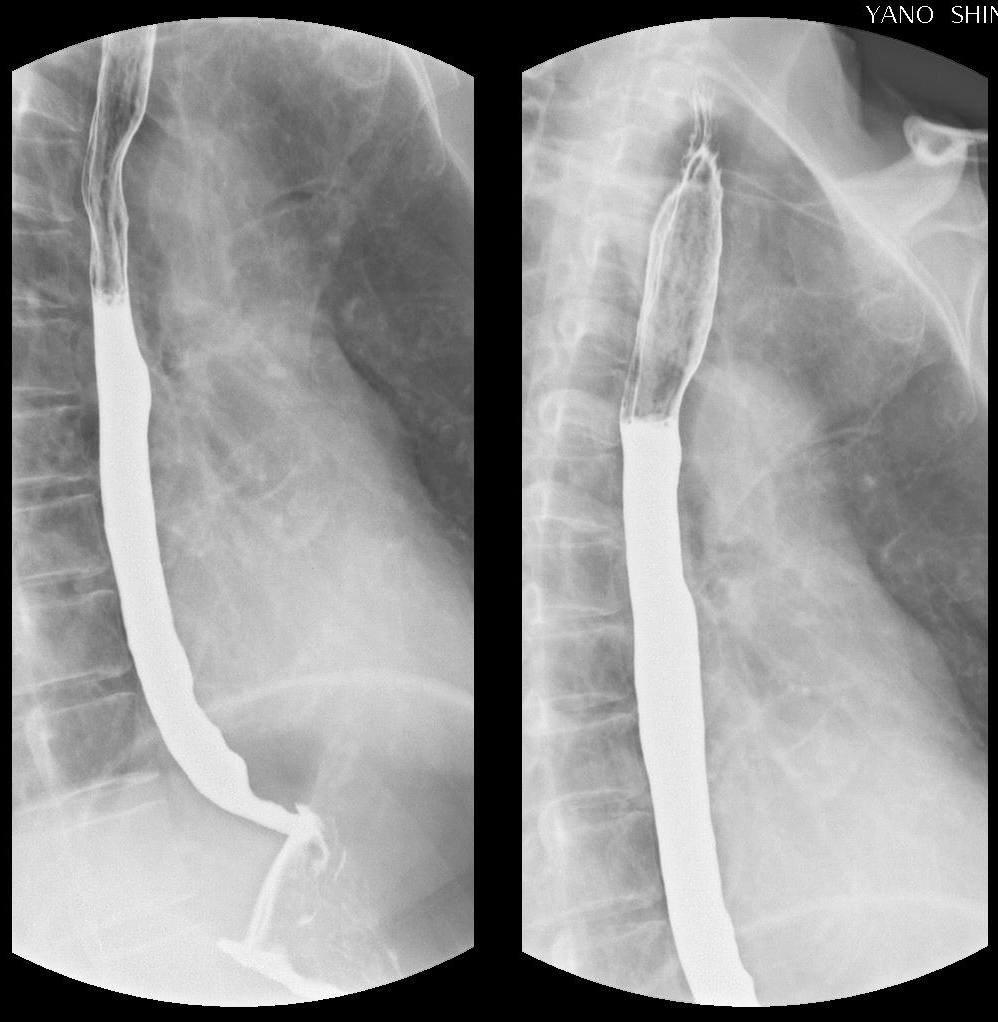
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 6 6s 2
![バリウム。写真: Matthias Zepper [パブリックドメイン]、Wikimedia Commons経由](wp-content/uploads/2010/03/b%C3%A1rio1-550x319.jpg)
バリウム。写真: マティアス・ゼッパー、 ウィキメディア・コモンズ経由

これは、英国の化学者ハンフリー デイビーによって、1800 年代頃に硫酸バリウム (BaSO 4 ) の 電気分解 プロセスを通じて発見および単離されました。このプロセスは、彼自身がその直前に開発し、すでに 金属 を含む他の塩に適用していたプロセスです。現在では、硫酸塩ではなく、塩化バリウム (BaCl 2 ) の電気分解によって得られるのが一般的です。
このアルカリ金属は鉱物埋蔵量でのみ見つかりますが、 酸化 力が高いため遊離形では存在せず、このため、たとえば 灯油 に浸しておかなければなりません。それは、酸化バリウムを シリコン で還元することによって、または前述のように商業的には塩化バリウムの電気分解によって、結晶化した硫酸バリウムまたは炭酸バリウム(BaCO 3 )である重晶石または重晶石から抽出されます。

その主な化合物は、 過酸化物 、塩素酸塩、硝酸塩、炭酸塩、硫酸塩、塩化物です。
これは毒性学的リスクが高く、その化合物は水に可溶化すると有毒になります。そのアプリケーションは無数にあります。以下にその一部のリストをチェックしてください。
- 油井の掘削に使用される物質中。
- ゴム(ゴム)業界では。
- 花火では緑色を帯びています。
- ガラス製造において。
- 塗料および顔料の製造。
- X線検査やシンチグラフィー検査における対照物質として。
- げっ歯類の 毒の場合。
- 電池の構成において;
- 乾燥剤として;
- 真空管の製造において。
- 蛍光灯の組成において。
- 製紙業界などで。
参考文献:
http://www2.fc.unesp.br/lvq/LVQ_tabela/056_bario.html
ギャラリー