パラジウム (Pd) は、 周期表 の第 10 族の 外側遷移金属 です。原子番号 Z = 46 (陽子と電子)、加重原子量は 106.42 u ( 同位体 Pd-102、Pd-104、Pd-105、Pd-106、Pd-108、および Pd-110 を使用して計算) を持ちます。それぞれ存在量の 1.02%、11.14%、22.33%、27.33%、26.46%、および 11.72%)。

 周囲条件下では、銀白色の外観と金属光沢を備えた固体です(
酸素
との反応性が低く、酸化しにくいため、空気にさらされてもこの外観は永久に残ります)。
周囲条件下では、銀白色の外観と金属光沢を備えた固体です(
酸素
との反応性が低く、酸化しにくいため、空気にさらされてもこの外観は永久に残ります)。
物理化学的性質

この金属は、中心面 (cfc) が立方体状に配置された結晶格子を持っています。最も一般的な 酸化状態 は +2 と +4 ですが、+1 と +6 も観察されます。 電気陰性度 は 、ポーリングスケール で 2.2 です。
密度は 12023 Kg/m3 と非常に高く、それぞれの融点と沸点の値は約 1550°C と 3140°C です。これは、格子配列が非常に安定していることを示しており、この構造を変更するには多量のエネルギーが必要です。融合プロセス。
また、熱(鉄とほぼ同じ伝導性)と電気(これも鉄とほぼ同じ伝導性)の優れた伝導体です。

発生と応用
パラジウムは、ほとんどの場合、 プラチナ または同じグループの別の金属と関連して自然界で発見されますが、その濃度はそれほど顕著ではありません。地殻では平均濃度が 0.01 ppm (地球 1 トンあたりのグラム数) です。
モリブデナイトやフェリモリブダイトなど、一部の鉱石には組成中に少量のパラジウムが含まれている場合があります。
主な埋蔵量はシベリア、カナダ、南アフリカで見つかり、他の鉱床はコロンビアとアラスカでも見られますが、これらは他の鉱床と同様に小規模であるにもかかわらず、採掘がより経済的に実行可能です。
主な用途は次のとおりです。
- 反応用の不均一系 触媒 としての使用(優れた水素吸着剤であり、石油成分の蒸留や自動車用触媒コンバーターの製造にも使用されます)。
- 電気機械接点(リレーなど)の製造。
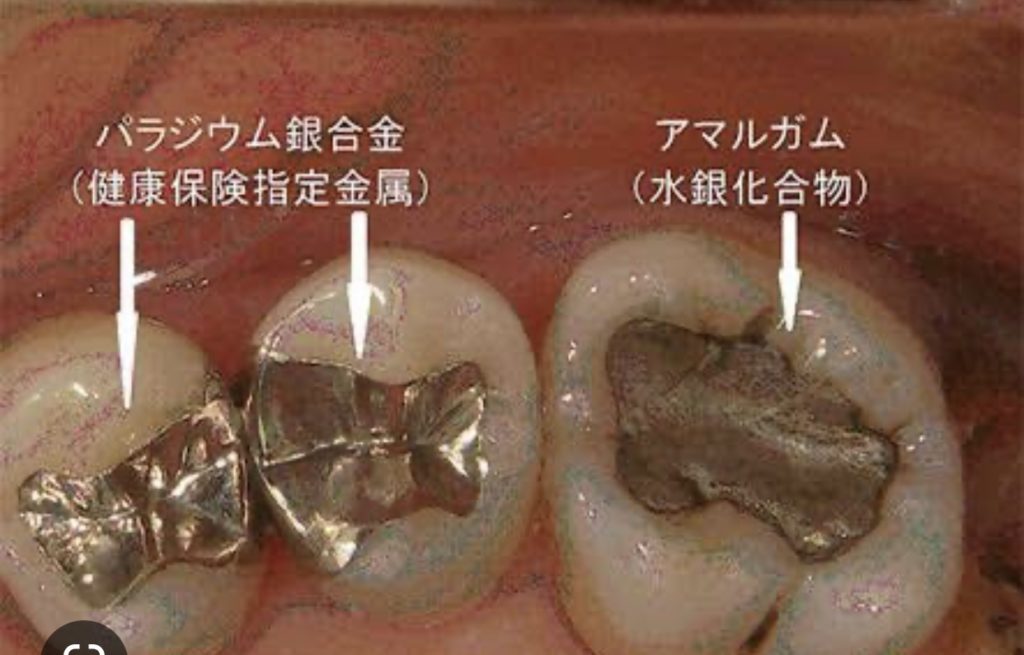
- 歯科では、歯の修復(補綴物)。
- 医学では、通常は手術器具の形で使用されます。
- 二塩化パラジウムの形で 一酸化炭素 を吸収します。その後、ガス検知器に使用されます。
- 金と(銀やニッケルなどの他の金属と)合金すると、「 ホワイトゴールド 」になります。
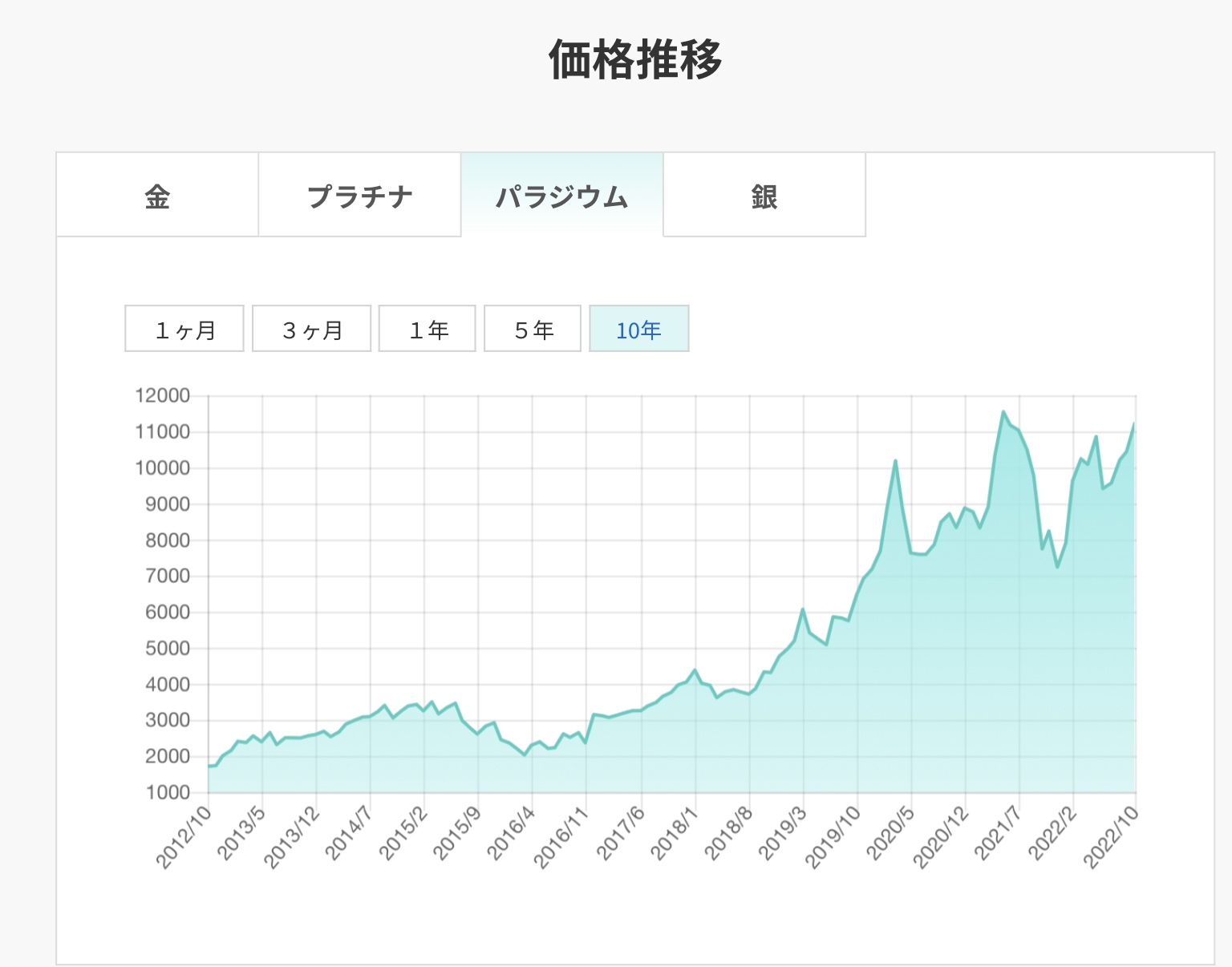
販売価格は、一般的に24金(実質的に純度の高い金)の販売価格の3分の1です。
参考文献:
http://nautilus.fis.uc.pt/st2.5/scenes-p/elem/e04695.html
(2011 年 6 月 9 日にアクセス)
http://www.mspc.eng.br/quim1/quim1_046.asp
(2011 年 6 月 9 日にアクセス)
ギャラリー