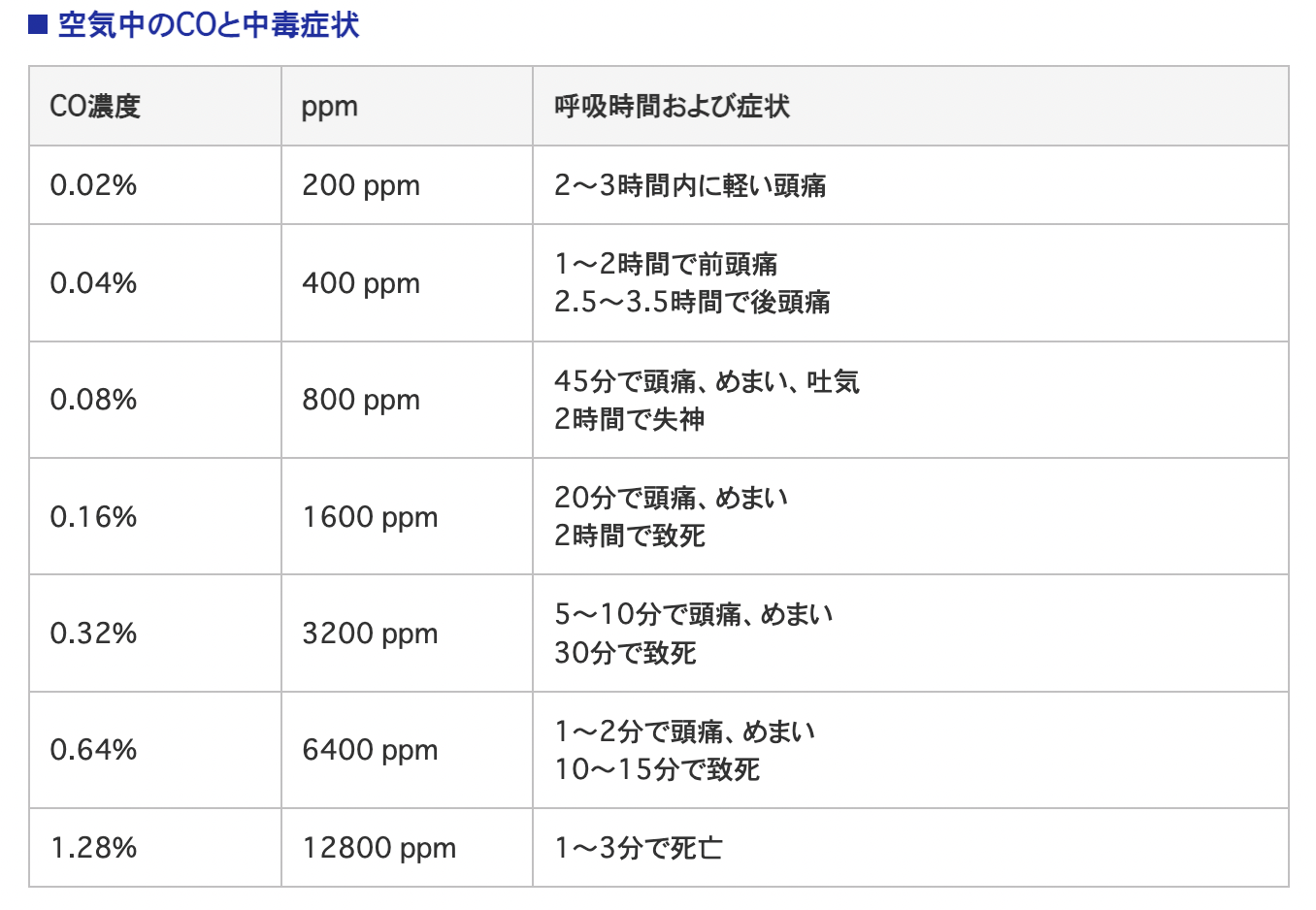
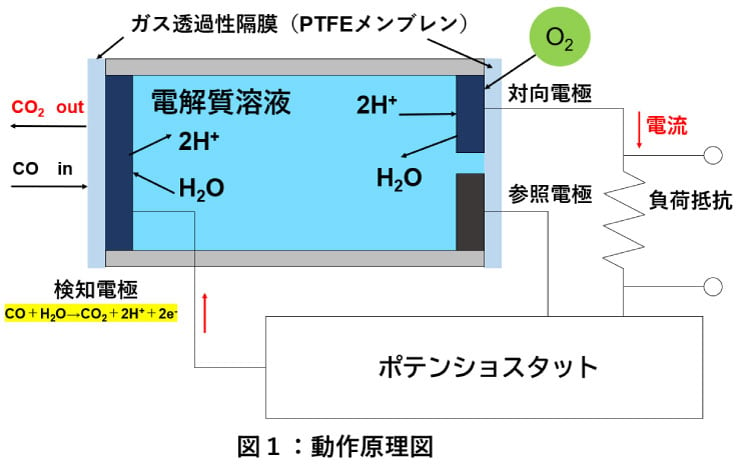
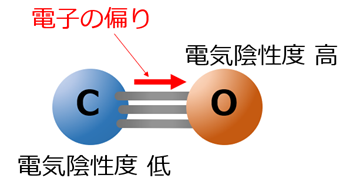
2CO + O 2 → 2CO 2
融点は -205.07 °C、 沸点 は -191.55 °C、密度は 1.25 kg m-3 (0 °C)、水 (30 mg L -1 ) および一部の有機物に部分的に可溶です。 クロロホルム 、エタノール、 酢酸 などの溶媒。一酸化炭素は 塩素 、 亜酸化窒素 、 アセチレン 、フッ素と混和性がなく、 金属 と反応すると有毒で可燃性のカルボニルを生成します。これは無色、無臭、わずかに可燃性のガスで、無臭ですが非常に有毒で、少量の濃度で吸入すると、頭痛、めまい、目の炎症、 視力 障害、手先の器用さの低下を引き起こします。中濃度では 神経系や心血管系 に問題を引き起こし、高濃度では窒息による死に至る可能性があります。

CO 分子は、 ヘモグロビン と非常に安定した化学結合を形成することによってカルボキシヘモグロビン (HbC) 分子 を形成し、 呼吸 過程での 酸素の 輸送を不可能にします。 ヘモグロビン に対する親和性は酸素の 200 倍以上です。さらに、CO 分子はミトコンドリアの酵素であるチトクローム C オキシダーゼを阻害し、血管周囲の酸化ストレスを増加させるほか、炎症作用があるため、濃度に関係なく吸入すると非常に有害です。さらに、光または熱の存在下で塩素 (Cl 2 ) と反応してホスゲン (COCl 2 ) を生成します。ホスゲンは、O 2 濃度が低い場所で プラスチック やその他の合成材料が燃焼するときによく発生する非常に有毒なガスです。
それは自然発生源または人為的発生源によって放出される可能性があります。自然放出には、火山活動、放電、 天然ガスの 放出が考えられます。

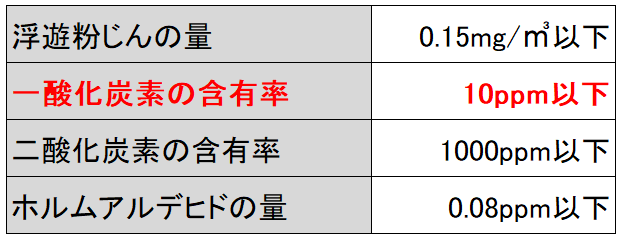
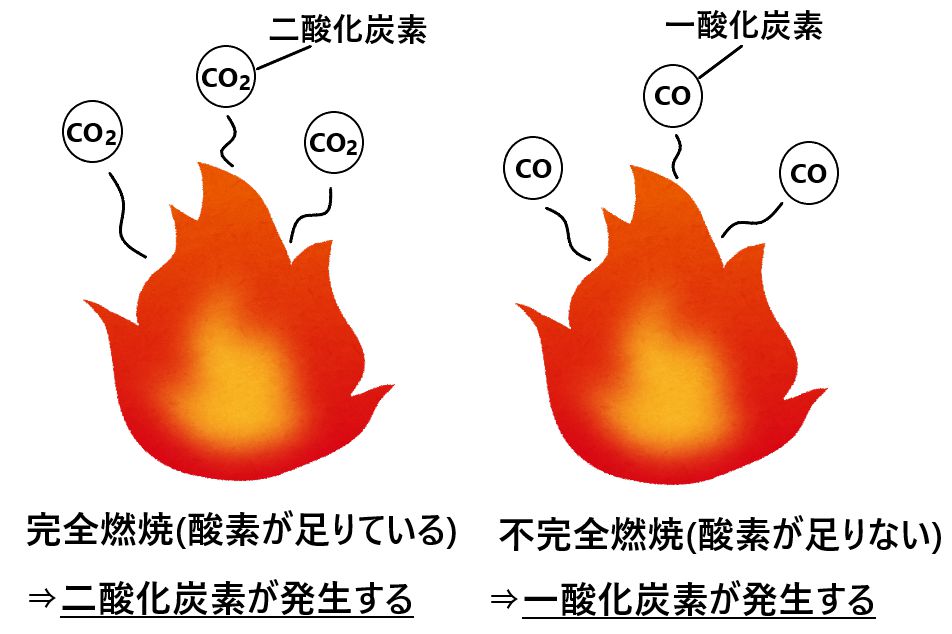
人為的排出物は、低酸素濃度または高温の環境における 石炭 、天然ガス、 石油 誘導体、 燃料 、 溶剤 、木材の不完全燃焼に関連しています。また、 大気 中、いわゆる揮発性 有機化合物 (VOC)、または水域に存在するさまざまな化合物の光化学酸化の生成物である可能性もあります。言及されたすべての発生源の中で、最も高濃度の CO が 化石燃料 の燃焼と森林 火災 によって放出されます。 CO は、大気質基準 (PQAr) で評価されるパラメーターの 1 つとして国家環境評議会 (CONAMA) のリストに載っています。CO は、保温性の向上に寄与するため、汚染ガスであり、 温室効果 の原因であると考えられています。
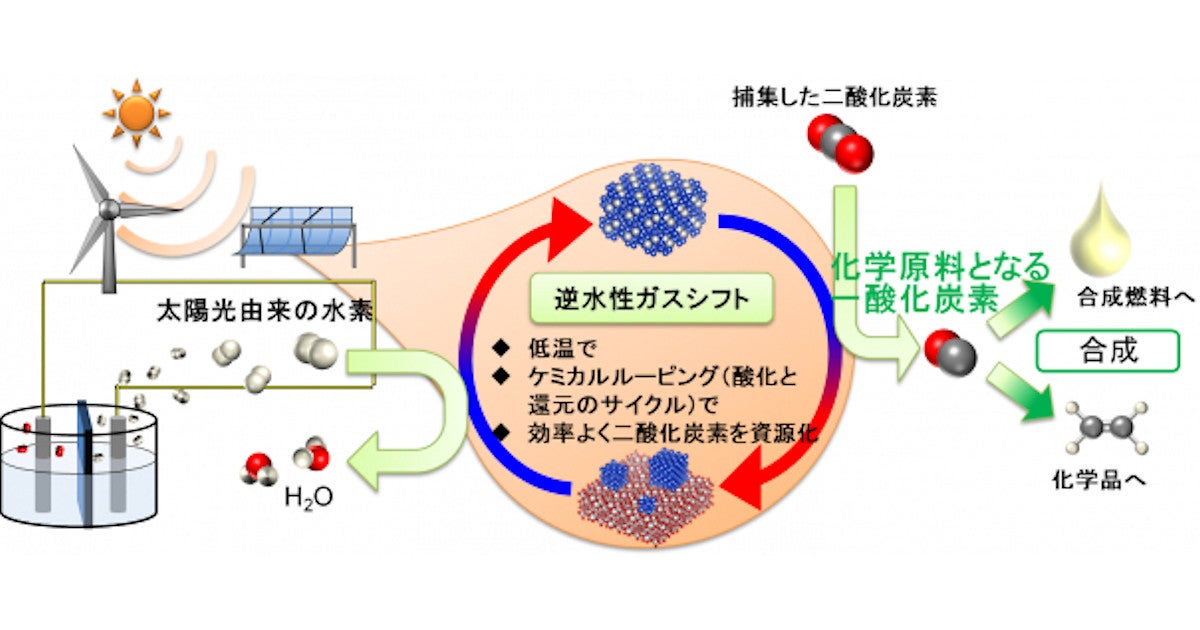
その用途に関しては、 第二次世界大戦 中、CO は 強制収容所 、より具体的にはガス室で使用され、数千人が死亡しました。現在、幸いなことに、CO の使用には他の目的があります。これは還元剤であるため、鉱石から 鉄 や ニッケル などのさまざまな金属を製造する工業プロセスでさまざまな化合物から酸素を除去し、水から 水素を 除去するため、CO 2 を生成します。さらに、酢酸、 メタノール 、 炭化水素 の合成にも応用されています。

参考文献
アトキンス、P.W.ジョーンズ、ロレッタ。化学の原理: 現代の生活と環境への疑問。単巻。第3版ポルトアレグレ:ブックマン、2006年。

Kotz、JC 一般化学と化学反応。第 1 巻、第 9 版、Cengage Learning、2015 年。
ガルバン、AC さまざまな温度と圧力でのグリコールへの メタン と 二酸化炭素 の溶解度の実験的研究、および化学ポテンシャルを適用した溶解度のモデル化。博士論文。 UNICAMP、カンピーナス、2011 年。

ティトとカント。日常的なアプローチにおける化学。単巻、パート C – 有機化学。編集者サライバ、2005 年。
ギャラリー