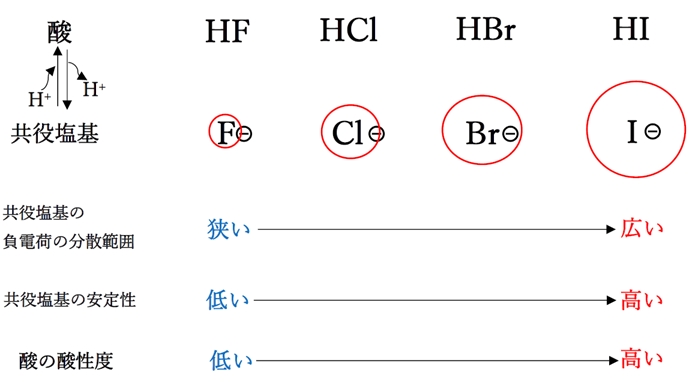
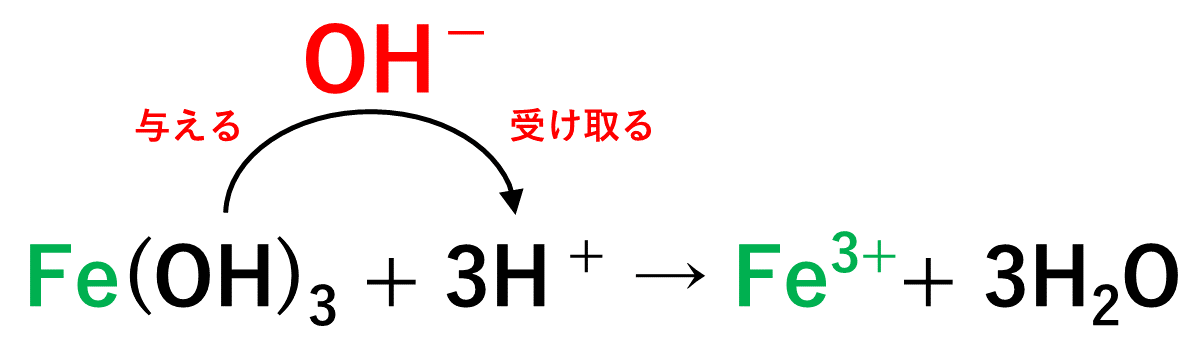
中和反応 の性質を理解することは、酸と塩基を含む アレニウス理論を 理解するための基礎です。中和反応は、酸と塩基が化学反応して塩と水を形成する反応です。たとえば、次のような中和があります。

HCl + NaOH → NaCl + H2O
しかし、分子を酸または塩基に分類するにはどうすればよいでしょうか?この分類が単に明らかではないようにするには、どのような基準を使用できますか?最も単純化された、しかし非常に有用な酸と塩基の定義の 1 つは、スウェーデンの化学者 スヴァンテ アレニウス によって提案されました。これには、電解解離のプロセスが含まれます。

アレニウスにとって、酸とは、水溶液中で解離して 水素 イオン (H + ) を放出する 物質 です。塩基は、水性媒体中で解離し、 水酸化物 イオン (OH – ) を放出することができる物質です。したがって、分子を酸またはアレニウス塩基に属するものとして特徴付けるには、 溶媒である水 (水性)が必要であることがわかります。
酸に関しては、アレニウス解離は次のように図式化できます。
HCℓ (g) + H 2 O (ℓ) → H 3 O + (aq) + Cℓ – (aq)
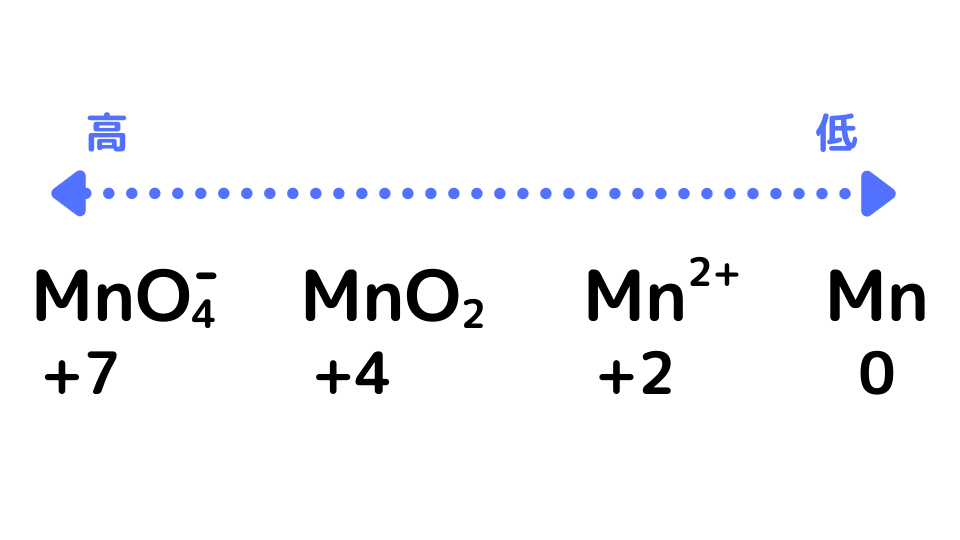
H + イオンの放出が観察され、これが水分子と協調して反応し、イオン (H 3 O + ) を形成します。
塩基に関して、アレニウス解離は次のように簡略化して図式化できます。
NaOH → Na ++ OH –

基本分子内にすでに存在するイオン間に分離が見られ、その分類に関与するこれらのイオンの 1 つが水酸化物イオン (OH – ) です。
中和は、次に示すように、酸からの H + イオンと塩基からの OH – イオンの間の反応による水分子の形成です。
H + (水溶液) + OH − (水溶液) H 2 O

このプロセスは、塩と一緒に水分子を生成する中和反応についてアレニウスによって与えられた定義を補完します。塩基から来る陽イオンは酸から来る陰イオンと化学反応して塩を生成します。このテキストの冒頭の例では、形成される塩は、ナトリウム イオン (塩基に由来するプラスの性質) と塩化物イオン (酸に由来するマイナスの性質) から生成される塩化ナトリウムです。
参考文献:
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ギャラリー