ポンデラルの法則は 、化学反応一般を支配する実験法則であり、これらの反応の成分の質量に相対的です。それらは基本的に、あらゆる化学反応における反応物質と生成物の質量を関連付ける法則です。

化学反応の法則は、ポンデラルの法則と体積法則の 2 つのグループに分けられるため、 ゲイ リュサックの法則は ポンデラルの法則には含まれません。

思案法は 18 世紀末に出現し、当時の数人の化学者や学者がその精緻化に積極的に参加しました。以下では、それぞれをより具体的に見ていきます。

質量保存の法則 (ラヴォアジエの法則)
「 自然界では、何も創造されず、何も失われず、すべてが変化します。 』(アントワーヌ・ラヴォアジエ)
1774 年頃、フランスの化学者 アントワーヌ ローラン ラヴォワジエ (1743 – 1794) は、化学反応における質量の変化を定量化し検証するために、妻のマリー アンヌ ラヴォワジエの協力を得て、 化学物質 の 燃焼 と 焼成 に関する実験を実施しました。 。ラヴォアジエ夫妻が行った実験の基礎となったのは、ロシアの化学者ミハイル・ロモノーソフによる1760年の実験だった。
この実験により、ラボアジエは、空気にさらされた金属をか焼すると、出発金属よりも重い金属 酸化 物が形成されるが、石炭などの有機物の燃焼を行う場合には、同様に空気にさらされることに気づくことができました。 、最終質量は開始質量よりも小さくなりました。その後、ラヴォアジエは、さまざまな化合物を焼成して燃焼させるときに起こる反応についてさらに多くの情報を取得し、燃焼反応を活性化するガスが 酸素 (しばらくしてラヴォアジエ自身がこのガスに付けた名前です) であることを観察しました。実験により、燃焼および焼成反応は酸素と他の成分の組み合わせによる化学反応の結果であると推測できました。閉じた系で実験を行うことで、か焼や燃焼反応に積極的に関与するガス状反応物や生成物を含む、反応物や生成物の質量をより正確に測定することが可能になったラヴォアジエは、実施された実験で観察されたばらつきは次のように結論付けた。開放系では、反応物質とガス状生成物の質量を合計すると、材料が受ける燃焼および焼成反応の開始時と終了時で一定でした。
ラヴォアジエの法則により、閉鎖系で行われる化学反応では、質量は反応の開始から終了まで一定のままである、つまり、反応物の質量の合計は、反応物の質量の合計に等しいと結論付けることができます。得られた製品の質量。
m (反応物) = m (生成物)
当初提案された形式のラヴォアジエの法則は、現在、 核反応 にのみ適用されるわけではありません。これらの反応には、反応物核の初期質量の変化に加えて、反応物核の突然変異が存在する核変換が含まれるためです。 、このタイプの反応の生成物の核の最終質量よりも常に大きくなります。

一定または定義された比率の法則 (プルーストの法則)
「 あらゆる物質はその組成において質量比が一定であり、それらが反応して形成される割合も一定です。 』(ジョゼフ・ルイ・プルースト)
フランスの化学者で薬剤師のジョゼフ・ルイ・プルースト (1754 – 1826) は、炭酸 銅 の組成に関連する実験を行った際、方法、起源、または調製プロセスに関係なく、その組成中の化学元素の割合は常に一定であると結論付けました。同じ。この実験は、プルーストが 1794 年または 1797 年 (入手可能な文献により日付にばらつきがあります) に、 定比例の法則 、または知られているように プルーストの法則 を提案するきっかけとなりました。
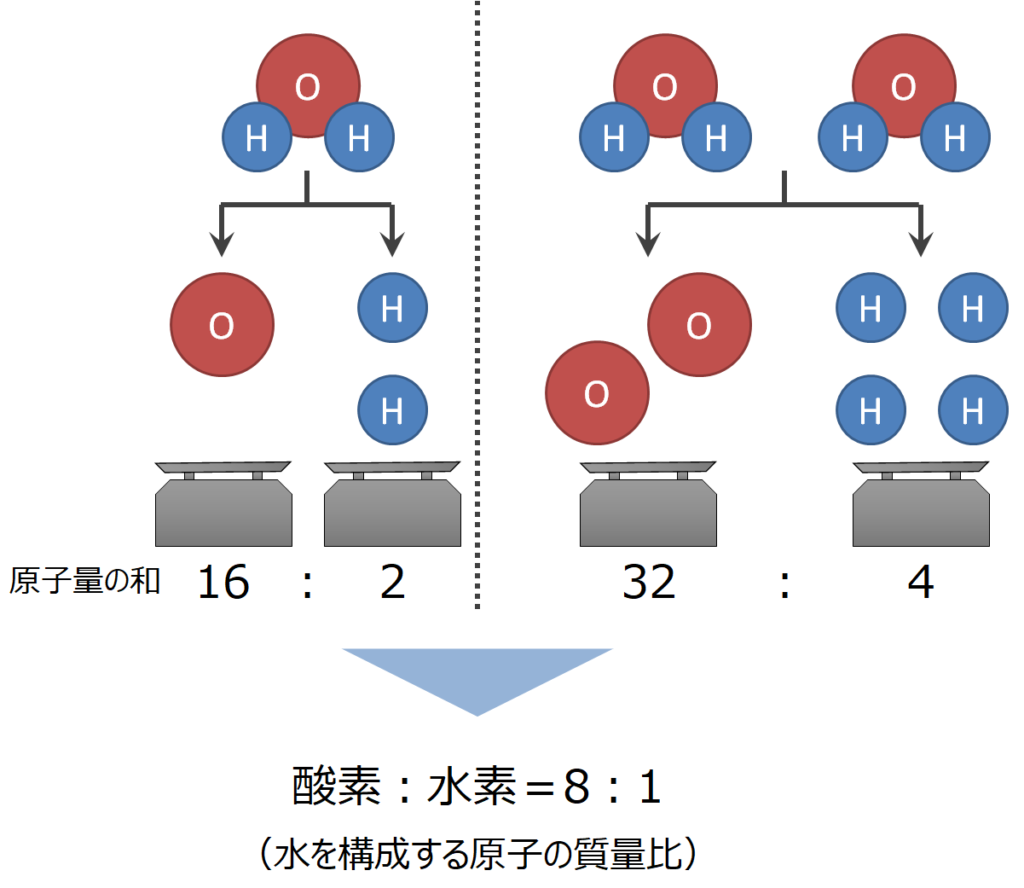
純粋な物質 のみを使用して実行された実験により、プルーストは、反応に関与する反応物と生成物の両方の質量が常に一定の比率を持ち、これは量に依存しないことを検証することができました。たとえば、次のとおりです。
H 2 + 1/2 O 2 → H 2 O
2g+16g→18g
0.4g+3.2g→3.6g
上記の例では、水サンプルには組成中に常に 11.1 質量%の 水素 と 88.9 質量%の酸素が存在すると結論付けることができます。反応物の質量の合計が生成物の質量の合計に等しいこと、また、複数の反応物が 1 つの生成物を形成している場合でも、それらの比率は常に一定であることを観察することもできます。

倍数比例の法則 (ダルトンの法則)
「 2 つの元素が 2 つ以上の異なる複合物質を形成するとき、一方の質量が一定であれば、他方の質量は小整数の関係で変化します 。」 (ジョン・ダルトン)
ジョン・ダルトン (1766 – 1844) はイギリスの化学者、気象学者、物理学者であり、いくつかの理論を生み出し、 現代原子理論の創始者 です。ダルトンは、化学反応の反応物質と生成物の質量に焦点を当てた実験を実行することにより、ある元素の固定質量が 2 番目の元素の異なる質量と結合して、次のような異なる化合物を形成する多重比率理論を作成しました。
一酸化炭素 : 1C + 1/2 O 2 → 1 CO
二酸化炭素 : 1C + 1 O 2 → 1 CO 2
最初の反応では、1:1 の比率で反応が見られます。つまり、1 つの炭素原子に対して 1 つの酸素原子が使用され、反応生成物は一酸化炭素になります。 2 番目の反応では、炭素の量は維持されますが、酸素の割合が 2 倍になり、1:2 の比率で行われ、二酸化炭素が生成されます。
この法則の効果的な適用を実証する文献で最も一般的な例の 1 つは、窒素によって形成される酸化物など、さまざまな 酸化物 の形成です。
| 窒素 | 酸素 | 酸化物が形成される | 割合 |
| 28g | 16g | N2O | 2:1 |
| 28g | 32g | N2O2 | 2:2 |
| 28g | 48g | N2O3 | 2:3 |
| 28g | 64g | N2O4 | 2:4 |
一般に、次のように定義できます。
A+B→C
m
a
+ m
b
→ m
c
A + B’ → C’
m
a
+ m’
b
→ m’
c
反応物の 1 つの質量を一定に保つと、他の反応物の質量と生成物の質量は変化します。
参考文献:
サントス、WLPdos。 MOL、G. de S. Química Cidadã: 第 2 巻: 中等教育。第2版サンパウロ:AJS、2013年。
フォンセカ、MRM da。化学 2.1.編サンパウロ:アティカ、2013 年。
http://www.portalmedquimica.com.br/downloads/Leis%20ponderais-Parte%2001-pdf.pdf
http://www.profpc.com.br/Exerc%C3%ADcios%20de%20Qu%C3%ADmica/Setor%20Gama/Gama%20-%20M%C3%B3dulo%2013.pdf
https://acervodigital.unesp.br/bitstream/123456789/41532/6/2ed_qui_m4d8_tm01_box3.pdf
https://acervodigital.unesp.br/bitstream/123456789/41532/7/2ed_qui_m4d8_tm01_box4.pdf
http://allchemy.iq.usp.br/metabolizando/beta/01/jdalton.htm
ギャラリー
















.png?resize=636,418&ssl=1)


