ジョゼフ・ルイ・ゲイ=リュサックは、ガス、水の組成、アルコールと水の混合物の挙動に関する研究で有名なフランスの化学者兼物理学者で、後者はアルコールの体積を表すゲイ=リュサック・スケール(°GL)を生み出しました。

彼の研究の中で、気体システムの理解に対する非常に重要な貢献は、一定の体積に閉じ込められた気体の圧力はその温度に比例するという結論でした。数学的言語では、これは次と同等です。
ここで、P は通常、圧力と T 温度を表すために使用されます。任意の定数 k を使用して、この比例関係を等式に変換して関係を書くことができます。
原則として、この定数は各ガスについて実験的に決定する必要があります。ただし、同じ初期条件 (圧力、温度、体積) にさらされた 2 つのガスは同じ k を持つことが観察されており、これは両方のシステムが温度変化に対して同様に応答することを意味します。これは、すべてのガスの挙動をより一般的な法則で記述できる可能性を示す最初の提案です。
/GettyImages-172212254-5c283eaac9e77c00016f1579.jpg)
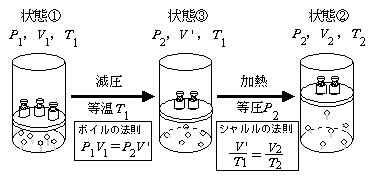
定数 k にはガスに関する情報を含めることができますが、システムの将来の状態を予測する場合には不便です。ただし、この問題は、体積が一定に保たれた 等積変換 を受けた気体の初期状態と最終状態の間の関係を確立することによって克服できます。
初期状態では次の価値があります。
最終状態でも、同様の方法で次のようになります。
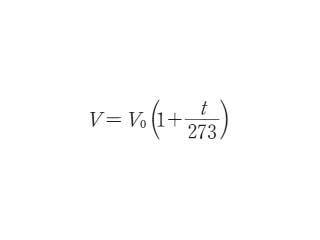
このタイプの変換では定数 k は変化しないことに注意してください。そのため、項を等価にして最も有用な法則形式を取得できます。
ゲイ・リュサックの法則 は次のように言えます。
等容性変換の場合、ガスの圧力と温度の比率は前後で等しくなります。
温度に応じて圧力がどのように変化するかを調べたい場合は、次のように書くことができます。

温度が変化すると圧力も同じ割合で変化すると結論付けることができます。たとえば、特定の変換で温度が 2 倍になると考えてみましょう。すると、次のようになります。
温度が2倍になると、圧力も2倍になります。温度は常にケルビン (K) 単位で使用する必要があることに注意してください。
次に、温度を半分に下げるとどうなるかを見てみましょう。

圧力も半分に下がります。この観察は、物質の体積と量が一定である変態を起こすあらゆる理想気体に当てはまります。代わりに圧力を変化させることにした場合、予想どおり、温度も同じ割合で変化に追従します。
ゲイ・リュサックの法則は、等積体変換を研究するための有用な関係を確立します。さらに、研究された方程式は、理想気体の法則を開発するための基礎を提供します。
ギャラリー