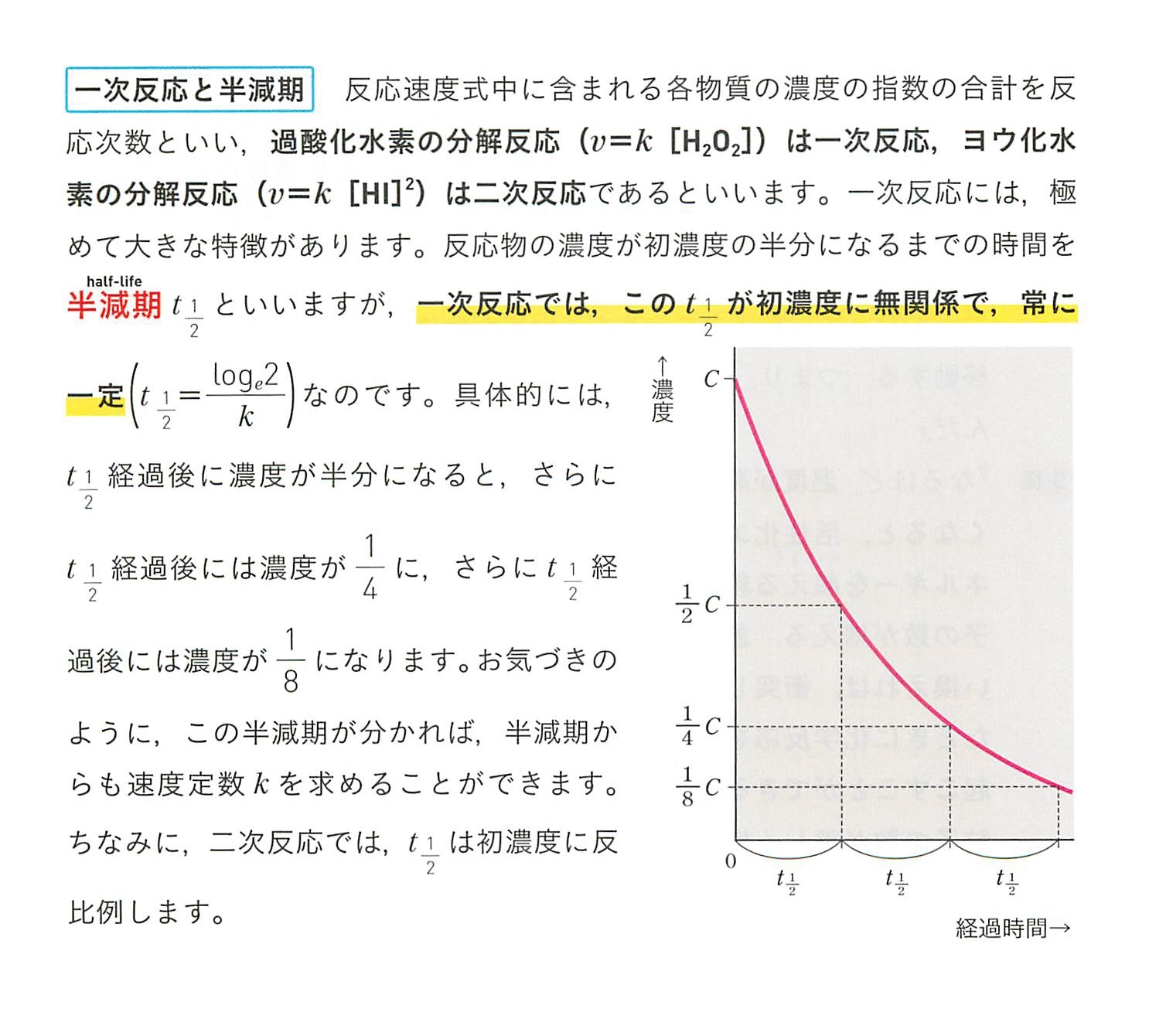
化学反応速度論 では、反応が起こる速度とそれを変化させる要因を研究します。動力学の研究を支配する理論は 衝突理論 です。この理論は、反応を開始するにはエネルギーが必要であり、そのエネルギーは系内の原子または分子間の衝突によって得られることを説明します。これらの衝突は効果的である必要があり、効果的であるためには正面衝突である必要があります。媒質の濃度が高いほど、より多くの衝突が発生し、その結果、より多くのエネルギーが得られますが、その逆も同様です。反応が始まるのに必要なエネルギー量を 活性化エネルギー といいます。活性化エネルギーは、反応を開始するために必要な最小エネルギーとして化学的に定義されます。

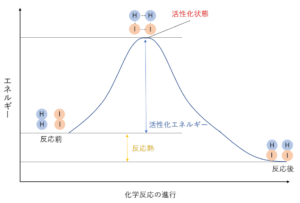
以下に化学反応のグラフを示します。

グラフでは、活性化エネルギーがグラフの最高点 (活性化された複合体) までの反応物の経路であることがわかります。反応のこの時点は最もエネルギーが高く、反応物と生成物が共存する反応の瞬間です。この時点以降、製品が形成されます。反応物質が活性化複合体を形成するまでの経路 ( 活性化エネルギー ) が長ければ長いほど、反応の発生にかかる時間も長くなることを理解する必要があります。反応速度に影響を与える可能性のある要因には、温度、圧力、濃度、接触表面、そして最後に触媒と抑制剤があります。
- 温度: 温度が上昇すると、反応速度の上昇が促進されます。
- 圧力 : 圧力が増加すると、反応速度が増加します。
- 濃度: 濃度が増加すると、反応物質間の衝突が増加するため、反応速度が増加します。
- 接触面: 一方の反応物が固体で、もう一方が液体の場合に影響します。固体の粒子サイズが小さいほど、化学反応は速くなります。
- 触媒: 生成物の生成を妨げたり、反応で消費されたりすることなく、化学反応の速度を変化させる (増加させる) 物質です。
- 阻害剤: 触媒のような働きをしますが、反応速度を阻害する、つまり遅くする効果があります。

ギャラリー