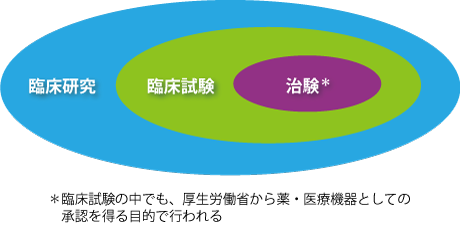
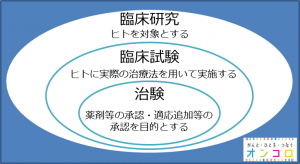
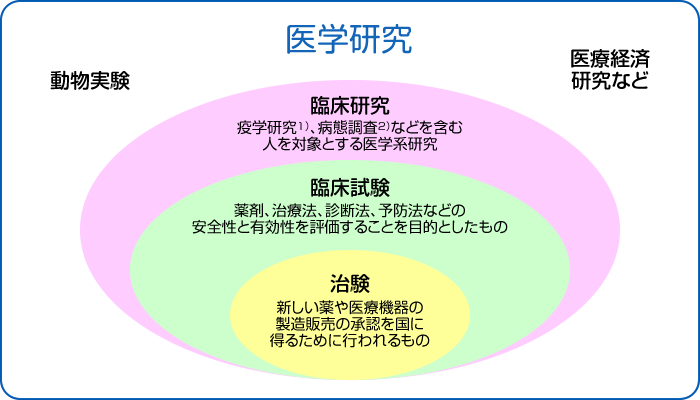
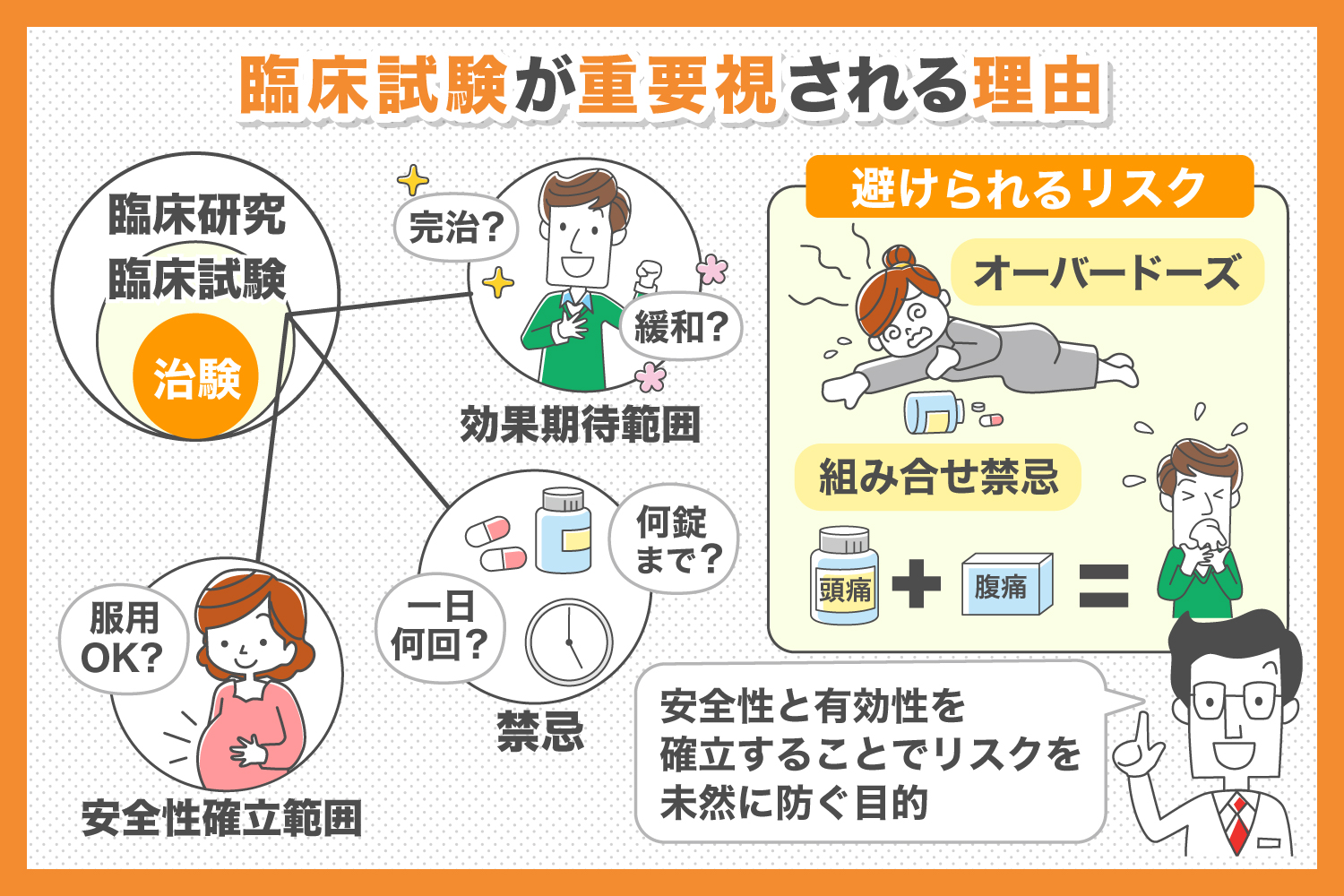
医薬品の臨床的、薬理学的、または副作用を発見したい場合、 臨床試験が 使用されます。臨床試験は、薬が体内でどのように吸収、分布、排泄されるかを観察することにより、薬の安全性と有効性を検証するためにも使用されます。
薬を開発するにはいくつかの手順を踏む必要があります。
1 つ目は研究段階で、研究対象の病原体に対する体の免疫応答がどのようなものであるかを発見します。開発する薬のターゲットを探している。
第 2 段階は前臨床試験で、薬理学的安全性が評価され、生物学的効果または薬理学的効果が発見または確認されます。この段階では、研究中の薬物の毒性作用も特定されます。

説明写真:joker1991 / Shutterstock.com
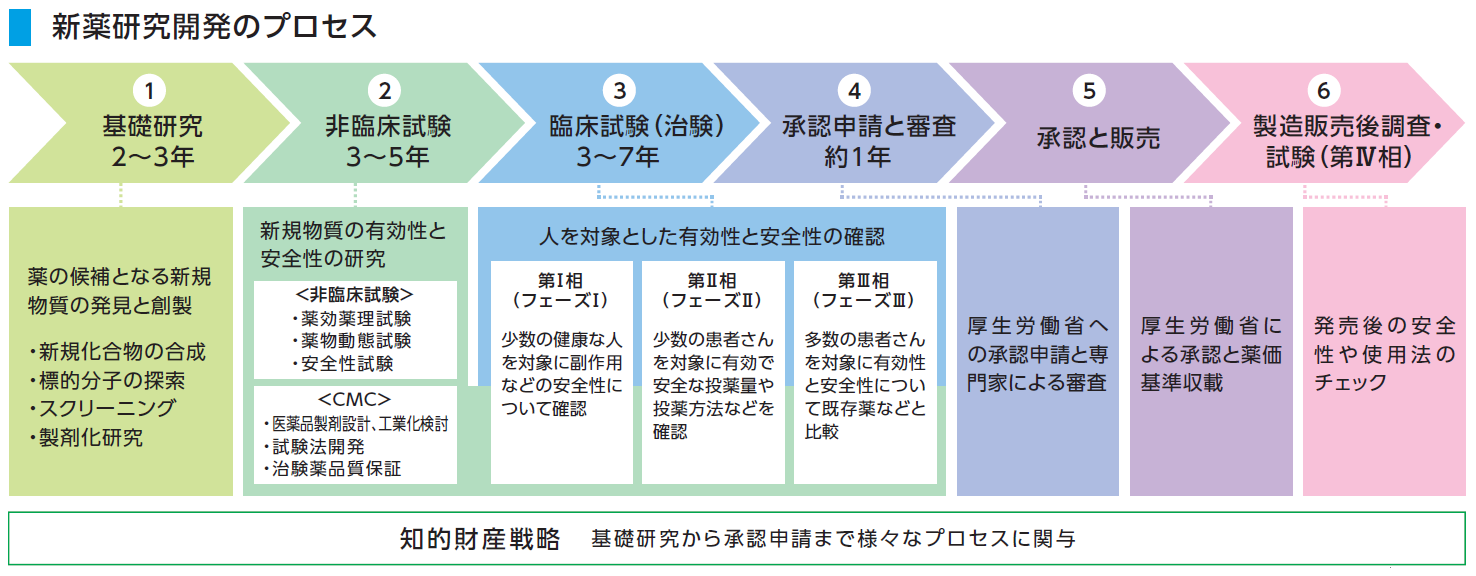
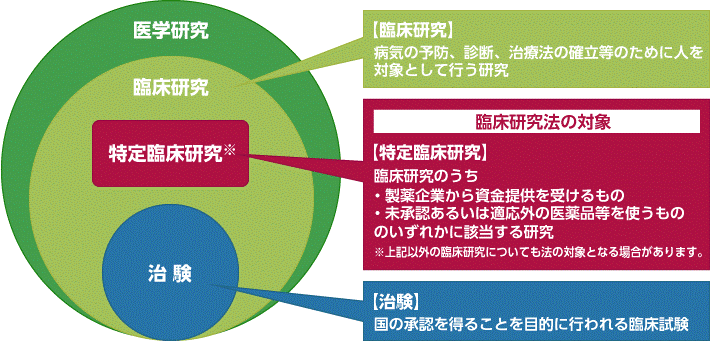
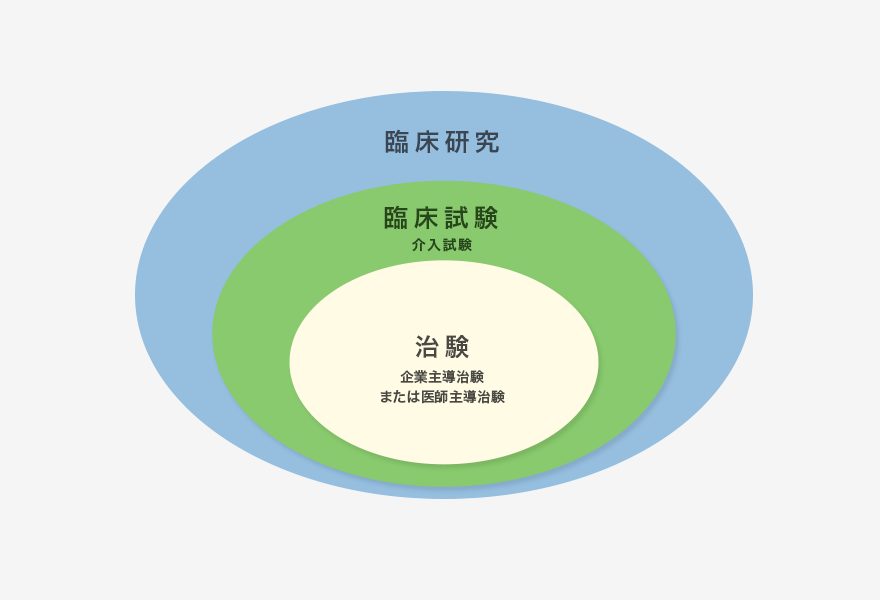
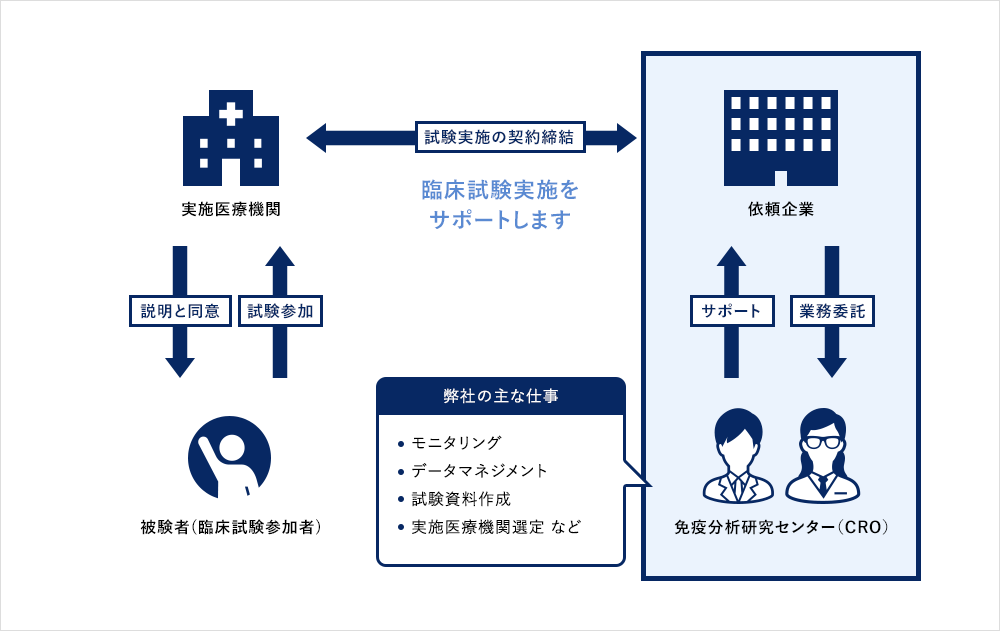
臨床試験
研究のこの段階では、対象グループが治療または曝露を使用し、その後に治療/曝露を使用しない対照グループが続きます。研究に参加する被験者の配分は、ランダム(ランダム化)または非ランダムで行うことができます。これらは 4 つのフェーズで構成されます。
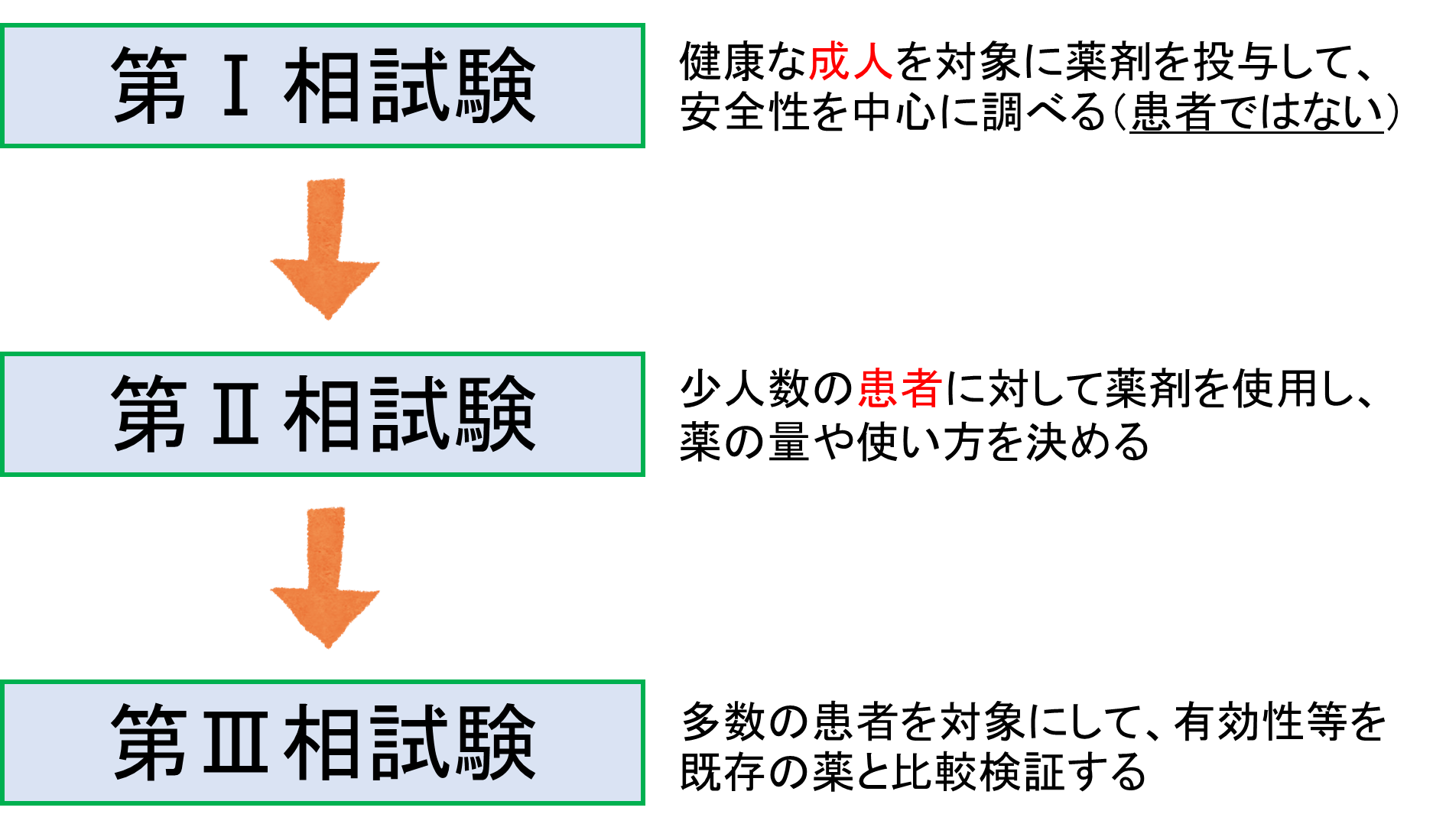
フェーズI
試験中の薬剤は初めて人体に使用される。研究対象の病気に罹患していない10~30人の健康なボランティアが参加する。さまざまな用量が評価され、安全性試験が実施され、薬物やアルコールの使用との相互作用が評価されます。この段階では、人体に毒性があるかどうか、またそれが多くの悪影響を引き起こすかどうかを調べます。
フェーズ II
この段階では、病気を患っている人が参加します。通常、70 ~ 100 人の参加者が招待されます。 免疫系を 刺激して 抗体 を産生する薬の能力が検証されます。数十人の参加者に適用されます。目的は、より多くの安全性データを取得し、新薬の有効性を評価することです。
フェーズIII
この段階では、参加者の数は数千人(100人から1000人)にまで増加します。 最も重要な段階です。この段階では、参加者の一方のグループには治験薬が投与され、もう一方のグループには効果のない物質である「 プラセボ 」が投与されます。これはランダム化された研究です。患者も研究者も、それぞれが何を受け取ったのか知りません。これは薬が安全で効果があるかどうかを確認できる重要な段階です。
薬が有効な場合、研究の評価とその後の登録のために ANVISA (国家健康監視局) に報告書が送信されます。このレポートには、病気、薬が体にどのように作用するか、制限事項、副作用、適用方法、および注意すべき事項についての情報が含まれています。登録が完了すると、Basic Health Unit による製造と流通、または薬局での販売が開始されます。
フェーズ IV
第 III 相で得られた結果の適用可能性は、患者集団の大部分で確認されています。薬物療法の長期的なリスクと利点が監視されます。新薬のプロフィールも、市販されている他の薬と比較されます。その薬の新しい適応症が特定されました。
新しい病気は常に出現しており、制御するには新しい薬が必要です。臨床試験を通じて、研究者はまだほとんど知られていない病気、または既知の病気に対する新しい薬を見つけることができます。私たちは常に保健当局の推奨に従う必要があり、自己判断で薬を服用しないでください。
こちらもお読みください:
参考文献:
臨床試験。以下で入手可能: http://www.butantan.gov.br/pesquisa/ensaios-clinicos 2020 年 10 月 19 日にアクセス。
臨床試験。入手可能場所: https://mooc.campusvirtual.fiocruz.br/rea/medicamentos-da-biodiversidade/ensaios_clnicos.html 2020 年 11 月 22 日にアクセス。
臨床研究の段階は何ですか?入手可能場所: https://www.fcm.unicamp.br/fcm/cpc-centro-de-pesquisa-clinica/pesquisa-clinica/quais-sao-fases-da-pesquisa-clinica 2020 年 10 月 19 日にアクセスされました。
ギャラリー