ラオールの法則は 、1887 年にフランスの化学者フランソワ マリー ラオールによって作成され、数式で混合物の圧力を研究することによって定義されています。
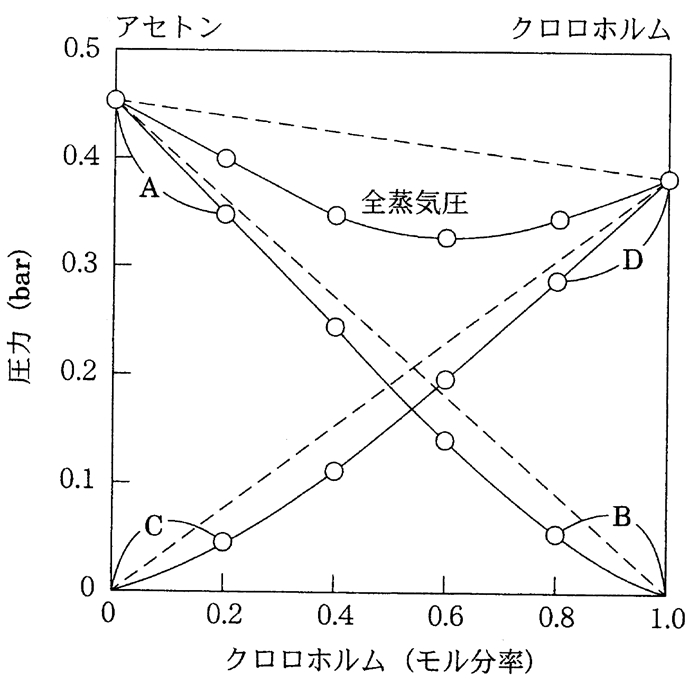
不揮発性物質(溶質)を加えると蒸気(溶媒)の分圧がどのように変化するかという観点からも、溶媒の蒸気の分圧はモル分率に比例すると推測できます。
理想的な解決策は、ラウールの法則に従う解決策です。これらは エンタルピー 数がゼロに最も近いものです。この法律は希釈された溶液にのみ適用されることに注意してください。

この法則は数学的に次のように表現できます。
P= P0
- P: は溶媒の蒸気値です。
- P 0 : 純粋な溶媒の蒸気圧
- X: 溶媒のモル分率。

溶液が平衡に達したときの 蒸発 圧力は、溶液の成分 (溶質 + 溶媒) を加えた次の式に従って測定できます。
P (溶液) = (P 1 )純粋 X 1 + (P 2 )純粋 X 2
- P=圧力
- X=モル分率

溶液の各成分の個別の圧力を測定するには、次を使用します。
P i = (P 1 )pure + X i
- P i = 個別の圧力
- (P 1 )pure= コンポーネントの初期圧力。
- X i = 成分のモル分率。

新しい元素が溶液に追加されると、そのモル分率が減少し、その結果、ガス圧力に対する各成分の寄与が減少します。
蒸発しない物質(蒸発圧力がゼロ)を蒸発する溶媒に加えると、その蒸発圧力は低下し、溶液の最終圧力は純粋な溶媒の初期圧力よりも低くなります。

この法則は、理想溶液のグループの一部である溶液に厳密に当てはまります。つまり、溶液の分子間の結合の種類は、個々の物質の分子間の結合と定性的に同じでなければなりません。
実際の値(溶液の蒸発)が理論値(式の前にある)と異なる場合、溶液中の結合に関するデータを取得できます。実際の蒸発結果が理論値よりも低い場合は、物質を個別に結合した場合よりも溶液の分子間の結合力が強いことを意味し、理論値よりも大きな結果が得られた場合は、溶液中の分子間の結合力が強いことを意味します。溶液の分子は弱くなり、より多くの分子が逃げて蒸気の形になります。
ギャラリー





















