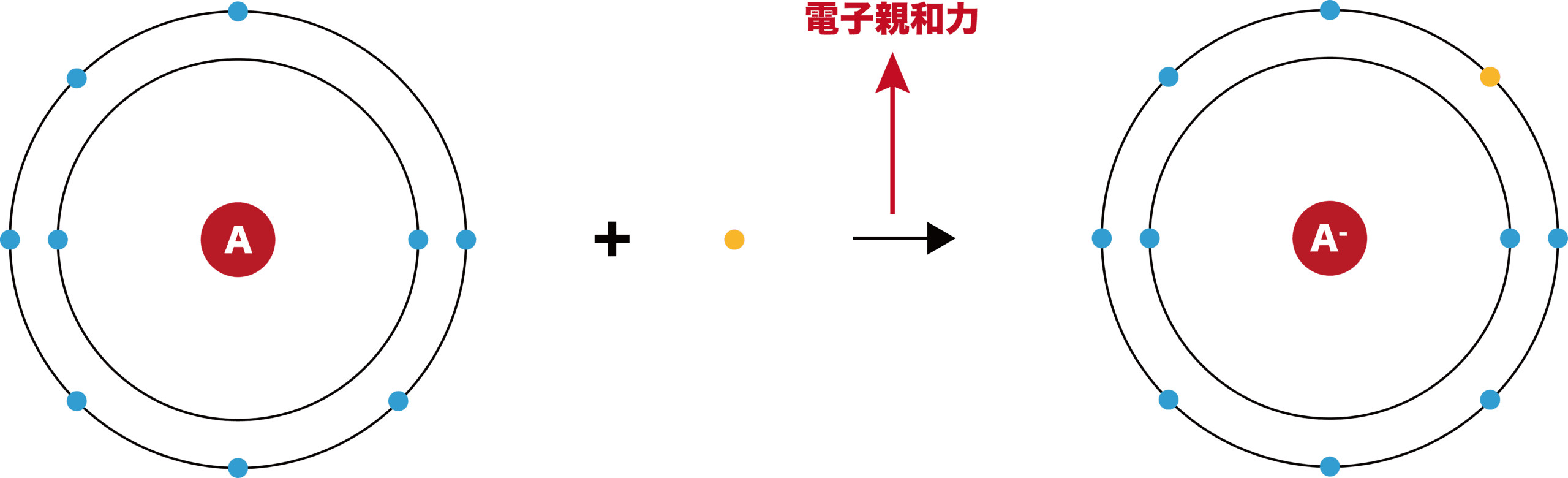
イオン化エネルギー とは対照的に、原子は電子を受け取り、負イオンを形成することもあります。
X(g) + 1 電子 → X- (g)
このプロセスには通常、エネルギーの放出が伴います。このエネルギー量によって、電子が原子にどれだけ強く結合するかを測定します。 「 原子の 電子親和力は 、基本状態にある孤立した気体原子が電子を受け取り、陰イオンを形成するプロセスに関与するエネルギー量 ΔH として定義されます。 」 1 。
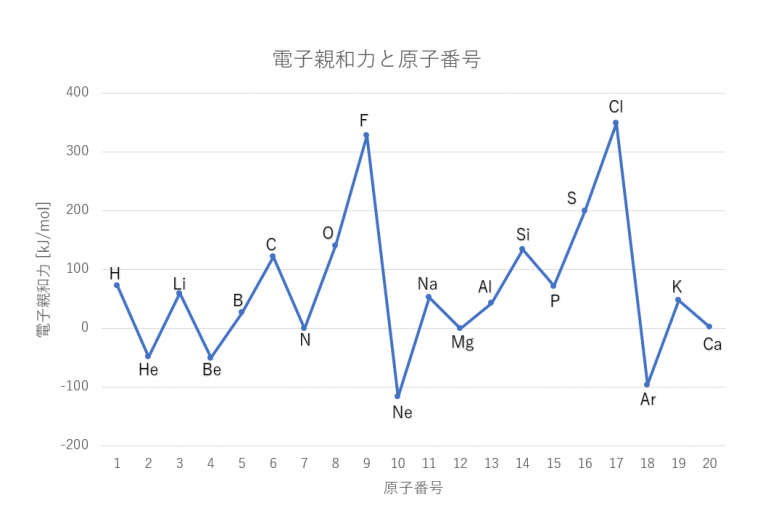
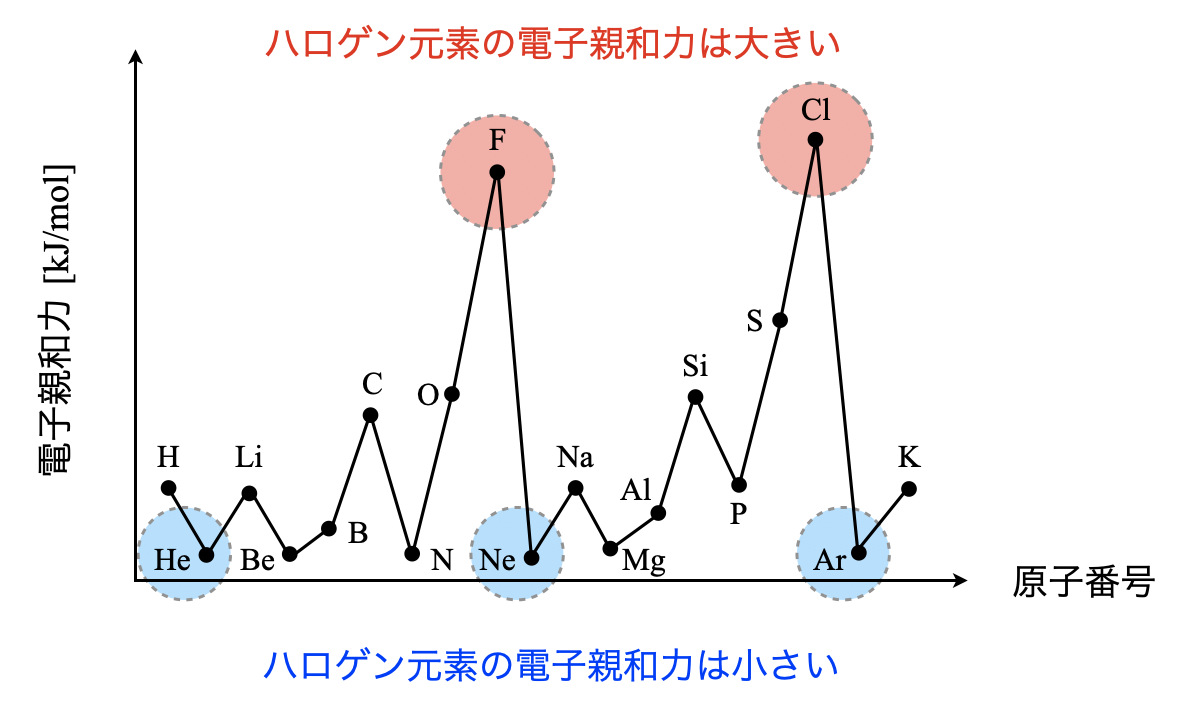
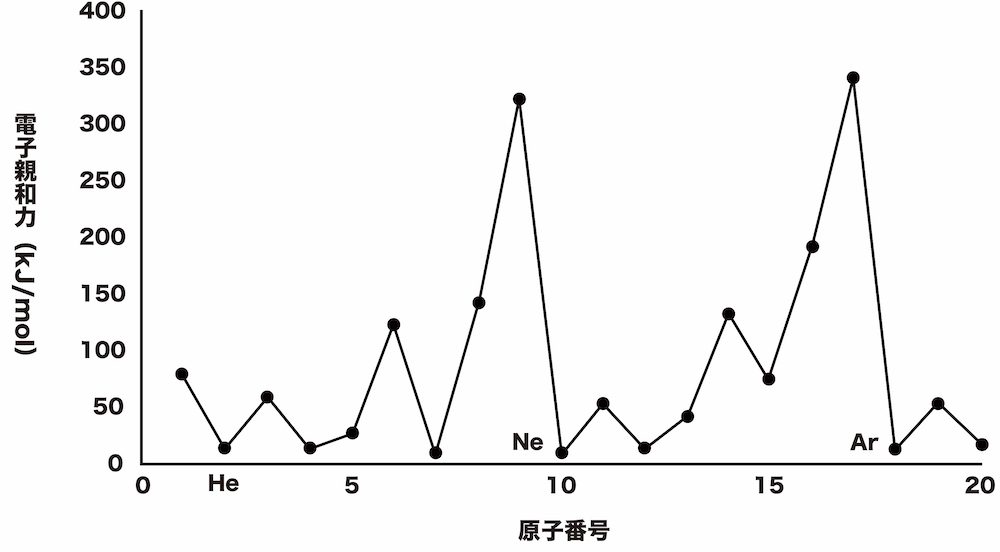
この原子が電子を獲得する傾向がある場合、ポテンシャルにこの傾向が現れ、エネルギーが放出され、ΔH は負になります。そして、それが負であるほど、原子は電子を受け取る傾向が大きくなります。 「 電子親和性は測定が難しく、すべての元素の正確な値は不明です。最初の 3 つの期間の元素の値は、以下の図に原子番号に従ってプロットされています。 (これらの値のすべてが実験的に得られたわけではなく、一部は理論的に計算されました。 )」 1 .
電子親和力 (または 電気親和力 ) の値が正の場合、原子が電子を受け取るときに周囲からエネルギーが吸収されることを意味します。

最初の 3 つの期間の要素の電子的親和性 (1)。
電子親和力という用語は、元素の 1 モルの気体原子と 1 モルの気体モノアニオンの間の内部エネルギーの差として定義されました。正の電子親和力は、アニオンのエネルギーが原子よりも低く、原子からのアニオンの形成が発熱であることを示します 2 。
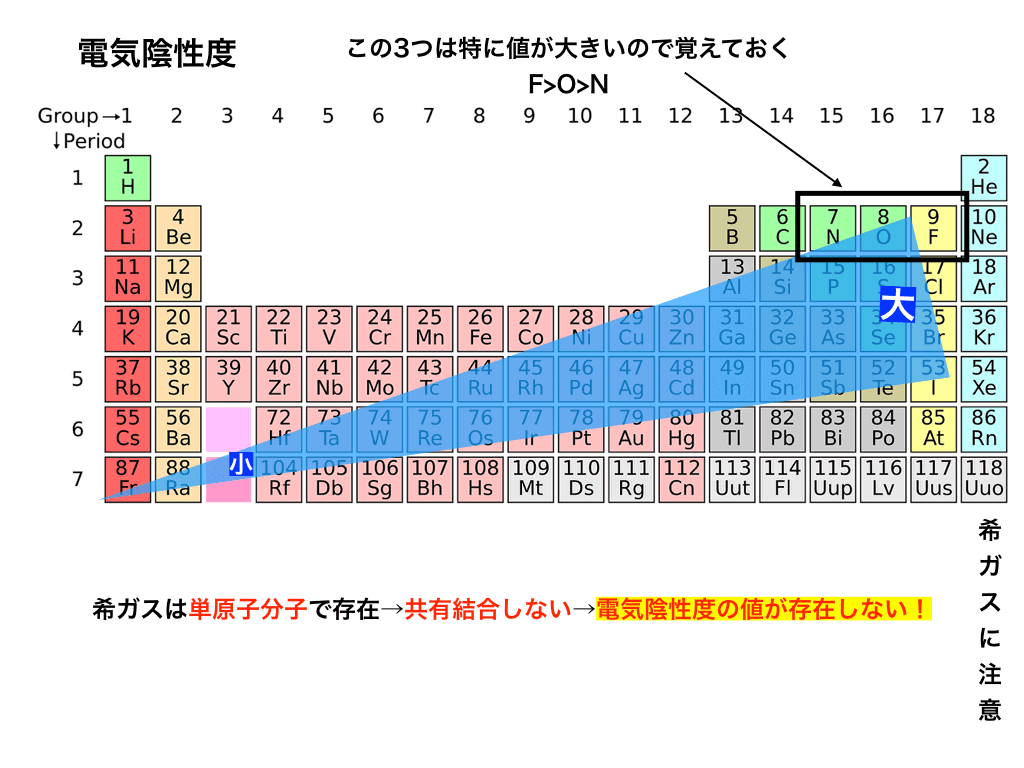
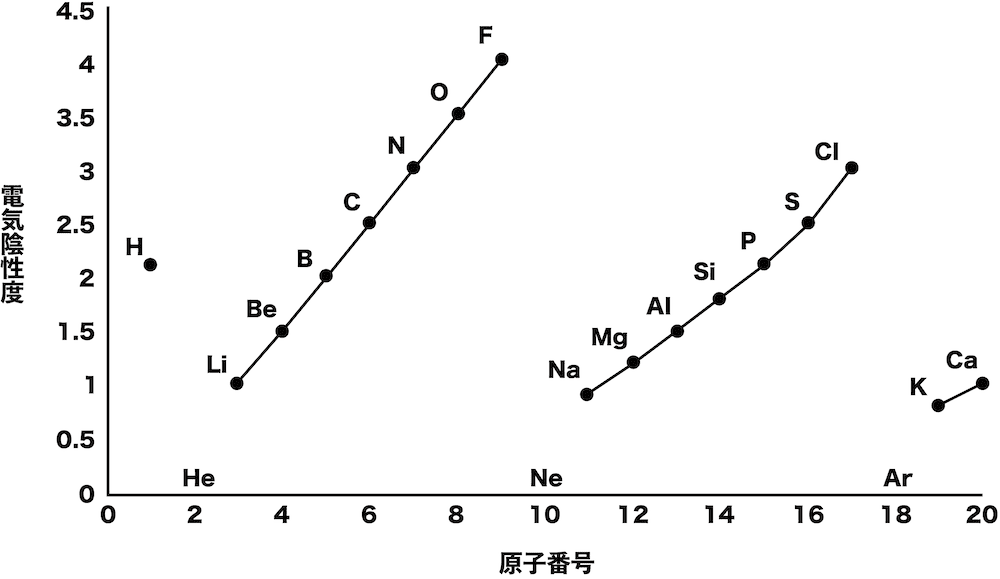
「 電子を取り除くのに必要なエネルギーは、原子が電子を受け取ったときに放出するエネルギーと同じです。 」 3 したがって、2 つの特性は周期表全体で同じ変化を示します。原子のサイズが小さくなると、原子が獲得した電子はより強く原子核に引き寄せられ、電子親和力が増加します。家族では下から上へ。期間中、原子のサイズは左から右に減少するため、電子親和力は左から右に増加する傾向があるという結論につながります。
以下に、 周期表 の族および周期における電子親和力の挙動を概略的に示します。

周期表の族および周期における電子親和力の変化。
電子親和力は、原子が電子を受け取る傾向があるため、非金属に対してのみ実用的です。金属の場合、その原子は 電子 を供与する傾向があり、エネルギー的により安定するため、電気親和力を測定することは非常に困難です。
参考文献:
1. ジョン・B・ラッセル; General Chemistry vol.1、サンパウロ: ブラジルのピアソン教育、マクロンブックス、1994 年。
2. ジョーンズ、クリス・J。
「ブロック要素の化学
」、ブラジル化学会、ブックマン、サンパウロ/SP – 2002。
3. サルデッラ、アントニオ。マテウス、エデガー。
化学コース: 一般化学
、アティカ編、サンパウロ/SP – 1995 年。
ギャラリー