反応の エンタルピー に関する情報だけでは、反応を評価するために必要なすべてのデータが得られないことがよくあります。場合によっては、反応またはプロセスの自発性を定義する必要があり、この場合、 エントロピー と ギブスの自由エネルギー 、それぞれ ∆S と ∆G を使用します。

エントロピーは熱力学的量であり、システム内の分子の無秩序または撹拌の尺度です。語源によれば、エントロピーという用語は、「変化」を意味するギリシャ語の「 entropêe 」に由来しています。
エントロピーに関して 3 つの系を比較すると、1 つは液体状態の水、2 番目は固体状態の水、3 番目は蒸気の状態の水です。3 番目の系のエントロピーは次のようになります。分子の撹拌が大きいため、他のものよりも大きくなります。固体状態の水は、この場合水分子間の間隔が小さく、その結果水分子が撹拌されるため、エントロピーが最も低い系になります。
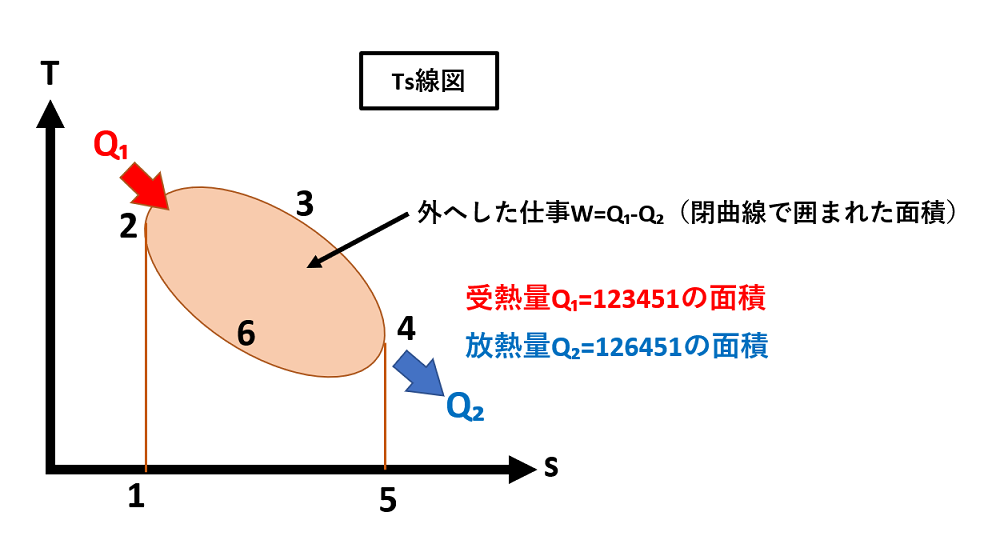
系に撹拌がなく、原子が完全な結晶格子に組織化されている場合、それはゼロまたは実質的にゼロとみなされ、理論的には 絶対ゼロ (0K) の状態になります。
また、系内の温度の上昇が大きいほど、そのエネルギーも大きくなり、この場合はエントロピーが増加することも認識しなければなりません。この一例は、加熱されると、以前は剛性と安定性が高かったその構造がより可動性を持ち、より大きなエントロピーを備えたよりエネルギー的なシステムを作り出す氷です。

システムのエントロピーを計算するには、単位が J/K であることを念頭に置き、次の式を使用します。
ΔS = 最終的な S – 最初の S

計算の結果が次のようになった場合:
- ゼロより大きい値: 自発的な反応の証拠があります。
- 値がゼロの場合: システムはバランスが取れています。
- ゼロ未満の値: 反応は自発的ではない傾向があります。
ただし、 エントロピーとエンタルピーの違いは 何なのか疑問に思われるかもしれません。
エンタルピー (ΔH) は、変換が起こるために物質に蓄えられるエネルギーを指しますが、エントロピーは仕事に変換できないエネルギーを測定します。
ギャラリー