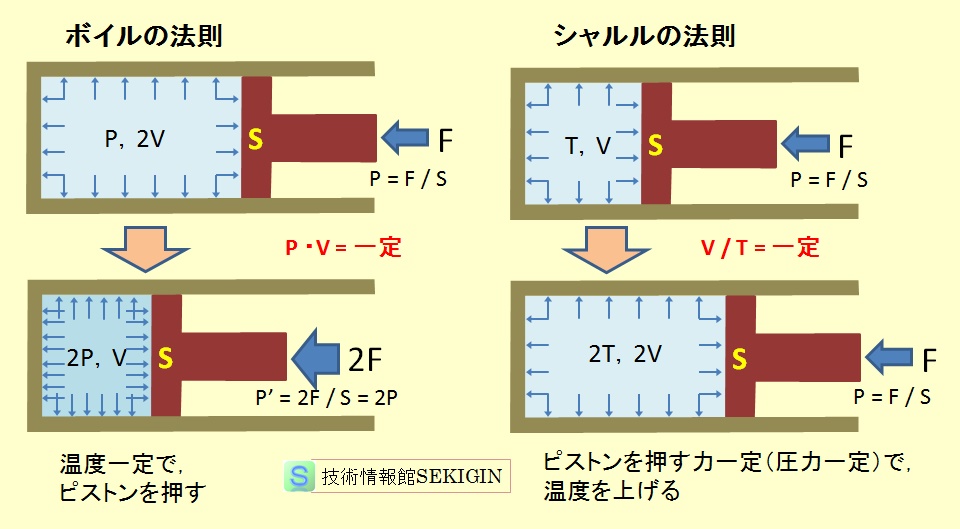
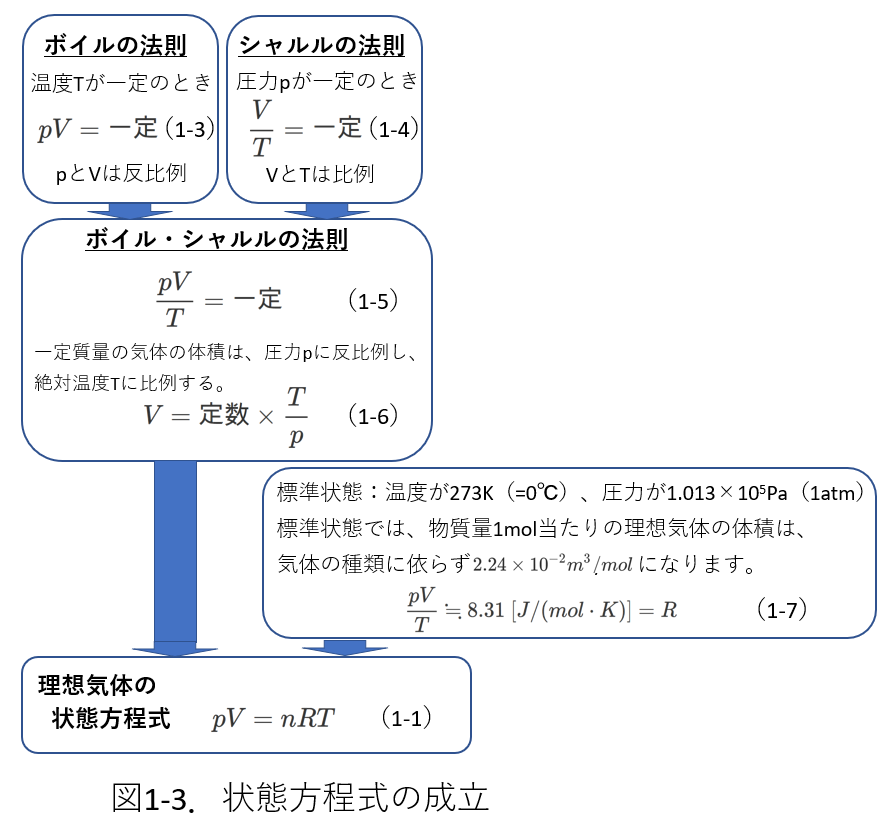
理想気体 または 完全気体 の法則は、気体システムの挙動を記述する法則の組み合わせから生まれました。これらの説明の最初は ボイルの法則 であり、次のように表現できます。

ここで、圧力と体積の積は温度に依存する定数 k 1 であることが確立されます。 2 番目の重要な表現は、以下で説明する ゲイ・リュサックの法則 です。
この法則は、特定の圧力が与えられると、体積は温度に比例するというものです。最後に、次の方程式に従って、圧力と温度は比例するという シャルルの法則 があります。
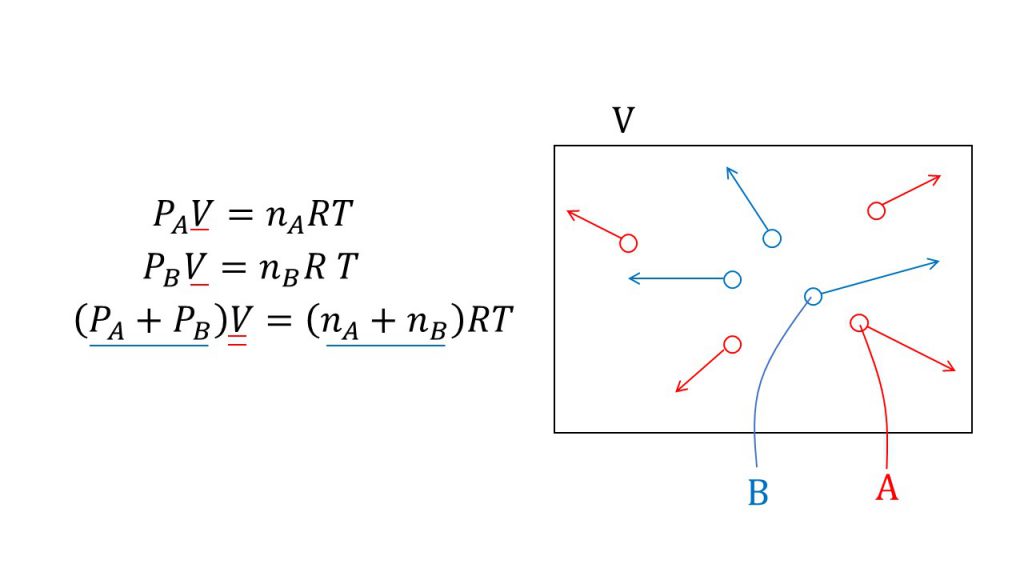
これら 3 つの式を簡単に組み合わせて次のように書くことができます。
ここで、k は定数です。この関係は、圧力と体積の積と温度の比が一定であることを示しています。この定数は、どのような条件下でもすべての 理想気体 で同じですが、系内の物質の量に応じて変化します。 アボガドロの法則 から次のことがわかります。

ここで、 n はシステム内のガスの物質量 (通常はモル単位で測定) です。次に、前の関係を書き換えることができます。
ここで、R は条件に依存しない理想気体の普遍定数です。このようにして、最も一般的な式が得られ、このタイプのガスを扱うのに役立ちます。この式は、 クラペイロン方程式 として知られており、以前に知られていた気体の法則を組み合わせてブノワ ポール エミール クラペイロンによって定式化されました。通常は次のように書かれています。
気体定数 R は、P、V、T の単位に従って使用する必要があります。次の表に、圧力と体積のさまざまな単位に対する定数の値をいくつか示します。
| 圧力(P) | ボリューム(V) | 温度(T) | 定数(R) |
| ATM | L | K | 0.0820atm.LK – 1.mol -1 |
| シャベル | ㎥ | K | 8.314 Pa.m3.K -1 .mol -1 |
| mmHg | L | K | 62.364 mmHg.LK -1 .mol -1 |
気体が物質の量の変化を伴わない何らかの変換を受ける場合、系の最終状態と初期状態に関連する式を定式化できます。

この関係は、ボイルの法則、ゲイ・リュサックの法則、およびシャルルの法則と一致します。
これまでに説明した方程式と法則は理想気体にも適用できることに注意することが重要です。理想気体は、次の条件を満たし、常にランダムに移動する粒子 ( 分子 ) の集合として理想化されます。
- 各粒子が占める体積は、粒子間の空間に比べれば無視できます。
- 粒子間には相互作用する力はありません。
- 粒子は 弾性衝突 を通じてのみ相互作用します。

理想気体モデルは多くの気体にとって非常に便利で正確ですが、このモデルでは十分に記述できないものは実気体と呼ばれます。ただし、実際のガスが理想的な挙動を示すさまざまな条件があり、一般に、これらの条件には低圧と大容量が含まれます。
ギャラリー