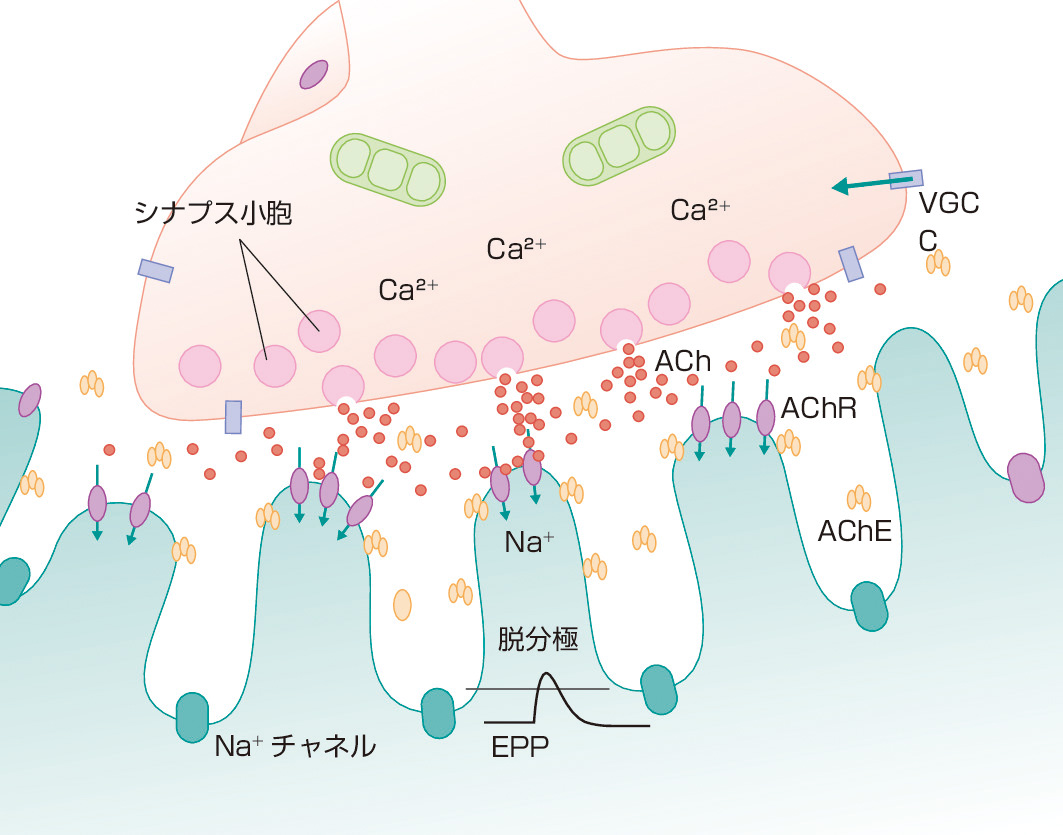
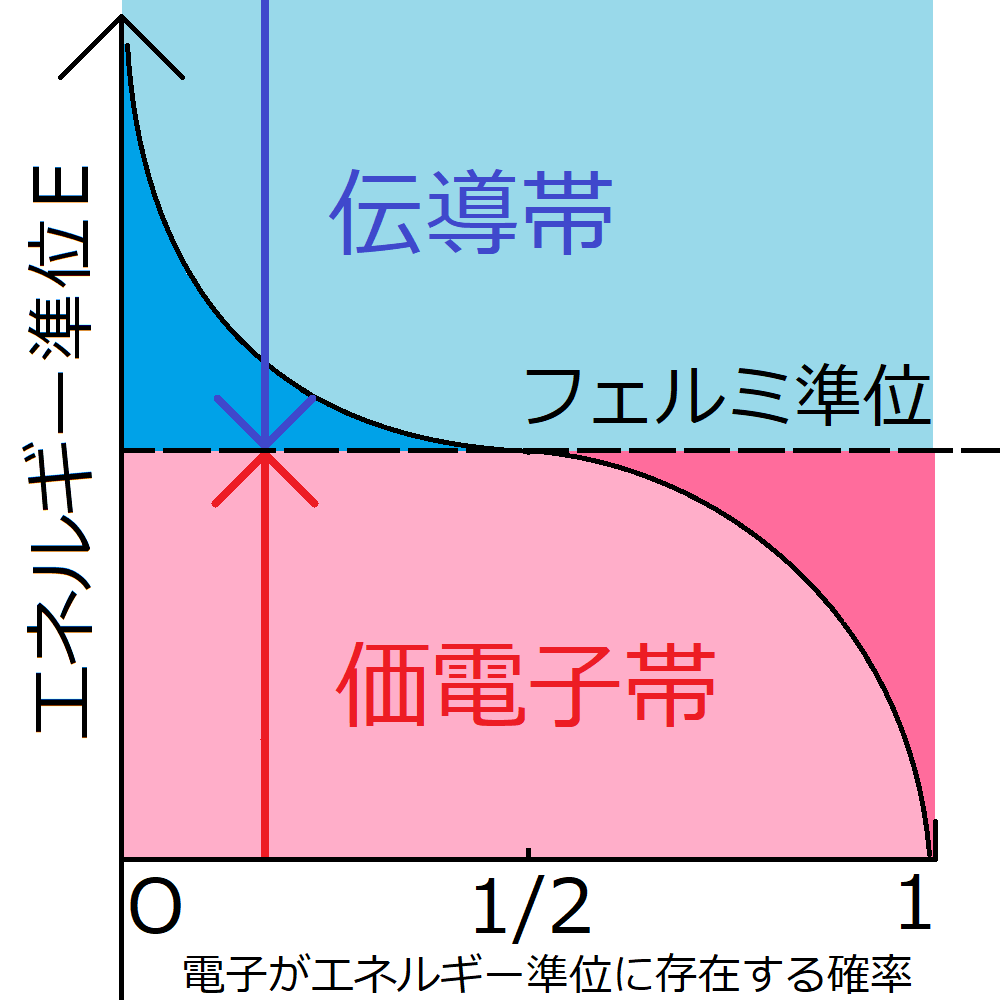
イオン化ポテンシャルは 、電子を 価電子殻 から除去する、つまり 原子 から最後の電子を除去するのに必要なエネルギーです。このエネルギーは、元素の特定の特性に応じて変化します。原子核の電荷と同様に、原子核の正電荷が多ければ多いほど、その電子をより強く引き寄せ、それらを除去するためにより多くのエネルギーが消費されます。あるいは、原子の大きさ、つまり 原子半径 に関しては、小さいほど電子が原子核に引き寄せられるようになり、電子を取り除くためにも多量のエネルギーが必要になります。

電子を除去するには、原子が気体状態でなければなりません。そのとき初めて、電子を除去するために必要な真のエネルギーを測定することが可能になります。また、このエネルギーは、原子核が電子を引き付けるエネルギーと同じです。気体状態でのみ気体原子は互いに隔離されています。
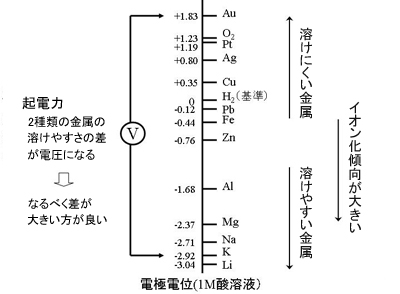
これらの条件下では、これを最初の イオン化エネルギーと呼びます。 価電子殻から最後の電子を除去するのに必要な最小エネルギーが存在しますが、最初に除去される電子は原子核から遠く離れているため、結果的により低いエネルギーになります。電子が層から除去されると、原子核は負電荷よりも正電荷の方が多く、より大きな力で電子を引き付けることができるため、イオン化エネルギーが増加します。

 この種のエネルギーの測定単位としては、電子ボルト (eV) が一般的に使用されます。
この種のエネルギーの測定単位としては、電子ボルト (eV) が一般的に使用されます。

元素の 周期表 から、どの元素が最も高いイオン化エネルギーを持つかを推測できます。原子半径に従って、小さいほどイオン化エネルギーが大きくなり、陽子の数、つまり原子の正の電荷を示す原子番号に従って、イオン化エネルギーは左から右に増加します。下から上へ。
ギャラリー