高校1年生を卒業した生徒でも、 原子 とは何かを知らない、物質が相互作用する基本法則を理解していないという生徒は珍しくありません。これらの質問に対する答えに到達するための選択肢の 1 つは、生徒の科学への興味を呼び起こす広範な必要性を示しています。生徒が議論の内容を理解すれば、これはより容易になります。以下に原子構造のいくつかのトピックを示します。これらは、少なくとも教科書を書いた人の意見では、教科書に載っている言語よりも学生に近い言語で書かれています。

- 今日、原子は、その化学的および物理的特性を保持する物質の最小部分として定義できます。つまり、原子はその一部である材料の同一性を保持しています。物質の最小粒子として定義するだけでは正しくありません。それは、部分粒子からも構成されているからです。

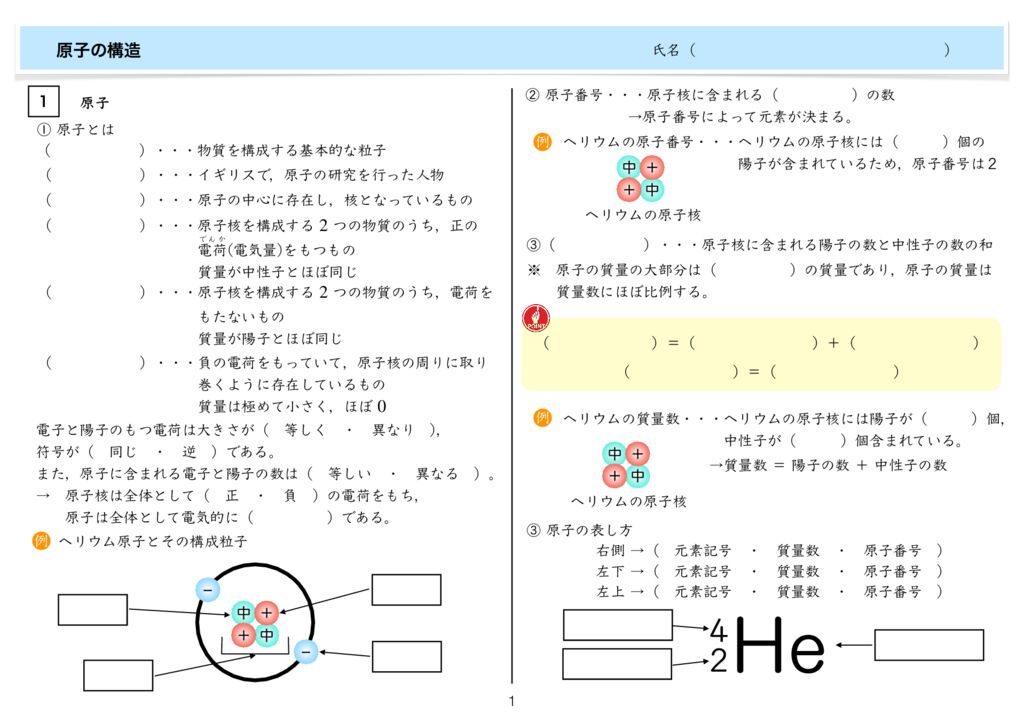
- 原子は、原子核 (原子の中心領域) と 電子圏 (原子の周縁領域) という 2 つの基本的な領域によって形成され、その間には空隙が広がります。つまり、有形のものは何もありません。



- 原子内の陽子 (p) の数は、原子番号 (Z で記号化) と呼ばれます。したがって、Z = p となります。原子内の陽子と中性子の合計は質量数と呼ばれます(Aで記号化)。したがって、A = p + nとなります。
- 原子の電子は、そのエネルギーに応じてレベル、サブレベル、軌道に分配できます。電子エネルギーレベルをチェックするための重要な手段は、 ライナス・ポーリング図 です。したがって、たとえば、1s²、2s²、2p²、3s²…; となります。ここで、大きい数字はレベルを示し、文字はサブレベルを示し、指数の合計は原子内の電子の総数を示します。
参考文献:
フェルトレ、リカルド。化学の基礎、vol.ウーニコ、モデルナ編、サンパウロ/SP – 1990 年。
ギャラリー