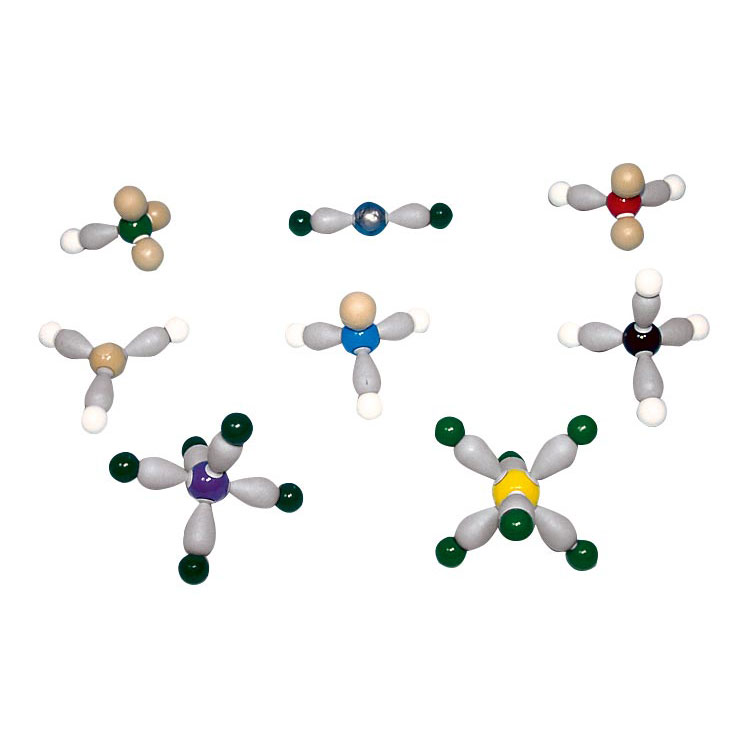
VSEPR 理論 または方法は、分子の幾何学形状、つまり分子が空間内でどのように配置されるかを予測するツールとして使用することを目的として、1957 年に科学者ロン ガレスピーによって定式化されました。英語の頭字語 VSEPR (ベスパーと発音) は 、価電子殻電子対反発 、または 価電子殻内の電子対間の電子反発 を表し、一部の教科書では REPECV とも表記されます。この理論は主にその名前が何を意味するかに焦点を当てています。中心原子の周囲の電子雲の組織内で非共有電子対が維持しなければならない最大距離に関連します。以下に示す手順に従って、この予測を行うのが簡単になります。
空間内の分子の形状を決定する手順:
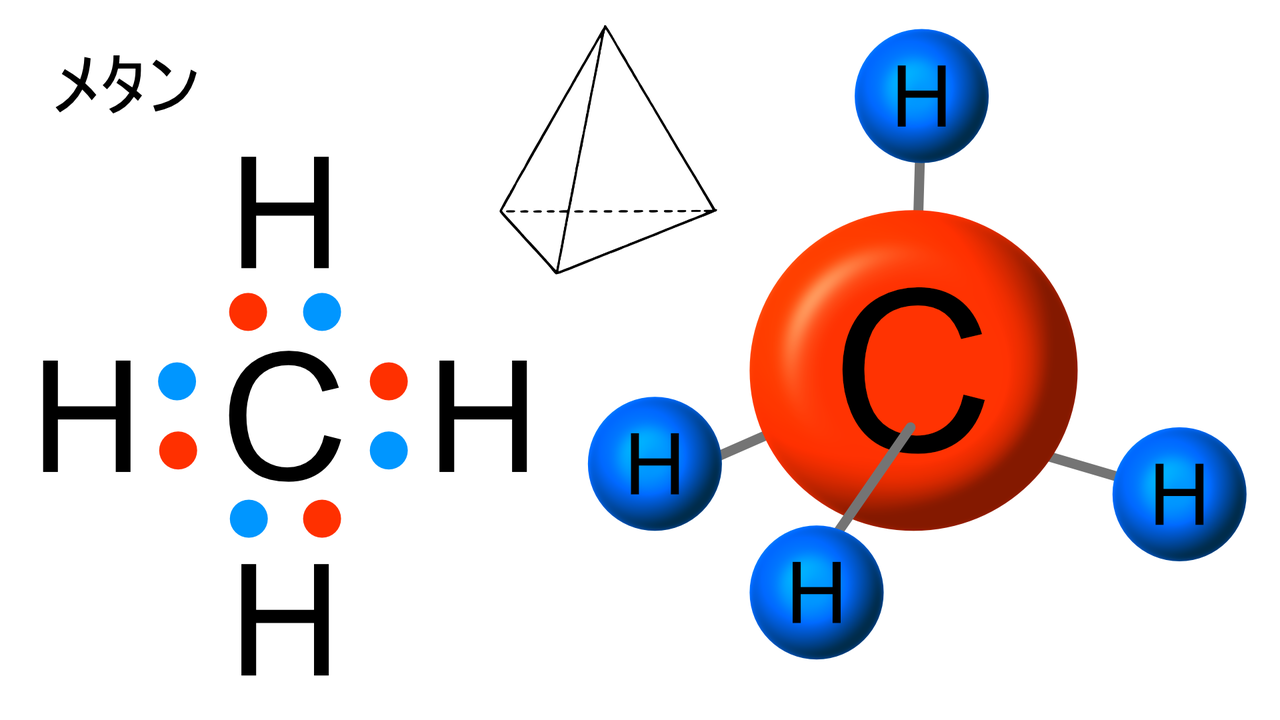
- 分子のルイス構造を観察して描画します。
- 分子内に存在する結合電子対と孤立電子対の数を数え、 立体数 (すべての孤立電子対と結合電子対の合計) を決定します。
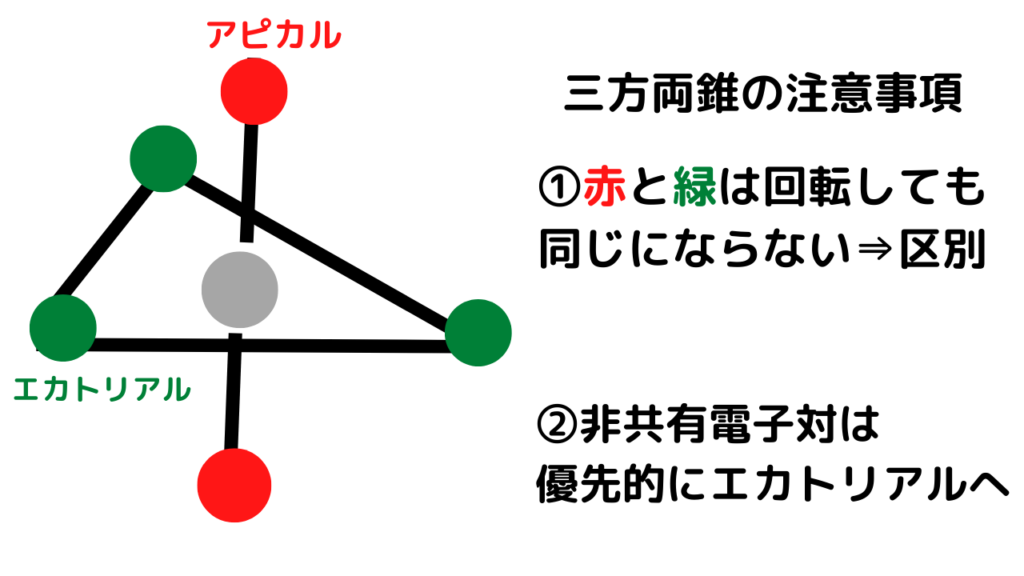
- 孤立電子対間の反発を最小限に抑えるために、幾何学図形の頂点に電子対を配置する配置を作ります。
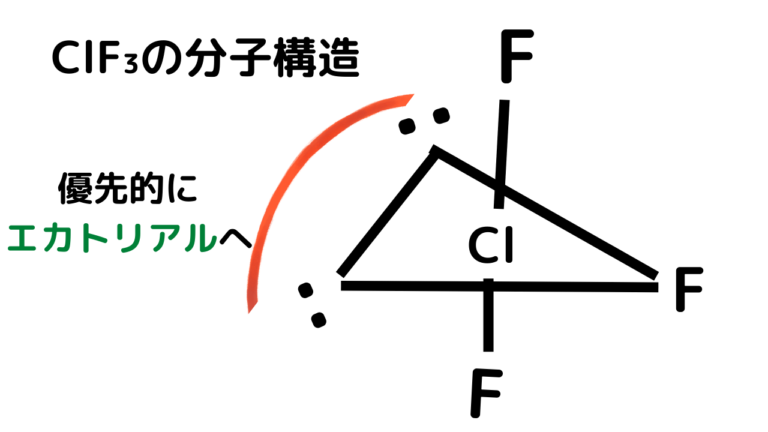
まず、三フッ化塩素分子 ClF3 を例として使用してみましょう。
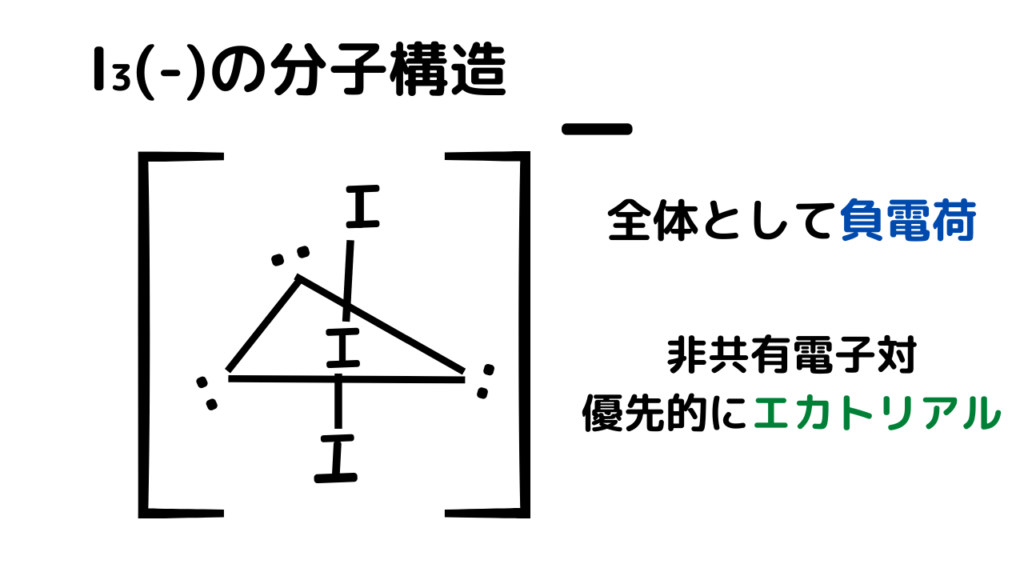
 この構造では、2 つの非共有電子対と 3 つの連結対が観察されるため、2+3=5 を追加します。つまり、5 が立体数です。
この構造では、2 つの非共有電子対と 3 つの連結対が観察されるため、2+3=5 を追加します。つまり、5 が立体数です。
この図を観察すると、立体番号 5 の分子は、次の表に従って三角両錐形と呼ばれる幾何学形状を持ち、非共有電子対が 2 つあるため、 T 字型のサブカテゴリーに分類されると結論付けることができます。この配置により、電子対間に最小限の反発が与えられます。
| 立体番号 | ロンリーペア | ジオメトリ | 幾何学模様 |
|---|---|---|---|
| 2 | 0 | リニア |

|
| 3 | 0 | 平三角 |

|
| 4 | 0 | 四面体 |

|
| 4 | 1 | 三角錐 |

|
| 4 | 2 | 角度のある |

|
| 5 | 0 | 三角両錐 |

|
| 5 | 1 | シーソー |

|
| 5 | 2 | T |

|
| 5 | 3 | リニア |

|
| 6 | 0 | 八面体 |

|
| 6 | 1 | 四角錐 |

|
| 6 | 2 | 平面正方形 |

|
VSEPR 理論は 小さな多原子分子やイオンを予測するのに効率的であることを強調することが重要です。最も重要な観察の 1 つは、孤立電子対が化学結合に影響を与える力を及ぼすため、この理論の主な目的に特に注意を払うことです。理論は、融点と沸点、結合エネルギー、溶解度の点で化学にとって非常に重要な分子形態を決定することです。
参考文献:
ラッセル、JB
一般化学
。
サンパウロ:マクロンブックス、2004 年。
フォーゲル、アーサー イスラエル、1905 年 – 定性分析化学 / アーサー I. フォーゲル; [アントニオ・ヒメノ・ダ訳]第5版。回転数G. Svehla著 – サンパウロ:メストレ・ジュ、1981年。
マハン、BM
化学: 大学のコース
。第4版サンパウロ:エドガルド・ブリュッヒャー、2003年。
デュワード・シュライバー。アトキンス、ピーター。
無機化学
– 第 4 版。ポルトアレグレ、ブックマン、2008年。
リー、JD。それほど簡潔ではない無機化学 – 第 4 版の英語訳。サンパウロ、エドガルド・ブリュッヒャー、1996年。
James Brady、Humiston Gerard E. 一般化学 – 第 2 版
ギャラリー