ル シャトリエの原理は、 外乱を受けたときの平衡状態にあるシステムの応答に関するものです。簡単に言うと、この原理は、平衡状態にあるシステムが障害を受けると、障害を除去してバランスを回復するために自らを調整する傾向がある、というものです。

化学反応における物質のバランスに影響を与える要因はいくつかありますが、その例としては、温度、濃度、圧力などがあります。ル・シャトリエの原理の観点から、これらの各変数の影響を調べてみましょう。


集中
以下に説明する反応が平衡状態にあると仮定します。
反応物または生成物の 1 つをシステムに追加できます。この追加により物質のバランスが崩れ、ル シャトリエの原理によれば、システムはこの乱れを中和するように変化します。
反応物 A を系に追加すると仮定します。物質が平衡に戻るには、A が過剰に消費される必要があるため、反応は生成物の方にシフトします。つまり、再び平衡に達するまで、より多くの C と D が形成され、A と B が消費されます。ただし、何らかの理由で A がシステムから除去されると、システムは C と D を消費して A と B を形成することで、除去された A の量を補おうとするため、反応は反応物の方にシフトします。
一般に、平衡状態での反応では、生成物の濃度の減少または反応物の濃度の増加は順反応に有利であり、生成物の濃度の増加または反応物の濃度の減少は順反応に有利であると言えます。反応物は逆反応を促進します。

プレッシャー
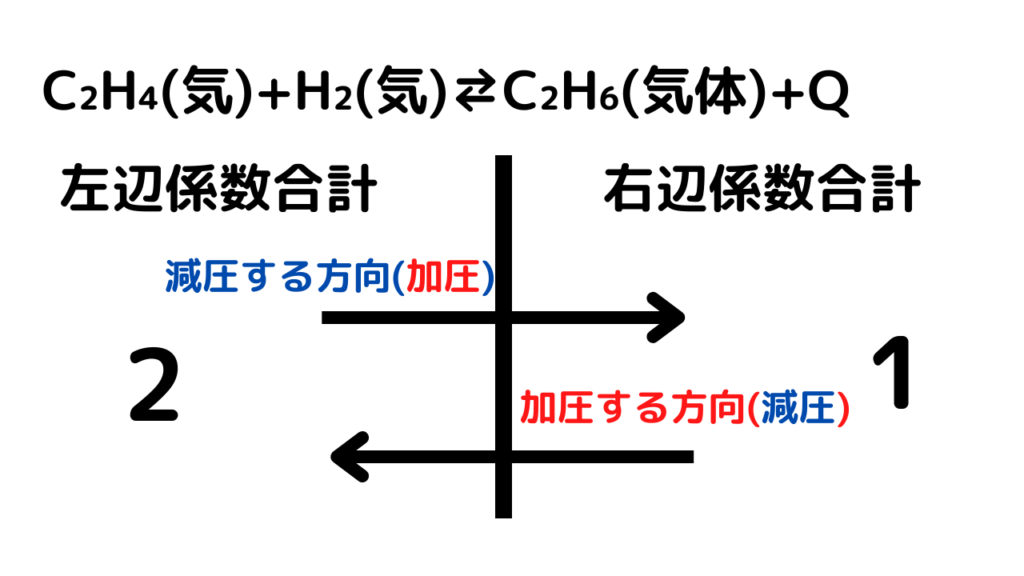
化学反応において反応物または生成物の一部が気体である場合、それらの 分圧 は上記の濃度と同じように動作します。つまり、反応物の分圧の増加は生成物に有利であり、その逆も同様です。ただし、全圧が何らかの外部要因によって変更されると、システムは圧力を調整するために移動してこの外乱を中和する傾向があります。次の反応を考えてみましょう。
反応物と生成物が気体である場合。この反応では、ガスのモル数が減少するため、システムの圧力が減少することに注意してください。したがって、圧力が増加すると、反応が生成物の方に移動し、この意味ではシステム圧力が低下します。反応物の生成により圧力が上昇するため、圧力の低下は反応物に有利になります。

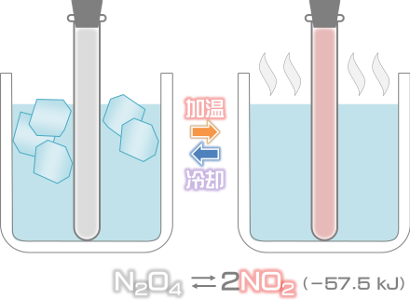
温度
温度が化学反応にどのように影響するかは、その エンタルピー の変化によって決まります。 発熱反応を 考えてみると、放出されるエネルギーは反応の生成物であると考えることができます。次に、次のように書きます。
反応物 → 製品 + エネルギー
吸熱反応 の場合、消費されるエネルギーを反応物として扱います。
反応物 + エネルギー → 製品
ル シャトリエの原理は、反応物の濃度を変更する場合と同じように当てはまります。温度の上昇は、反応に利用できるエネルギーが増加することを意味し、したがって吸熱反応が促進されます。一方、システム温度が低下すると、発熱反応が促進されます。平衡状況では、生成物の形成が発熱性である場合、たとえば、高温が反応物側に有利な場合、反応のどちらの側が発熱性であり、どちらの側が吸熱性であるかを評価する必要があります。
ギャラリー