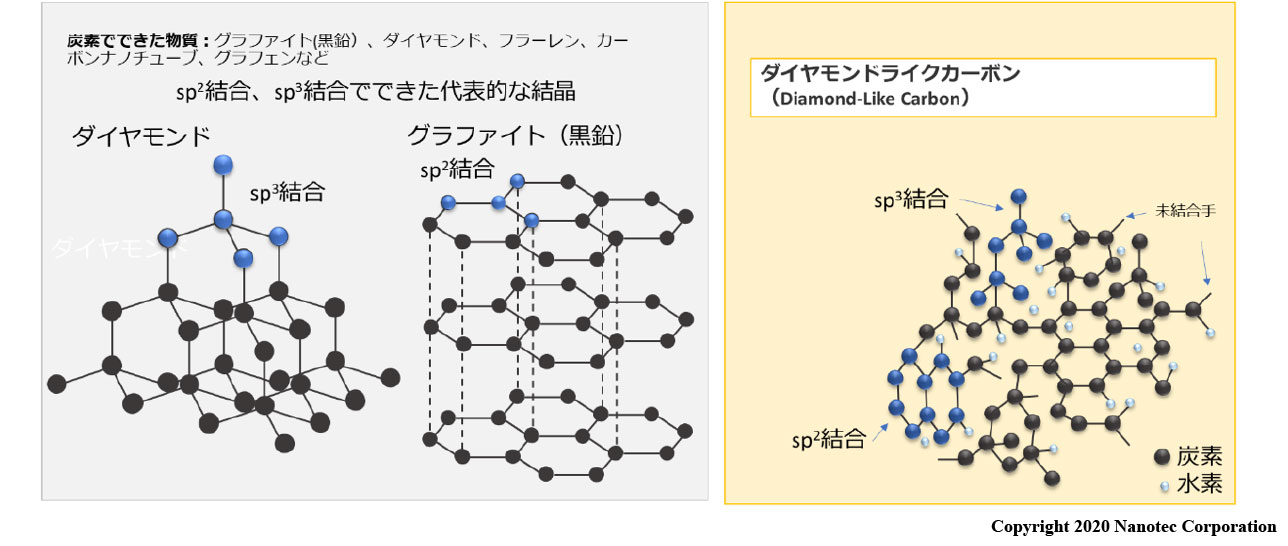
同素性とは 、化学元素が 2 つ以上の異なる 単体物質 を生成する現象です。同素体(生成される単体物質)を形成できる元素は、 周期表 では 炭素 、 酸素 、 硫黄 、 リンの 4 つだけです。炭素はグラファイトとダイヤモンド、酸素は酸素ガスと オゾン 、硫黄は斜方晶系と単斜晶系の構造を形成し、リンは白と赤色の品種を形成することで知られています。
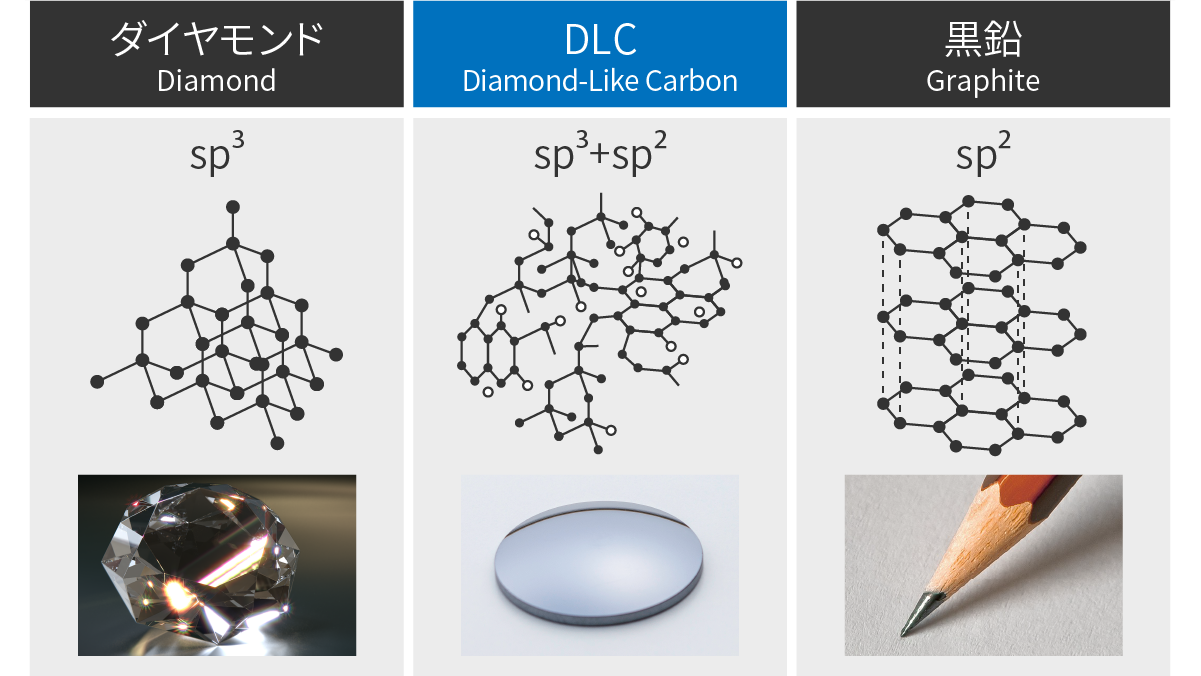
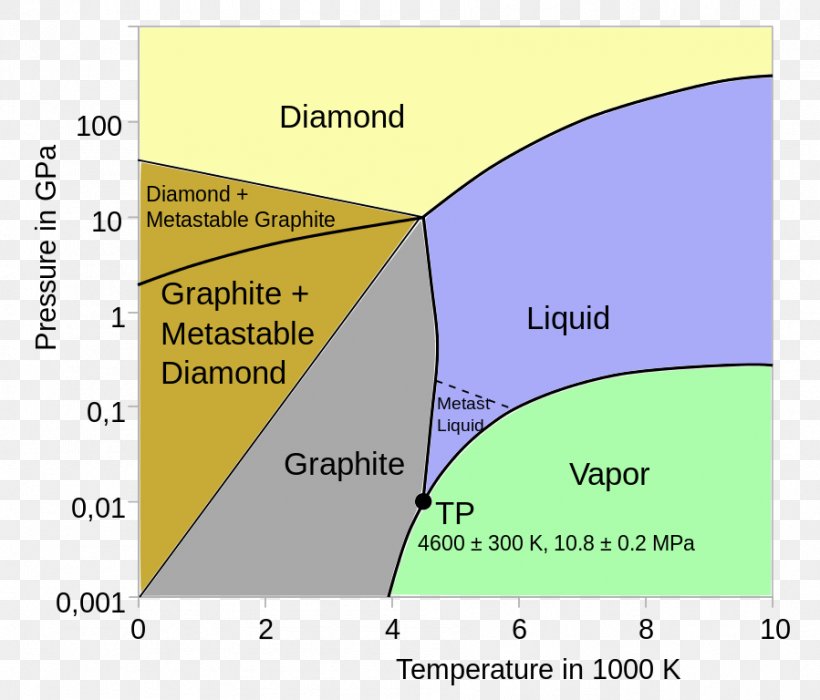
化学元素炭素の場合、言及した同素体品種 (グラファイトとダイヤモンド) は両方とも、明確に定義された結晶構造を持っています。黒鉛の構造は化学層の種類によって構成されており、筆記時にはこれらの層がバラバラになり、一部が紙に重なり合います。ダイヤモンドの場合、複雑な三次元構造により 、自然界で最も硬い物質 となります。

さらに化学元素である炭素を考慮すると、3 番目の同素体品種で あるアモルファス カーボン が重要です (炭素には、フラーレンやカーボン ブラックなど、他の既知の同素体品種もあります)。遊離炭素または反応性炭素とも呼ばれるアモルファス カーボンは、特徴的な結晶構造を持たない、あまり一般的ではない同素体炭素です。それは一般に水素化された形、つまり水素原子によって組み込まれています。アモルファスカーボンは aC と呼ばれ、その水素化された形態は aC:H と呼ばれます。

水素化された形は、その適切な化学構造により、さまざまなフィルムの製造に役立ちます。
「アモルファスカーボン (aC) および水素化アモルファスカーボン (aC:H) フィルムは、 sp 2 と sp 3 の混合物、さらには sp 1 の混成を持ち、高い硬度や弾性率など、ダイヤモンドに似たいくつかの特性を備えています。化学的に不活性。これらは、不定の粒界を有する等方的に無秩序な薄膜として生成されます。一方で、ダイヤモンドよりも製造がはるかに簡単で、さまざまな用途に利点があります。 」
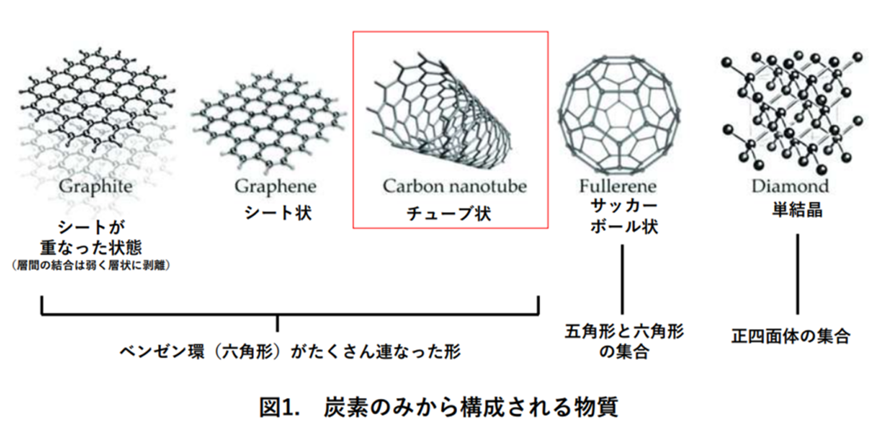
鉱物学では、石炭または煤という用語は、非晶質炭素、およびグラファイトでもダイヤモンドでもない不純な形態の炭素元素を指します。アモルファスカーボンを製造する方法は常に改良されています。アモルファス炭素は sp 2 混成炭素原子で構成され、かなりの濃度の sp 3 混成炭素も含むことが知られています。構造の細孔を制御することで、重要な機能特性を備えた構造を得ることができ、たとえばさまざまな電極に応用できます。

参考文献:
1.
http://www2.dbd.puc-rio.br/pergamum/tesesabertas/9924963_03_cap_02.pdf
フェルトレ、リカルド。化学の基礎、vol.ウーニコ、モデルナ編、サンパウロ/SP – 1990 年。
ギャラリー