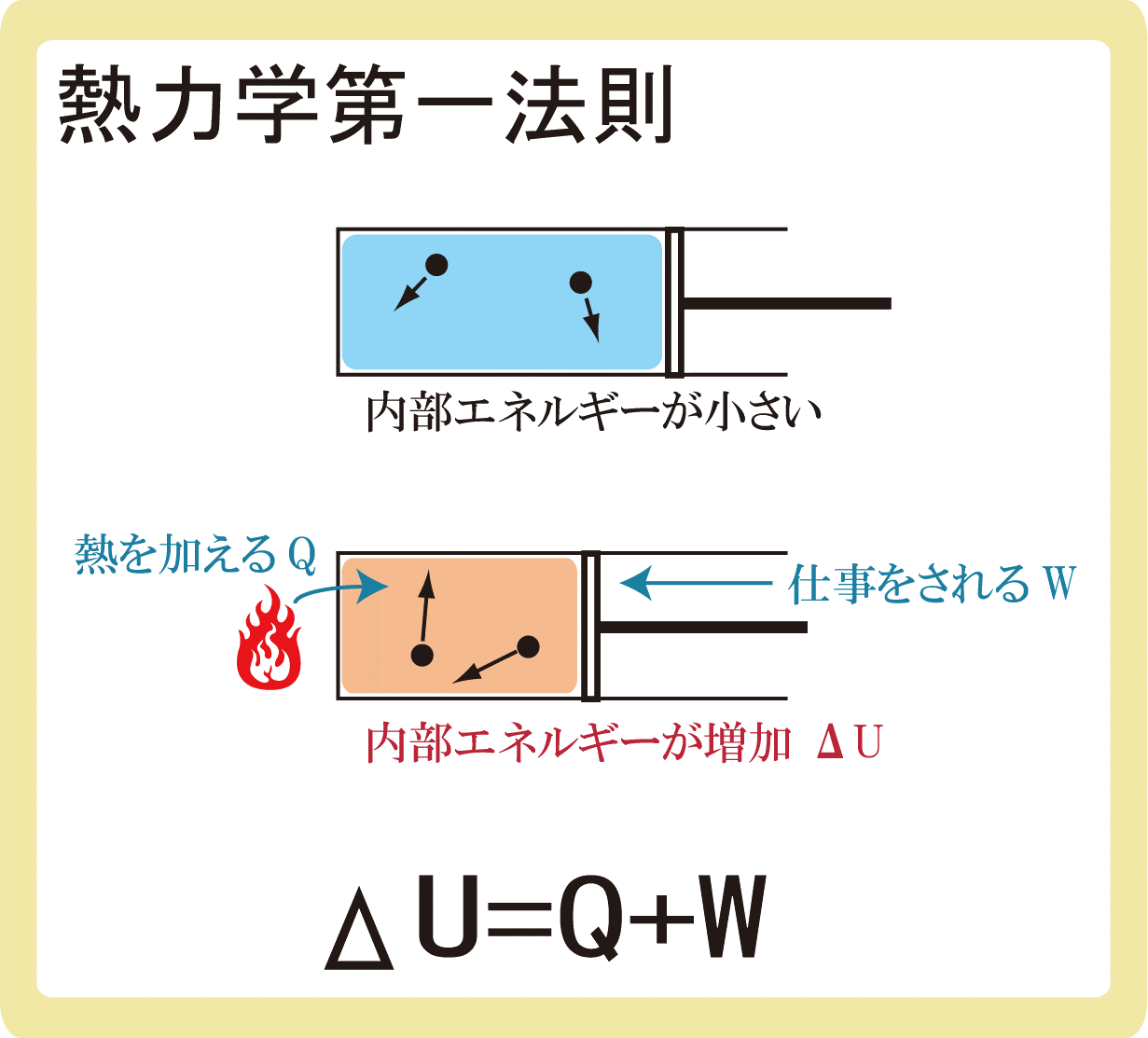
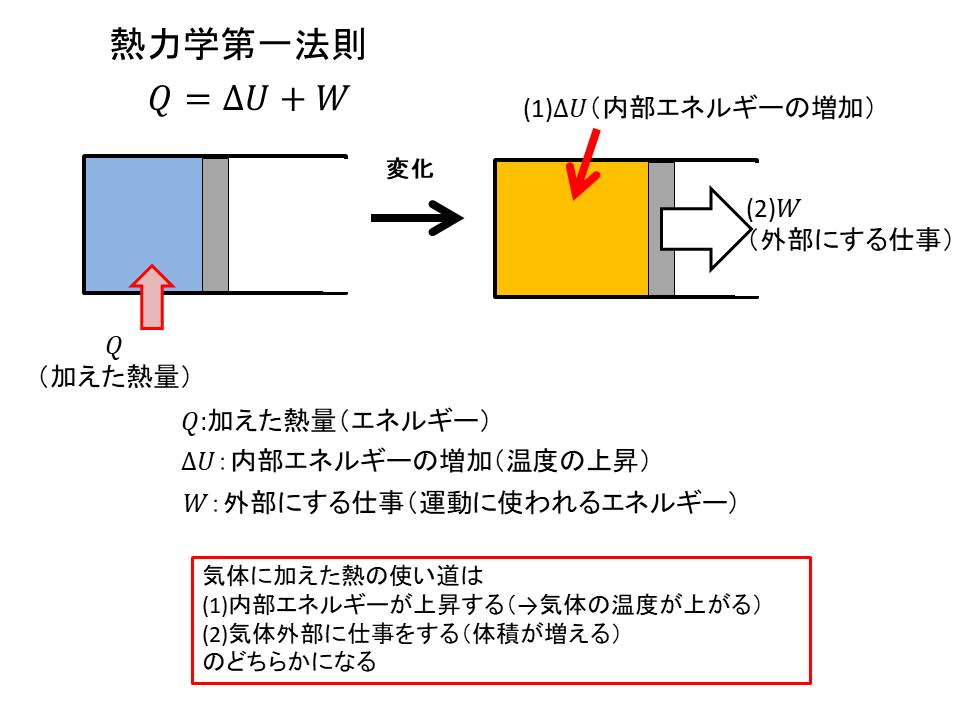
体の内部エネルギー (U) を変化させる可能性のある 2 つの異なるプロセスがあります。彼らです:
- 熱 (Q) : 熱プロセス。
- 仕事 ( τ ) : 機械的プロセス。

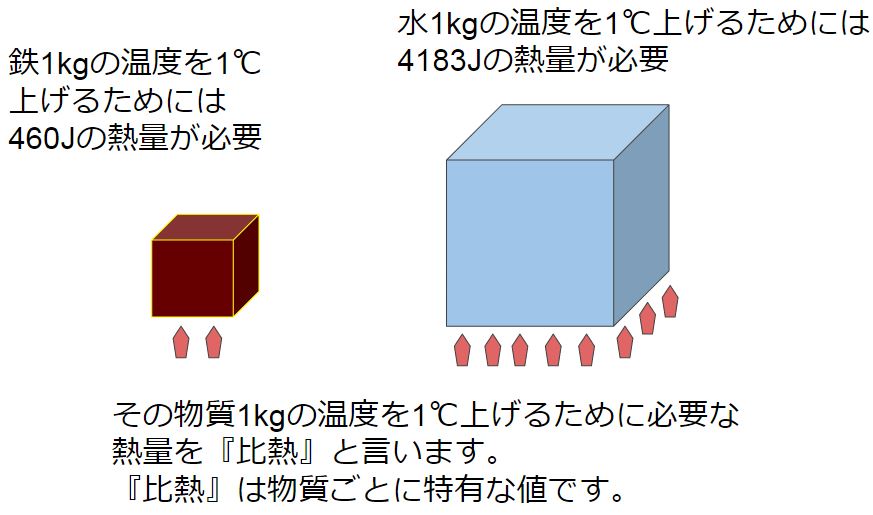
熱は、異なる温度の物体が接触し、温度が平衡に達するまで 熱エネルギー が伝達されることによって発生します。
この仕事には、ピストンに力がかかる場合のように、力を加えて変位を生じさせることが含まれます (ピストンは、力によって生成される 圧力 の変化によって動きます)。
熱力学の第 1 原理は、エネルギー保存則 (エネルギーは決して生成も損失もせず、ある形式から別の形式に変換されるだけである) を通じて、身体の内部エネルギーへの介入のこれら 2 つのプロセスがどのように発生するかを解明しようとします。
Julius Robert von Mayer (1814-1878) と James Prescott Joule (1818-1889) は 、熱力学の第一法則 を定式化した功績を共有しています。どちらも異なる手段を通じて同じ結論に達しました。彼らは次のように結論づけた
- 熱はエネルギー源です。
- このエネルギーは保存されます。
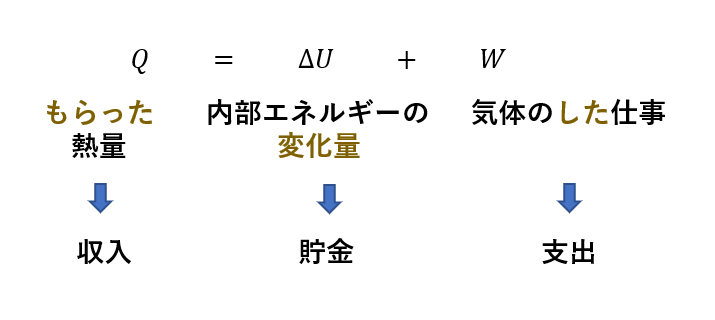
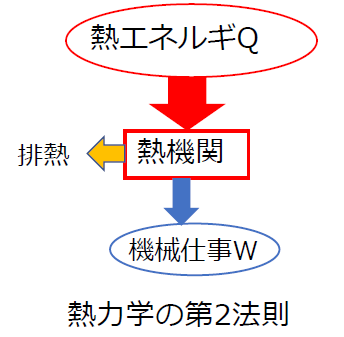
たとえば、システムが熱 (Q) の形で 100 ジュールを受け取ると考えてみましょう。その後、60 ジュールを使用して動作します (τ)。残りの 40 ジュールはシステム内に保持されたままとなり、内部エネルギー (ΔU) の形で蓄えられます。このように、熱の形でのエネルギーは失われず、システム自体の内部エネルギーの仕事と変化に変換されただけであり、保存されたことは明らかです。このような、
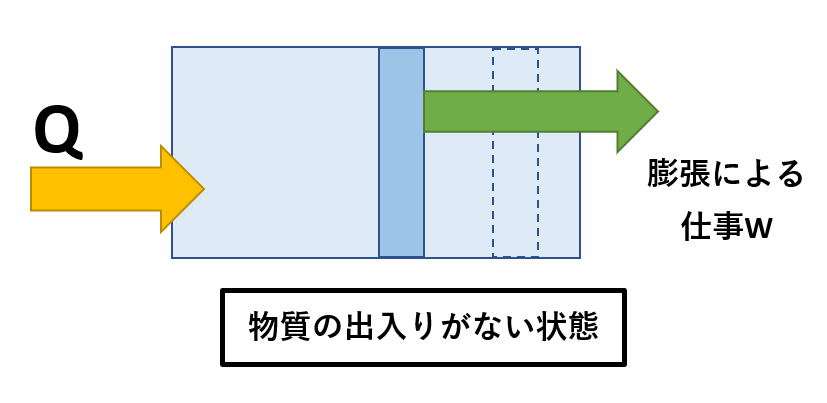
- 熱の形でのエネルギー (Q): システムに入ります 。
- 内部エネルギー変動 (ΔU): システム内に残ります 。
- 仕事の形のエネルギー (τ): システムを終了します 。

図 1. 熱力学の原理によるエネルギー保存。
したがって、熱は、変換される次の 2 つの形式のエネルギーの合計と等価です。
または、入るエネルギー (Q) と出るエネルギー (τ) の差は、系に残る内部エネルギーの変化 (ΔU) に等しくなります。

これらの方程式を通じて、 熱力学第一法則 のステートメントが得られます。
「システムにおいて、その内部エネルギーの変化は、環境と交換される熱と、システムが周囲に及ぼす力によって行われる仕事との差である。」
最初の式を考慮すると、信号について次のように検討できます。
| Q > 0 | システムが受け取る熱エネルギー |
| Q < 0 | システムによって放棄される熱エネルギー |
| τ > 0 | システムによって実行される作業 |
| τ < 0 | システム上で行われた作業 |
| ΔU > 0 | システム温度の上昇(加熱) |
| ΔU < 0 | システム温度の低下(冷却) |
熱力学の第一法則は、特に気体系のために確立されました。ただし、熱、仕事、内部エネルギーの変化を伴うあらゆるシステムに適用できます。
ギャラリー