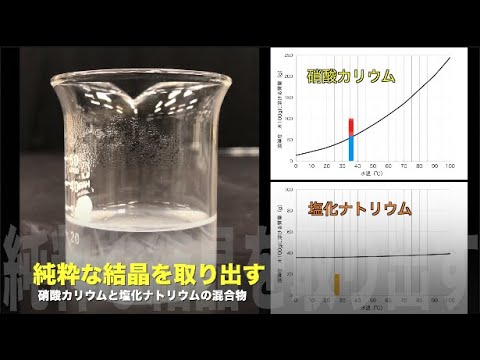
チリ硝石 としても知られる 硝酸ナトリウム は、化学式 NaNO 3 で表される 無機塩 で、周囲条件下では粉末または結晶の形で、無臭、無色または白色です。水、アルコール、液体アンモニアに可溶で、密度は 2.3 g/cm3、融点は 308°C、沸点は 380°C です。

この塩は、 アンモニア から、または 硝酸 と 水酸化ナトリウム の反応から人工的に得ることができます。通常、自然界に存在し、商業的な供給源の中で最も重要です。アルゼンチン、ボリビア、チリ、ペルーの領土には、硝酸ナトリウムの主な自然埋蔵量があります。

硝酸ナトリウムの主な用途としては、次のものが挙げられます。
- 窒素肥料 の製造。
- 爆発物 (主にダイナマイトと黒色 火薬 )、ガラス、花火、接着剤、塗料添加剤、写真試薬の製造。
- 乳製品、缶詰、ソーセージ(ソーセージ、ソーセージ、ハム、モルタデッラ、サラミ、ローストビーフ)およびその他の肉製品の製造において防腐剤として使用され、色固定剤としても機能します。
- 食塩(NaCl)に代わる食糧生産。
- 酸化剤として作用する木炭ウエハースの製造。
- 氷や雪の液状化、
- 下水および汚染水の処理 。
- 清掃用品の製造
- タバコ産業では、タバコの特性を強化します。
- 冶金産業、焼き戻し浴。
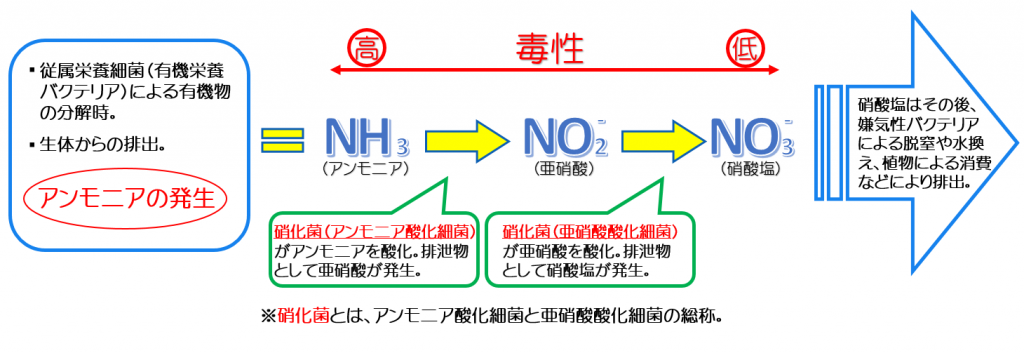
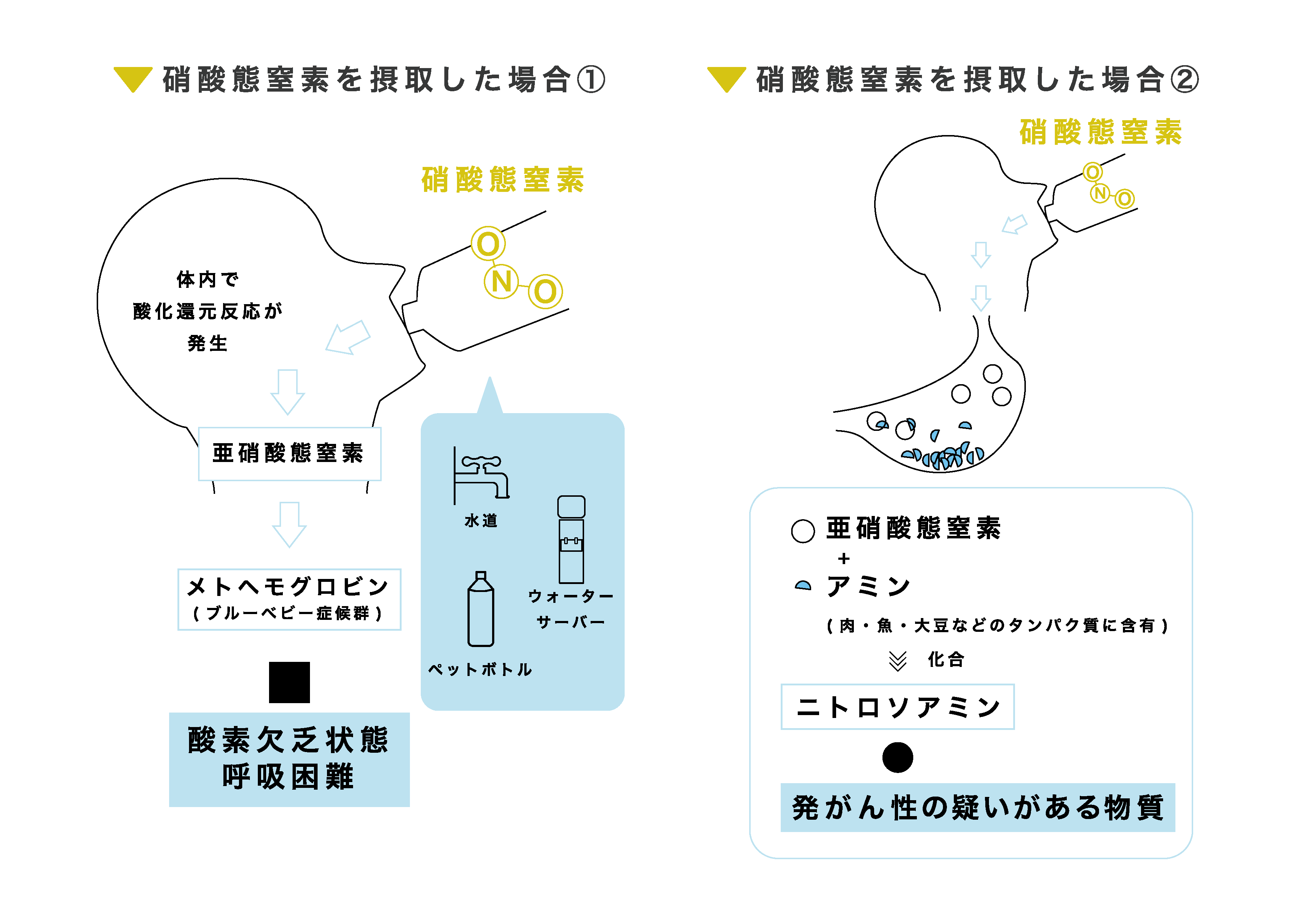
硝酸ナトリウムは、可燃性物質、引火性物質、一部の 有機化合物 、還元剤、シアン化物にさらされると危険を引き起こす可能性があります。これは酸化生成物であり、安定性が低く、酸化します(ただし可燃性ではありません)。人間の健康に悪影響を与える可能性があります。摂取すると、腹痛、チアノーゼ(皮膚が青くなる)、下痢、めまい、けいれん、呼吸困難、頭痛を引き起こす可能性があります。皮膚や目に接触すると刺激、発赤、痛みを引き起こします。その分解生成物は窒素酸化物、亜硝酸ナトリウム (NaNO 2 ) および過酸化ナトリウム (Na 2 O 2 ) であり、これらは高リスク物質です。

参考文献:
http://www.spumol.com.br/index.php?option=com_content&view=article&id=124:nitrato-de-sodio&catid=43:quimicos&Itemid=86
http://pt.wikipedia.org/wiki/Nitrate_de_s%C3%B3dio
http://www.pdamed.com.br/diciomed/pdamed_0001_11985.php
ギャラリー