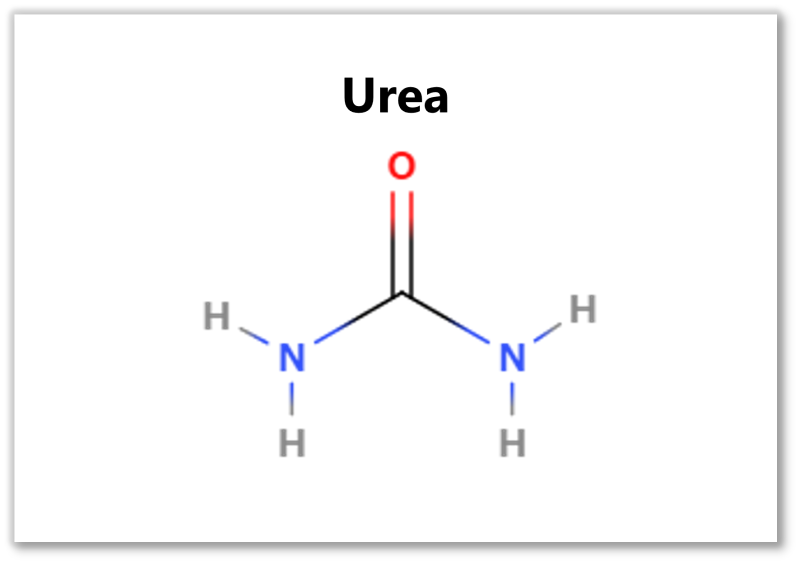
尿素 、CO(NH 2 ) 2 は 白色の結晶として現れるカルバミドであり、水、アルコール、 ベンゼン に可溶です。これは、シアン酸アンモニウムを加熱するか、カルシウムシアナミドを希酸で処理することによって得られます。医学や生化学の研究で使用され、 爆発物 や プラスチック の安定剤としても機能します。高濃度の 窒素 を表すため、農業にとって重要な用途があります。

これは哺乳動物の体内の窒素代謝の最終生成物であり、尿中に排泄されます。植物や キノコ だけでなく、血液にも含まれています。その in vitro 合成は、純粋に無機物質を使用して 1828 年に ヴェーラー によって達成され 、有機製品の唯一の生産者としての 生命力の理論 を覆しました。
尿素は、以下で説明するように、いくつかの実験に非常に適しています。

A) 開始溶液は 3 mol/L の尿素でなければなりません。
B) ガス状分子の放出。

1. N 2 : 漂白剤は、NaClO、NaOH、および Cl 2 を水中に含む溶液です。尿素は以下の方程式に従って漂白剤と反応します。
- 前に調製した尿素溶液 20 mL を三角フラスコに加え、次に漂白剤 (次亜塩素酸ナトリウム) 30 mL を加えます。生成されたガスの可燃性をテストし、観察を記録します。

2. NH 3 : 尿素は、以下の方程式に従って 、水酸化ナトリウム と反応して、強くて不快な臭いを持つアンモニアガスを放出します。
- 三角フラスコに、20 mL の 3M 尿素溶液と 20 mL の 3M 水酸化ナトリウム溶液を加えます。均質化して5分間観察します。観察結果を書き留めます。

3. CO 2 : 以下の方程式に従って、尿素は塩酸と反応して 二酸化炭素 を放出します。
- 三角フラスコに、3M 尿素溶液 20mL と 3M 塩酸溶液 20mL を加えます。均質化して5分間観察します。観察に注意してください。

C) 重合反応。
-
尿素ホルムアルデヒドプラスチックは、ホウ酸の存在下で尿素をギ酸
アルデヒド
に縮合させることによって得られます。
- 尿素3g、ホルムアルデヒド4mL、ホウ酸0.2gを試験管に入れます。シェイク。
- 三角フラスコに水 100mL を入れ、アスベストスクリーンの上に置き、水を ブンゼンバーナー で沸騰するまで加熱します。
- 木製クランプで試験管を保持します。試験管の底を三角フラスコに差し込み、沸騰中に発生する水蒸気を受けるようにします。可塑化するまでこの位置に保ちます。粉末状のプラスチックが生成します。
- 小さな缶に、尿素が溶けるのに十分な量の尿素と少量のホルムアルデヒドを加えます。濃塩酸約1mLを一滴ずつ加えます。溶液は沸騰します(加熱しないでください)。冷えると、生成されたプラスチックが底に残ります。
参考文献:
ルフティ、マンスール。フェラドスとクロマドス:化学知識の社会的生産と私的流用、UNIJUI編、Ijuí/RS – 1992年。
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ギャラリー