有機化合物は
長くて重い原子鎖を形成することが知られており、
水素化
や
ハロゲン化
などの化学反応を実行することもできます。しかし、多くの学生が疑問に思っているのは
、
有機化合物
の酸性またはアルカリ性をどのように判断するか
ということです。
有機化合物は
長くて重い原子鎖を形成することが知られており、
水素化
や
ハロゲン化
などの化学反応を実行することもできます。しかし、多くの学生が疑問に思っているのは
、
有機化合物
の酸性またはアルカリ性をどのように判断するか
ということです。
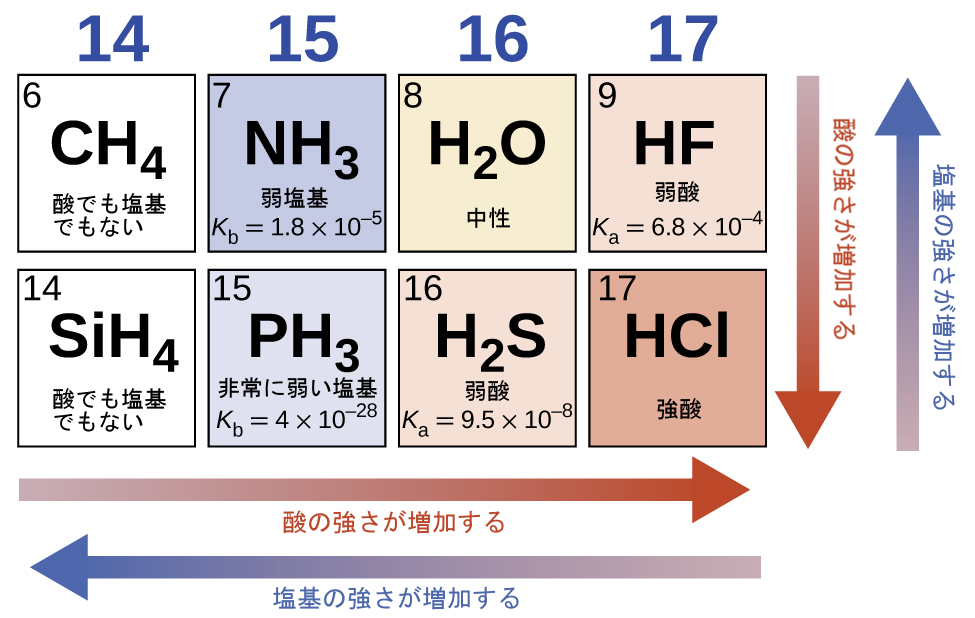
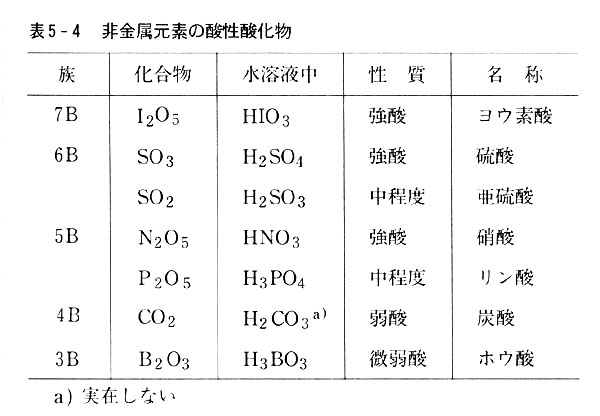
この分析を実行するには、まず分析全体が化合物間の比較に基づいており、酸性またはアルカリ性のレベルが 有機酸や合成酸 と比較して非常に低い傾向があることに留意する必要があります。
次に、 分子 の共役塩基を操作する必要があります。塩基が不安定であればあるほど、分子の酸性度が低くなるということを常に念頭に置いてください。そして、不安定性を判断するために、CREIO ルール: 電荷、共鳴 ( メソメリック効果 )、誘導効果、および軌道を使用します。
負荷
これを行うには、どの原子に電荷があるかを確認します。
- 周期表 の同じ行にある原子
原子が表の同じ行にある場合、どの原子が最も高い電気陰性度を持っているかを確認します。これらの原子は、電気陰性度が低い原子よりも容易に負電荷に対応するためです。ヒント: FONClBrISCPH Metais を使用します。 (左から右へ電気陰性度の降順)。
この場合、酸素は負電荷をよりよく吸収するため、右側の分子の安定性が高まります。
- 周期表の同じ列にある原子
この場合、原子半径が最も大きい原子を探す必要があります。これは、原子半径がより小さい原子よりも負の電荷によく対応するためです。この場合、原子半径が大きい硫黄が勝ちます。

共振
多くの有機化合物は静的であるように見えますが、帯電している (または帯電していない) 有機化合物の多くは、理論的には元の形態よりも安定した瞬間的なハイブリッド形態をとっている可能性があります。
ハイブリッドを設計する方法の 1 つは、電荷を評価し、次の例のように通常は負の電荷が二重結合に引き寄せられることに留意することです。
誘導効果
 このタイプの効果は、化合物内で異なる電気陰性度の原子が結合しているか、非常に近くにある場合に発生します。最も電気陰性度の高い原子は、
電子を
それに近づける傾向があり、双極子を形成します。
このタイプの効果は、化合物内で異なる電気陰性度の原子が結合しているか、非常に近くにある場合に発生します。最も電気陰性度の高い原子は、
電子を
それに近づける傾向があり、双極子を形成します。
この双極子は、場合によっては過剰な電荷を「緩和」し、電荷をよりよく吸収するため、分子に安定化効果をもたらすことができます。
この場合、右側の塩素化基の方が安定です。
ただし、場合によっては、塩素ラジカルを含む鎖の代わりに、メチルラジカルを含む鎖を持つことができます。アルキル基が電子供与体であることを念頭に置くと、これは誘導効果に大きな影響を与えます。
したがって、右側の分子はより不安定です。
軌道
軌道は、原子核の周囲の領域で電子が見つかる可能性のある領域と考えることができます。これらの領域は、電子のエネルギー レベル、つまり電子が位置する殻に応じて変化します。
この基準でどの塩基が最も安定であるかを知るために、混成軌道 (結合) 間の優先順位を定義します。
sp > sp² > sp³
軌道の混成状態を決定するには、実際的な規則を使用できます。三重結合を持つ炭素は sp、二重結合を持つ炭素は sp²、単一の炭素は sp³ です。
(Sp 軌道形状)
研究開発部門副部長のルーカス・サンタンナ・ペレイラ氏による。 Biotec Júnior – キャンパス アシスの Unesp にあるジュニア バイオテクノロジー エンジニアリング会社。
参考文献:
クライン、デヴィッド。第二言語としての有機化学 I – 第 2 版–ジョンズ・ホプキンス大学。出版社 John Wiley & Sons, Inc.2008
アトキンス、ピーター。ロレッタ、ジョーンズ。化学の原理:現代の生活と環境への疑問。リカルド・ビッカ・デ・アレンカストロ訳。 – 第 3 版 – ポルト アレグレ: ブックマン、2006 年。968 ページ。
ギャラリー