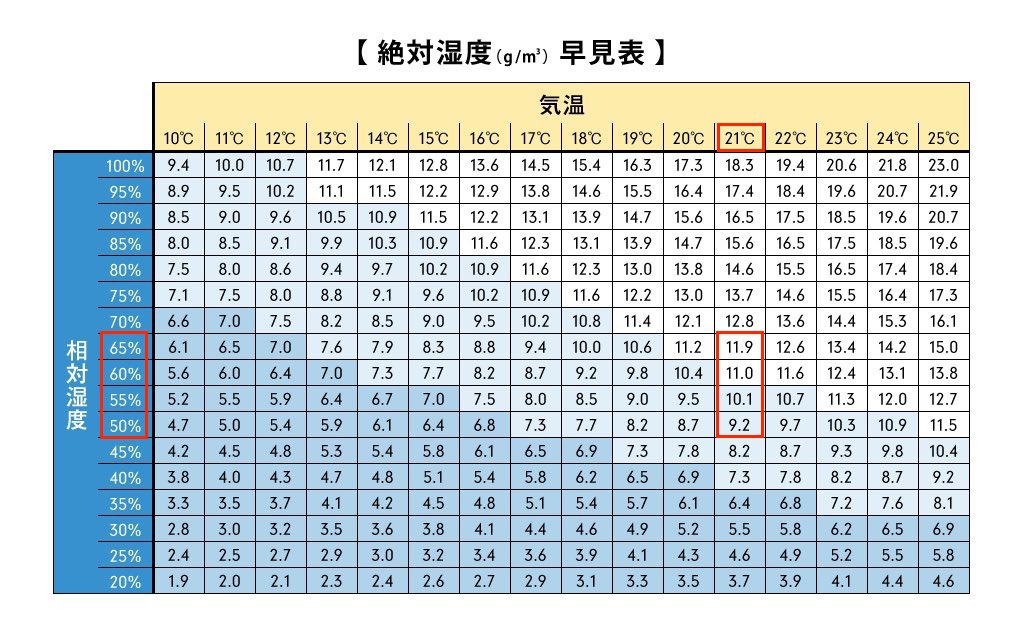
自然界に存在する 純粋 な物質はほとんどなく、そのほとんどは 混合物 として知られる複数の物質から構成されています。 2 つ以上の物質から構成され、均一な外観を持つ混合物を 溶液 と呼びます。 地球を取り囲む大気は、O2 や N2 などのガスによって形成される気体溶液の一例であり、 海水 はさまざまな塩が溶解した溶液であり、金属合金 (鋼など) は固溶体です。

溶液が形成されるには、2 つの成分が必要です。 溶媒 (溶解するもの) と 溶質 ( 溶解するもの) です。溶媒は常に溶質よりも多くの割合で存在し、溶媒が溶解できる一定量の溶質も存在します。これは、 溶解係数 と呼ばれる量です。

例として、水 ( 万能溶媒 と考えられています) と NaCl (食塩) の溶液を考えてみましょう。 20℃で100 gの水に溶解できるNaClの最大量は36 gです。この条件下の溶液は 飽和溶液 と呼ばれます。したがって、この塩の溶解係数は 、20℃で 36 g NaCl/100 g 水 です。ただし、系には常に最大量の溶質があるとは限らないため、溶解係数よりも低い溶質量を含む溶液は 不飽和溶液 と呼ばれます。
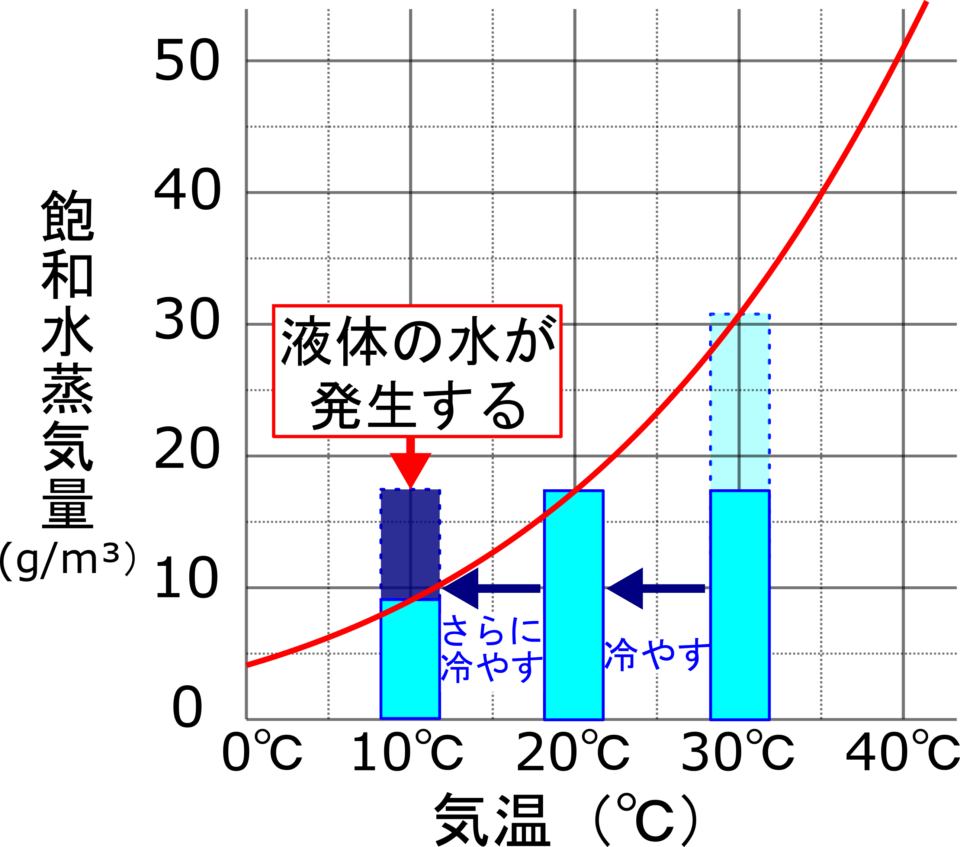
しかし、水100mlとNaCl50gからなる系を加熱撹拌すると塩を完全に溶解することが可能です。この系を絶対静止状態で初期温度 (20℃) まで冷却すると、それぞれの飽和溶液 (36 g) よりも多量の溶質 (50 g) を含む溶液が形成されます。この溶液は 過飽和 として知られており、非常に不安定です。これを振ったり、溶質の小さな結晶を加えたりすると、14 g の塩が沈殿します。これはまさに溶解係数に対して過剰量の溶質であり、したがって溶解できません。この沈殿は 底体 とも呼ばれます。

したがって、溶媒に溶解できる溶質の量は温度に比例することが理解できます。この理由は 、溶解度曲線 と呼ばれるグラフで最もよく表現できます。ご注意ください:
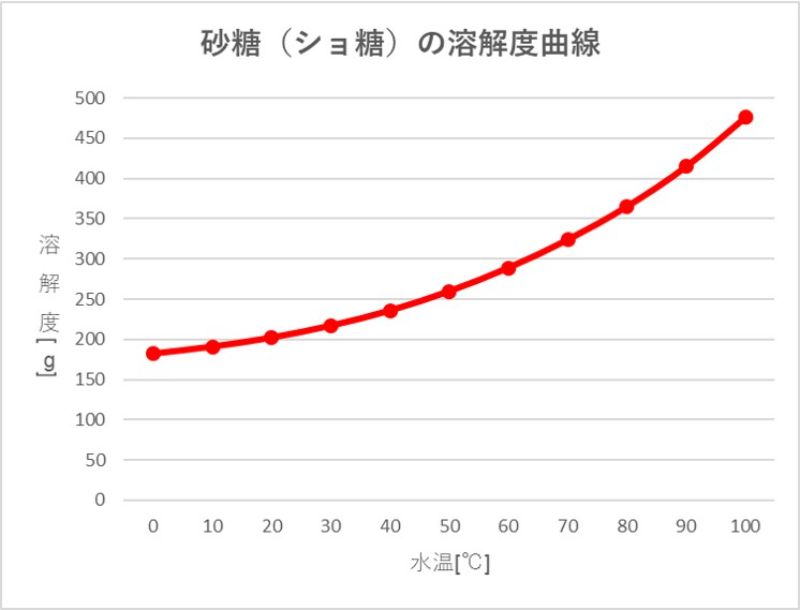
上のグラフには、100 g の水中の硝酸カリウム (KNO3) の溶解度曲線があります。温度が上昇すると、この化合物の水への溶解度が増加し、過飽和溶液が形成されることに注意してください。
参考文献
ウォルター・J・ムーア訳:アイヴォ・ジョーダン。物理化学。 Edgard Blucher: サンパウロ、1976 年。第 4 版。
ピラ、ルイス。物理化学。技術および科学書籍編集局 SA: リオデジャネイロ: 1979。初版。
ギャラリー