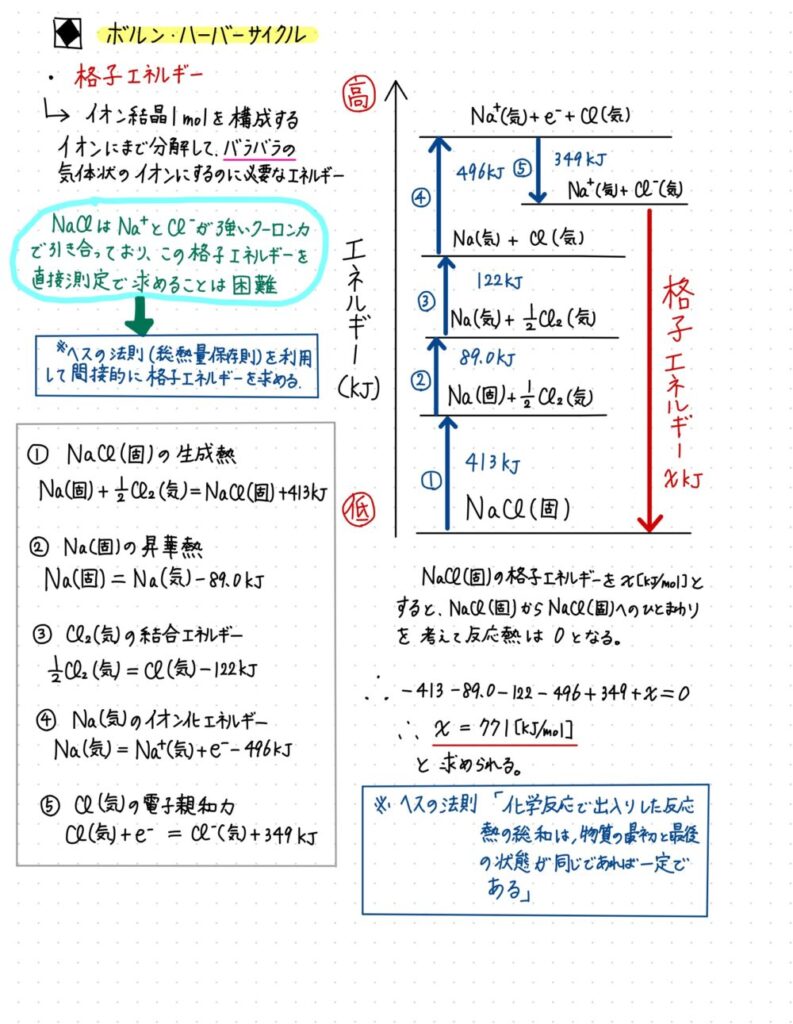
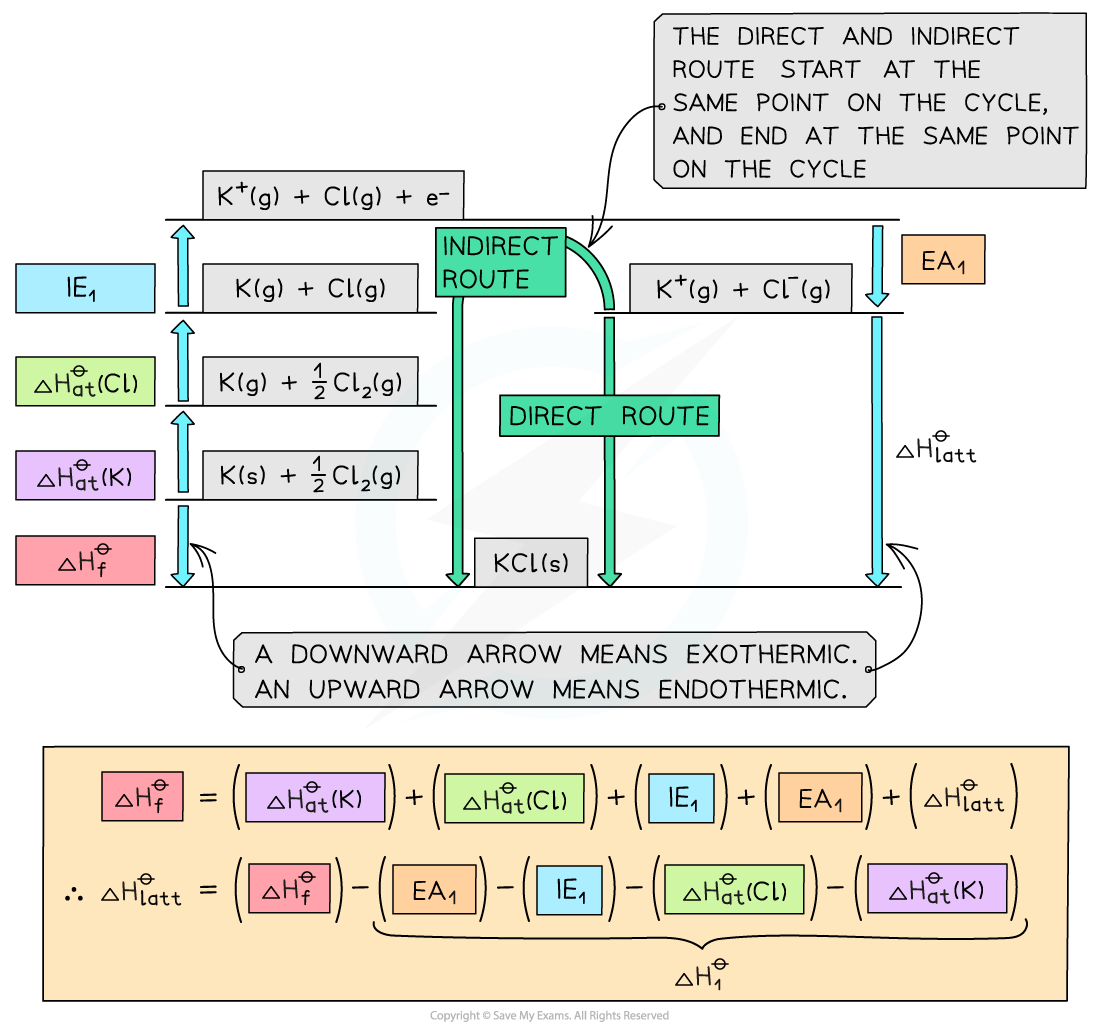
ボーン・ハーバー サイクルは、 ヘスの法則 (反応の エンタルピー 変化を決定するため) の応用の 1 つと考えられており、このサイクルを通じて イオン性化合物 の網様体エンタルピーを間接的に (他の変数を使用して) 測定することができます。

格子エンタルピーは、 気体状態 のイオンが結合して固体状態の生成物を形成するときに放出されるエネルギー、またはイオン性化合物が気体イオンに分解されるのに必要なエネルギーとして定義できます。良い例は、化合物 LiF (フッ化リチウム) のエンタルピーの決定です。
LiF (s) に関連する格子エネルギーは、次の方程式で表すことができます。
- LiF (s) → Li + (g) + F – (g) Δ H f = U LiF
同様に、固体リチウムとガス状フッ素からの LiF の 生成エンタルピーは 次 の方程式で与えられます。
- Li (s) + 1/2F 2(g) → LiF (s) Δ H f = -594.1 KJ
リチウムとフッ素のガス状イオンへの変換を分析すると、次のエンタルピー変化値が得られます。
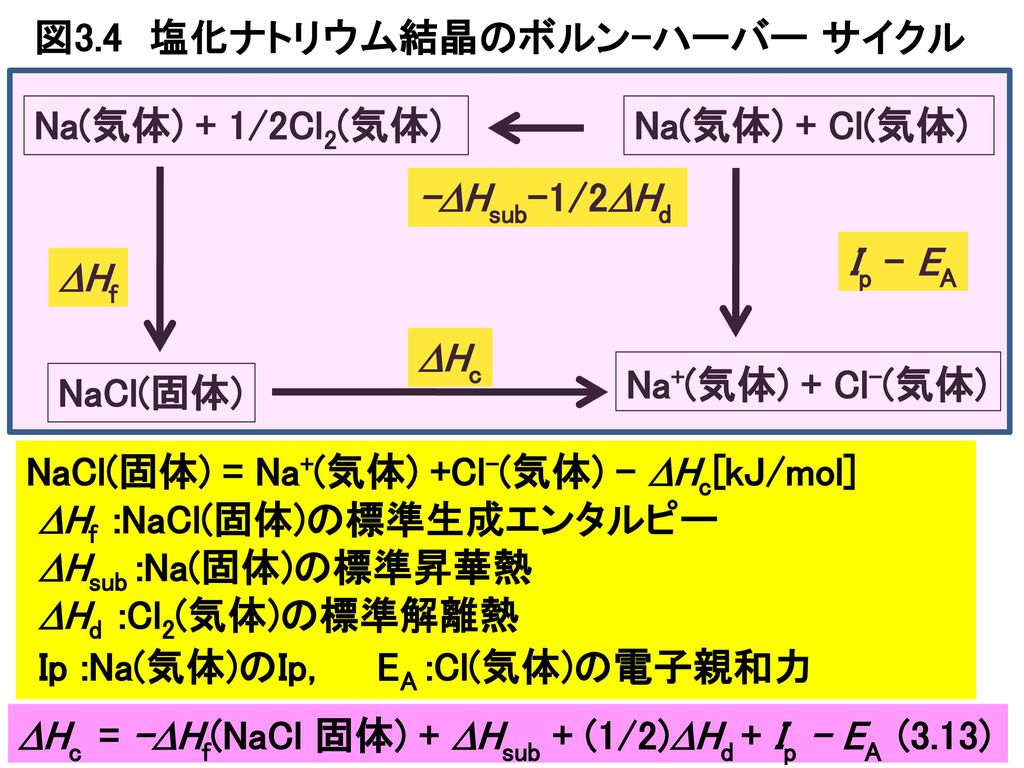
- Li (s) → Li (g) ΔH s = 155.2 KJ
- Li (g) → Li + (g) + 1e – ΔH I1 = 520.0 KJ
2) フッ素 の場合、解離 (結合の切断による分子の分離) およびイオン化 (ただし電子の獲得を伴う) のプロセス:
- 1/2F 2(g) → F (g) ΔH d = 1/2 ΔH 0 d = 150.6/2 = 75.3 KJ
- F (g) + 1e – → F – (g) Δ H AF1 = -328.0 KJ
これらのステップを経た後のイオン間の反応は次のように表されます。
- Li + (g) + F – (g) → LiF (s) Δ H f = – U LiF
ヘスの法則を使用すると、各中間ステップのエンタルピー変化の合計は、あたかも単一の経路で起こったかのように最終反応のエンタルピー変化をもたらします。したがって、LiF (s) の生成エンタルピーはエンタルピーの合計に等しくなります。固体リチウムの昇華とイオン化、フッ素の解離とイオン化(電子を受け取るときの 電子親和力 によって測定)に、化合物に関連する格子エネルギーを加えたものです。つまり:
- ΔH f = ΔH s + ΔH I1 + ΔH d + ΔH AF1 – U LiF
- -594.1 = 155.2 + 520 + 75.3 – 328 – U LiF
- -594.1 = 422.5 – U LiF
- U LiF = 1,016.6 KJ

したがって、フッ化リチウムの格子エンタルピーは 1,016.6 KJ/mol に等しいため、この化合物を気体状態のイオンに変換するには、少なくともその量のエネルギー (物質の量に比例) を提供する必要があります。 。
以下の図も同様に 、U LiF 決定プロセス全体を表しています。
 参考文献:
参考文献:
http://www.aridesa.com.br/servicos/click_professor/alexandre_lima/Ciclo_de_Born_Haber.pps
(2011 年 1 月 8 日閲覧)
ギャラリー