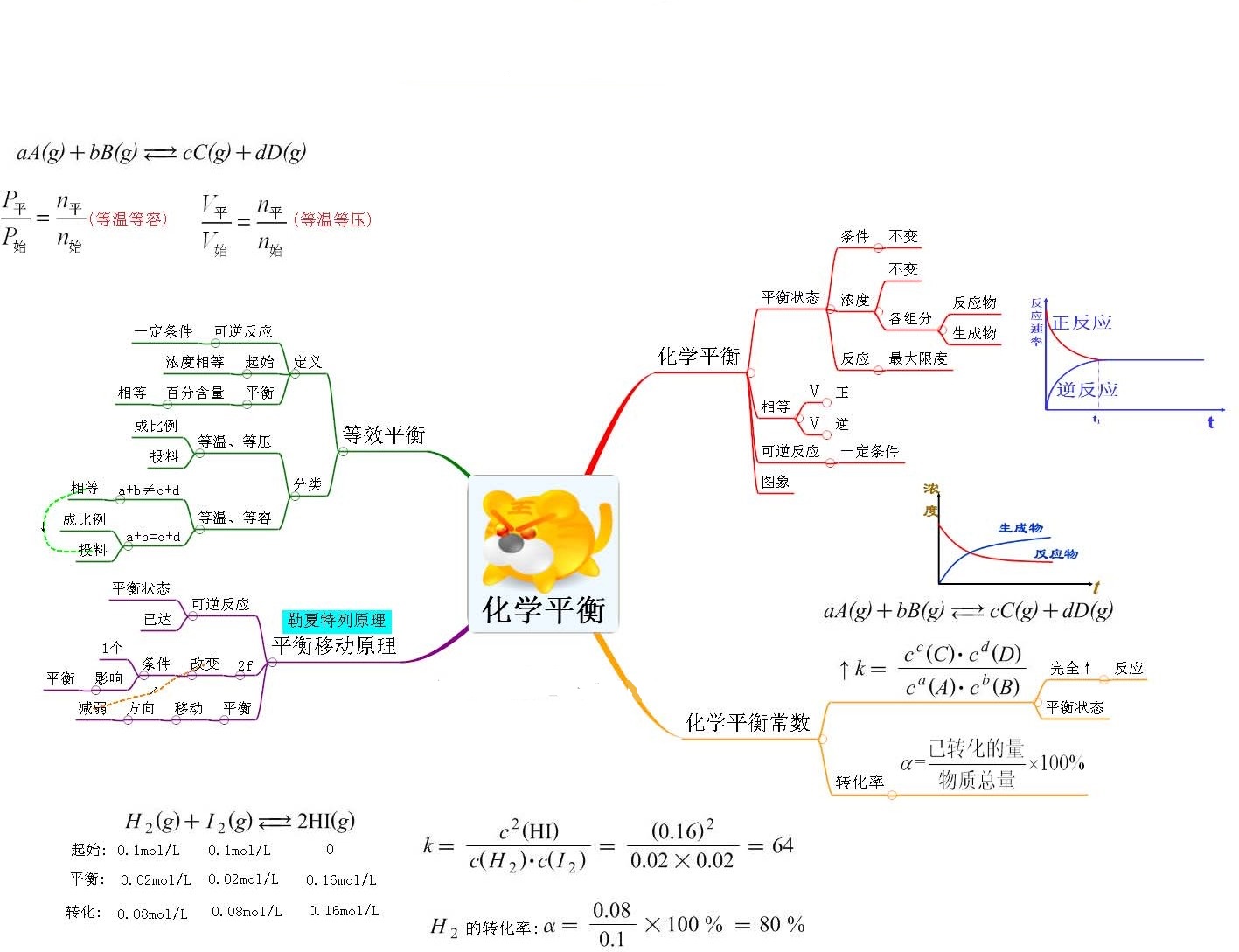
化学平衡の変化の原因の分析を開始するには、 化学平衡が 一定の濃度と等しい反応速度 (直接および逆) を持つ可逆反応として定義されることを理解する必要があります。
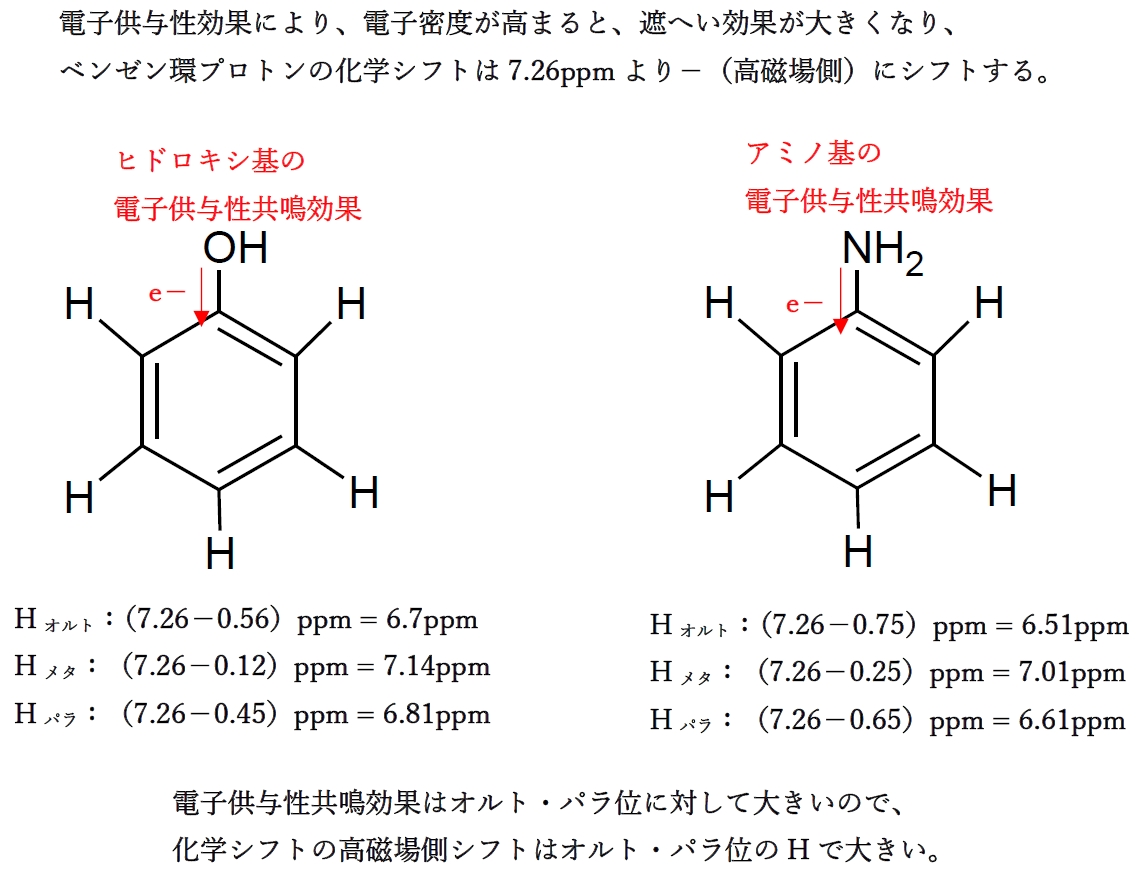
いくつかの要因が、この平衡を反応物または生成物の方にシフトさせる原因となります。この現象は、次のような ル シャトリエの法則 に基づいています。「平衡状態にあるシステムが、いずれかの成分の濃度、温度、または圧力の変化によって乱されると、その影響を相殺するためにシステムは平衡位置を移動します。」騒動の。 」
1884 年、科学者シャトリエは、平衡の変位に対する圧力の影響を説明する理論を発表しましたが、1888 年に理論を改良し、温度や濃度の変化などの外部効果に拡張しました。

この理論の発展は、主に工業的な方法でアンモニアを入手できるようになったために、産業界にとって非常に重要でした。アンモニアは、他の多くの用途の中でも特に、肥料(尿素など)、プラスチック、洗剤の原料として産業界で広く使用されています。
以下では、化学平衡の変化に対するさまざまな要因の影響について具体的に説明します。
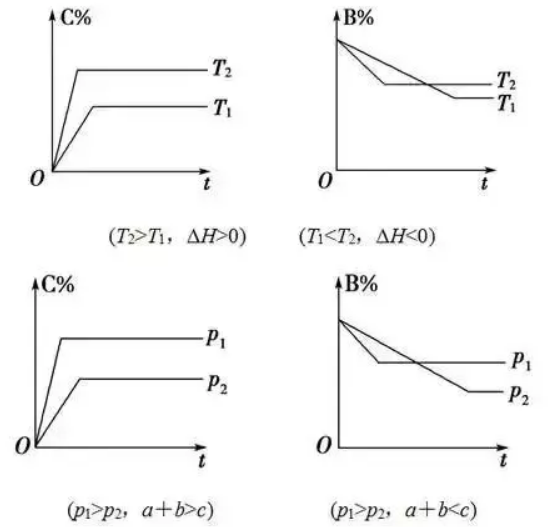
圧力変化の影響: 圧力が増加すると、平衡は分子の数が最も少ない側に移動し、圧力が減少すると、平衡は生成される分子の数が最も多い側に移動します。
例: 2 A ↔ B

この場合、圧力が増加すると、分子の数が増えるため、平衡は左に移動します。
濃度変動の影響: 反応物の濃度が増加すると、バランスは生成物の方にシフトし、その逆が発生すると、バランスは反応物の方にシフトします。

例:A ↔ 2B
この場合、A の濃度を増加すると、平衡は 2B の形成に向けてシフトします。
温度変化の影響: 温度が上昇すると平衡は吸熱反応に有利にシフトし、温度が低下すると平衡は発熱反応に有利にシフトします。
例: 2 A + O 2 ↔ B + CO 2 ∆ H – + x Kj/mol
この場合、直接反応は燃焼反応、つまり発熱を表すため、温度が低下すると平衡が有利にシフトします。
ギャラリー