隔壁で区切られた、堅い壁で断熱されたコンテナを考えます。コンパートメントの 1 つに ガス が入っており、もう 1 つは空であると仮定します。

隔壁を取り除くと、ガスはいわゆる自由膨張を起こし、仕事も 熱も伝達されません 。 熱力学の第一法則 (ΔU = Q – W) によれば、Q と W は変化しないため、内部エネルギーは変化しないことがわかります。この自由膨張において気体が温度変化を受けるかどうかを調べるために、科学者のジュールは 1843 年にいくつかの実験を実施しました。これは ジュール効果 として知られる実験です。

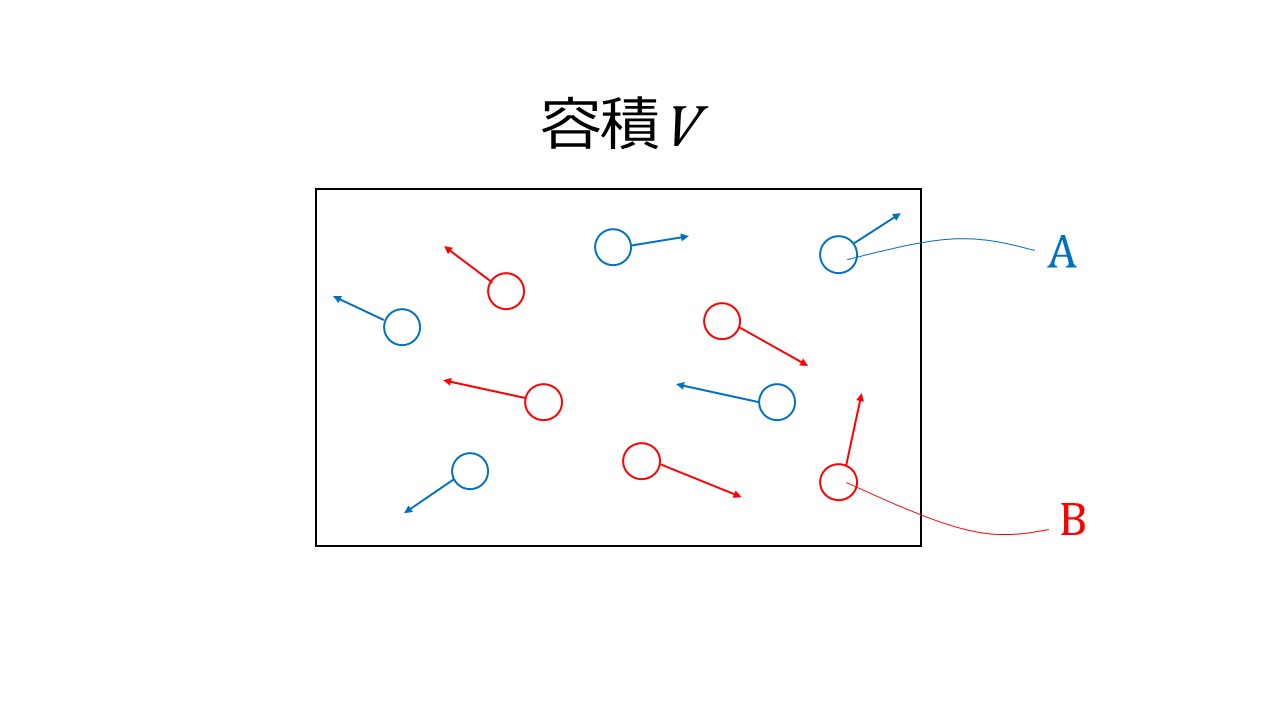
内部エネルギーと体積または圧力の変化との間に何らかの関係を確立しようとするために、ジュールは元の実験で 2 つの容器 (図に示すように) を浸し、1 つはガス、もう 1 つは真空にしました。水温変化の前後で温度を測定した。この実験では、水とジュール容器の 比熱 の差については何も決定できません。

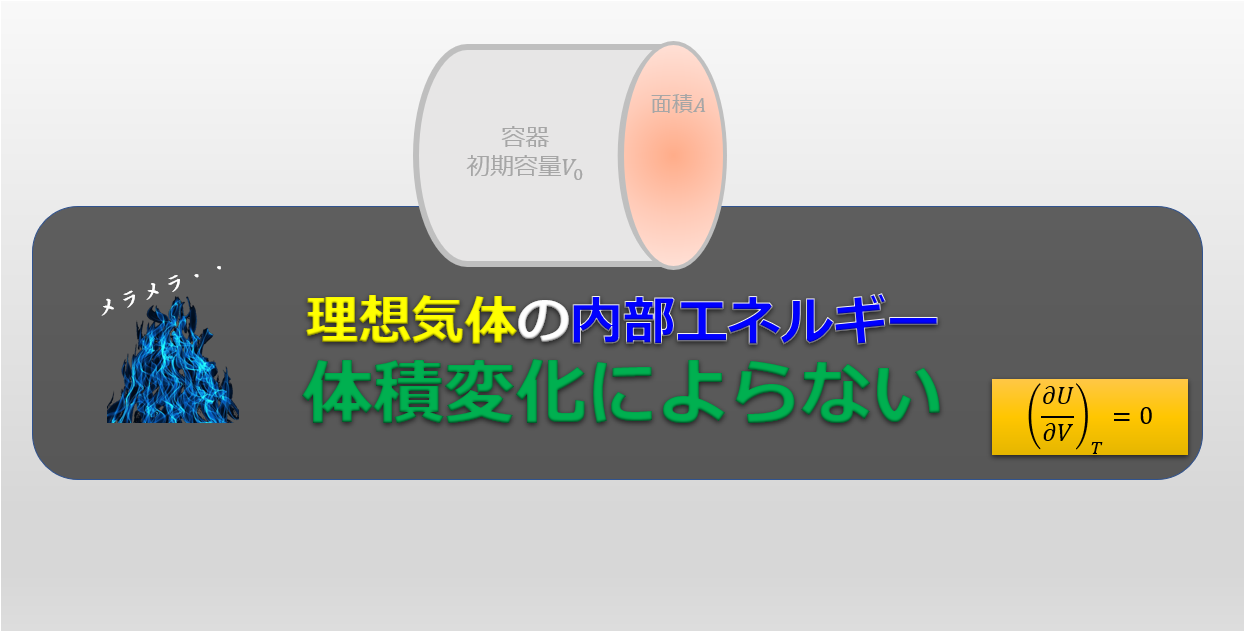
今日、実際の気体の内部エネルギーは、温度だけでなく圧力や体積にも依存することが知られています。ただし、圧力と体積への依存性は非常に小さく、温度への依存性は非常に高くなります。結論として、気体の内部エネルギーは、その気体が受ける温度変化に直接依存すると言えます。
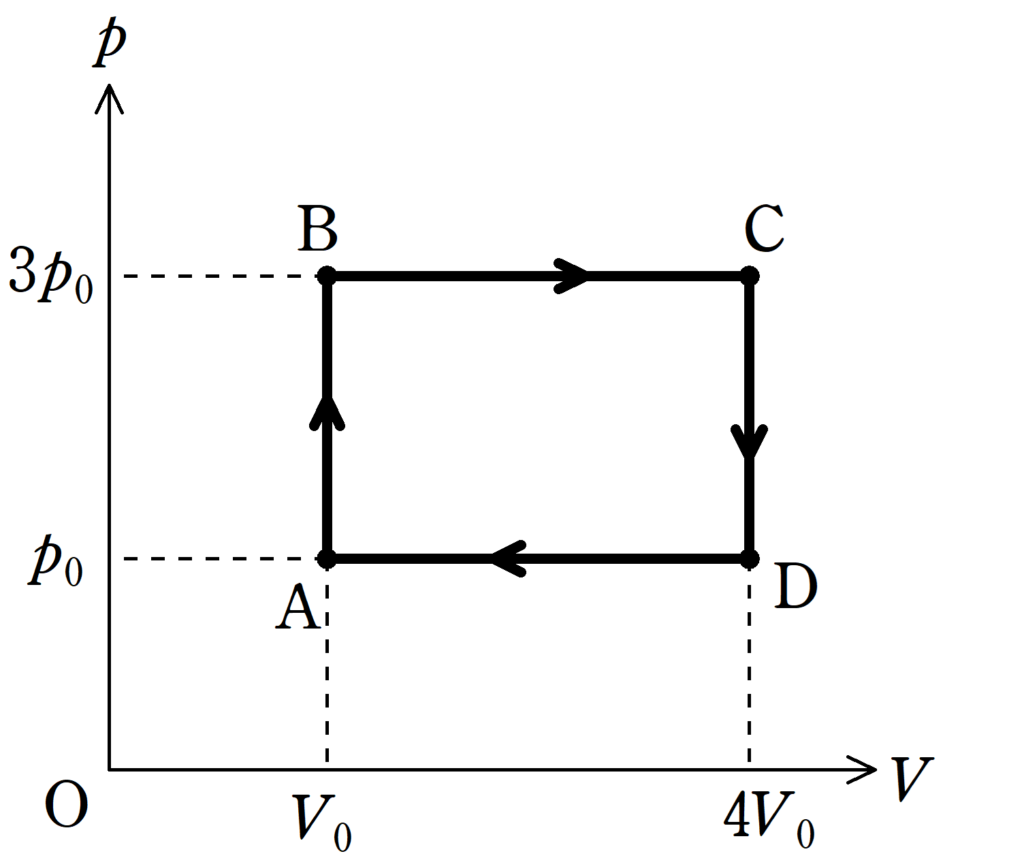
内部エネルギーの変化は圧力や体積の変化に依存しないので、P×Vのグラフでは経路に依存しないと言えます。 2 つの断熱間の物体の内部エネルギーの変化を計算してみましょう。

ΔU
AB
=
Qv
= mcΔT
ΔU
BC
= 0 (断熱)

したがって、温度変化があるABプロセスでは内部エネルギーの変化のみが生じます。
ギャラリー