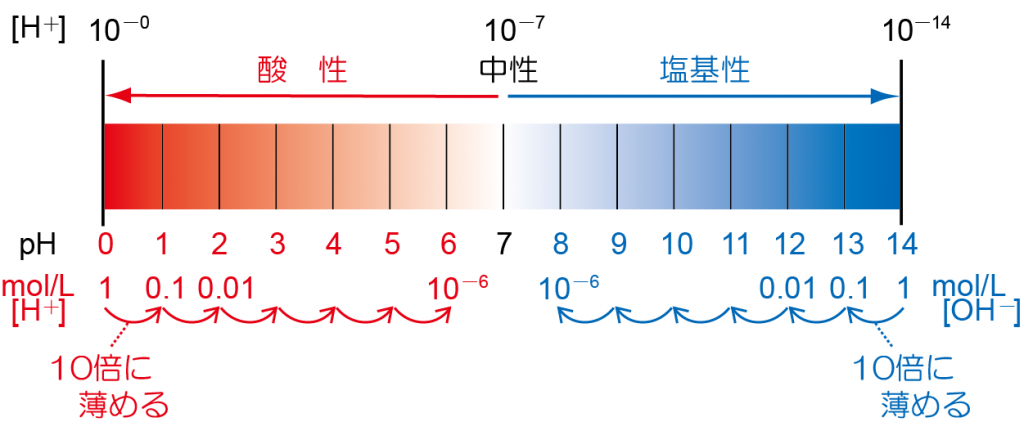
溶液 の濃度は、基本的に 2 つの異なるプロセスによって下げることができます。 希釈 (溶媒の量が増加し、その結果、溶液の量も増加する)、または別の溶液 (または同じ溶質、より低い濃度、または別の溶質) を混合することです。 、元の溶液とは化学反応しません)。どちらの場合も、溶質の増加はなく、溶液の最終体積が増加し、濃度の低下につながります。

溶液の濃度を下げる際に最も一般的な希釈プロセスは、溶媒を加えて溶液の体積を増やすことで構成され、結果として濃度が低下します。希釈は化学実験室で日常的に行われるだけでなく、たとえば豆に水を加えたり、濃縮果汁に水を加えたりするときにもこのプロセスが行われます。どちらの場合も、溶液の体積を増やし、その溶液中の溶質の濃度を減らします。

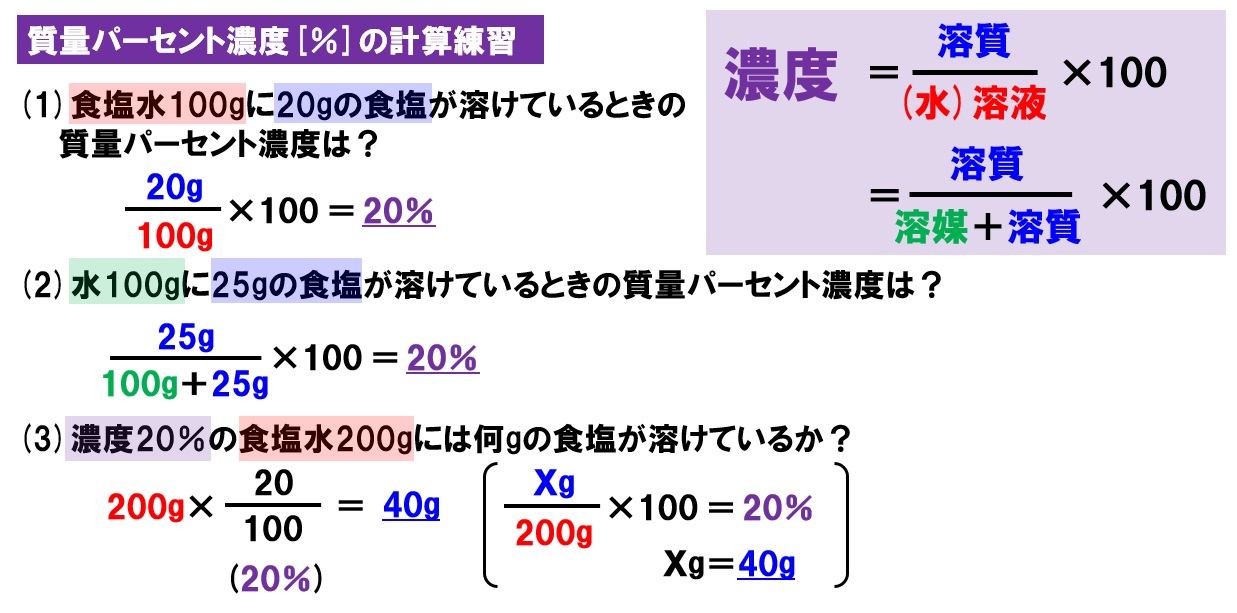
数学的には、以下の方程式に従って、最も一般的に使用される濃度 (C)、モル濃度 (M)、標準濃度 (N) のいずれかで希釈を表すことができます。
- 一般的な濃度; C 1 V 1 = C 2 V 2
- モル濃度; M 1 V 1 = M 2 V 2
- 通常の濃度。 N 1 V 1 = N 2 V 2
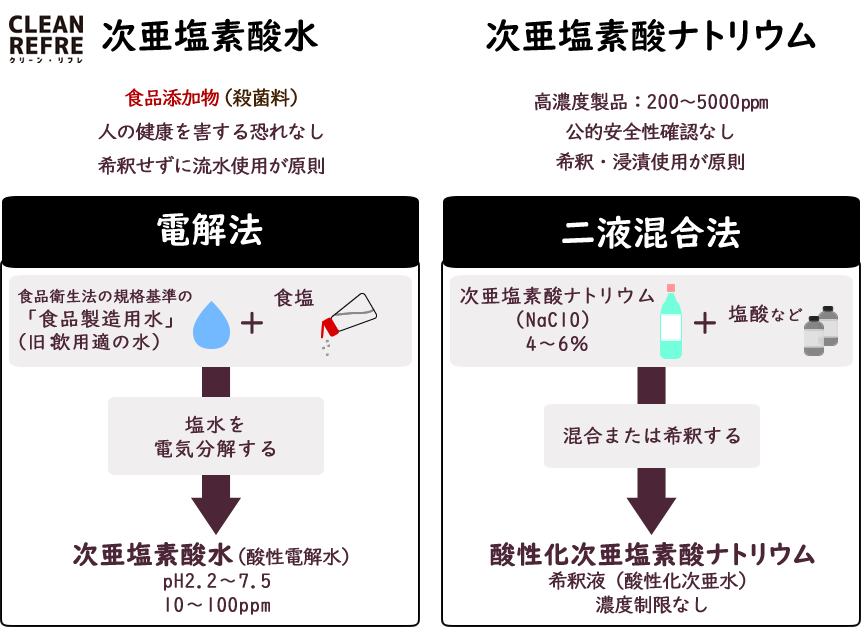
2 つ以上の溶液の混合物の場合、次の 3 つの異なる可能性が考えられます。
- 同じ溶質からなるもの。
- 1 つは別個の溶質で構成されていますが、互いに化学的に反応しません。
- または、異なる溶質で構成されている場合でも、化学反応が発生します。

3 番目に関しては、初期のものとは異なる化学種の形成があり、したがって、溶質の初期濃度は考慮できなくなります。これは、溶質 (またはそれらの少なくとも 1 つ) が結果の生成物中にもはや存在しないためです。解決。第2および第3のプロセスに関しては、第2の場合、第2の溶液の溶質濃度が第1の溶液の溶質濃度よりも低いという条件で、濃度が低下する。

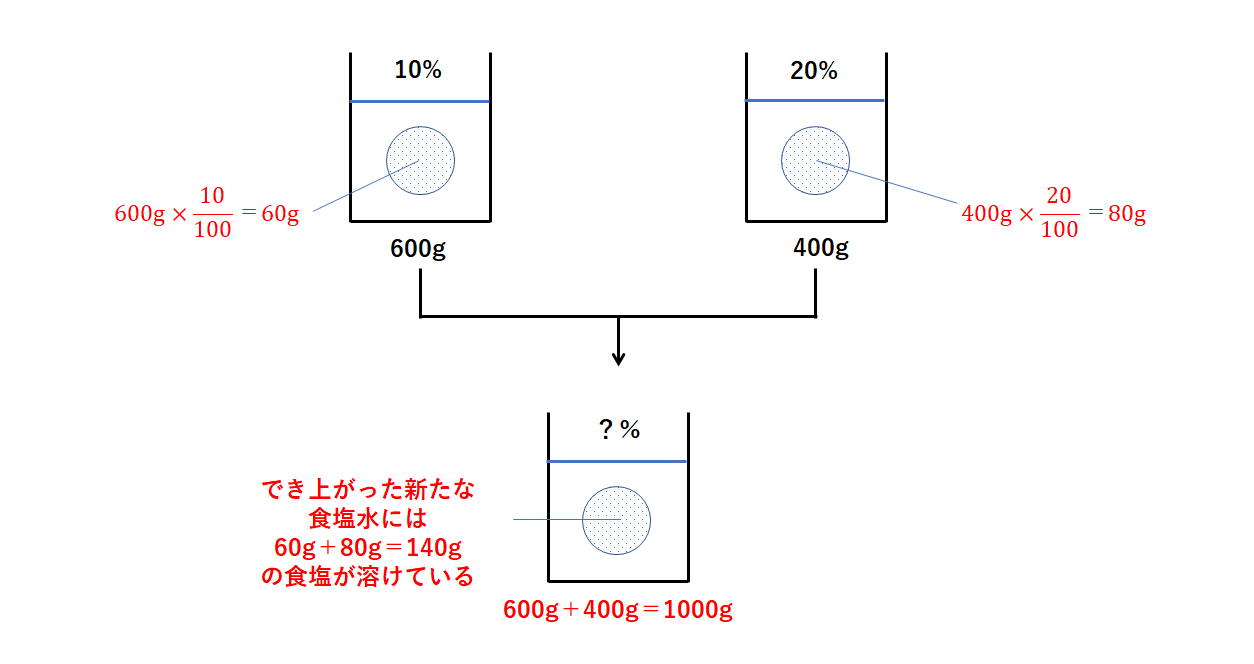
2 番目のプロセスで説明した混合物の場合でも、同じ溶質からなる 2 つ以上の溶液を混合するのが非常に一般的です。この場合、個々の体積を合計する必要があり、結果として得られる濃度は常に個々の濃度の中間になります。数学的には、希釈プロセスと同様に、2 つ以上の溶液の混合物も、最も一般的に使用される溶液 (C)、モル濃度 (M)、標準濃度 (N) のいずれかを使用して、以下の方程式に従って表すことができます。
- 一般的な濃度; C 1 V 1 + C 2 V 2 = C 3 V 3
- モル濃度; M 1 V 1 + M 2 V 2 = M 3 V 3
- 通常の濃度。 N 1 V 1 + N 2 V 2 = N 3 V 3
参考文献:
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
サルデッラ、アントニオ。マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
ギャラリー