化学反応の効率が 100% に達することはほとんどありません。元の反応物に代わる生成物が常に存在するためです。したがって、可逆性がほぼゼロであっても、 すべての反応は可逆的である と言えます。



HCl (水溶液) + H 2 O (l) → H 3 O + (水溶液) + Cl – (水溶液)
反応の方向は単一の矢印で示されていますが、これは最も正しい方法ではありません。反応は酸の完全な解離では起こらず、一部は常に分子の形で残ることが実験的に確認されています (約 8%)。
ケミカルバランス
塩酸の脱プロトン化反応に戻ると、それを表す最良の方法は次のとおりです。
HCl (水溶液) + H 2 O (l) ⇌ H 3 O + (水溶液) + Cl – (水溶液)
二重矢印記号 (⇌) は、反応が両方向に進行することを意味します。したがって、リバーシブルです。
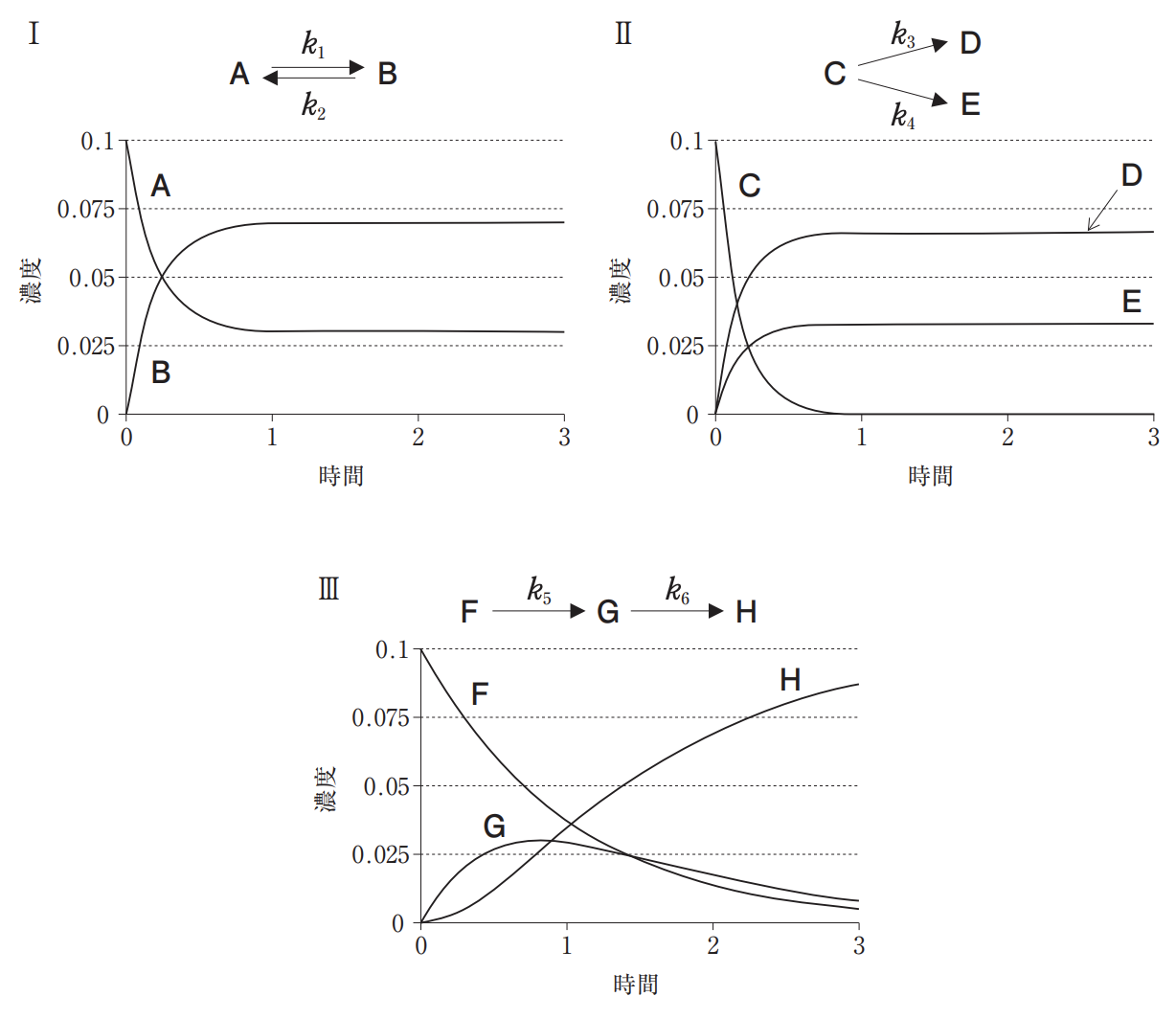
H 3 O + と Cl – の形成は、反応物がある速度で戻されるのと同じように、ある速度で発生します (最初は最初とは異なります)。これらが等しくなるとき、いわゆる 化学平衡 に達します。これは、生成物の形成速度が反応物の復元速度と同じであることを示しています。
この平衡点からは、どれだけ放置しても反応収率は変わらず、酸のイオン化・解離プロセスは停滞します。

平衡に達した後、生成物の形成速度は反応物の復元速度と等しくなります。
反応の 平衡定数 は、生成物と反応物の濃度、およびそれぞれの化学量論係数の関数です。
一般的な反応の場合: aA + bB ⇌ cC + dD
次の平衡定数値があります。
塩酸の解離反応の場合、平衡定数の値は次のとおりです。
各反応 (直接反応と逆反応) の速度方程式を使用すると、同じ Kc 値が得られます。
一般的な反応を考える: aA + bB ⇌ cC + dD
製品形成の速度は次のとおりです。
ここで、K’ は反応と温度によって変化する定数です。
反応物の復元速度については、次のようになります。
ここで、K も (K’ と異なるかどうかに関係なく) 反応と温度によって変化する定数です。
平衡状態では、形成速度と復元速度が等しいことがわかっているため、次のようになります。
ギャラリー

反応の速度式と濃度比.jpg)


反応 薬剤師国家試験.jpg)