化学反応が起こるには、関与する種 ( 原子 、 分子 、 イオン ) が機械的衝撃を通じて相互作用する必要があります。したがって、これらの衝突を通じて、活性化された複合体が形成され、その後最終生成物が形成されます。
活性化された複合体は、反応物と生成物の間の中間状態にすぎず、反応物分子の結合が弱まり、結合が強固な生成物が瞬時に形成されることを特徴とします。衝撃は無秩序に発生し、反応は瞬間ごとに起こるため、それらは非常に短期間しか存在しません。

ただし、活性化された複合体が形成されるには、種の電子圏の近接によって生じる反発力に打ち勝つために一定量のエネルギー、いわゆる 活性化エネルギー が必要です。したがって、それは反応物間の衝突や結合の切断に関与しており、たとえば熱の形で供給される可能性があります。

 触媒は、活性化エネルギーを減少させることで反応を促進する特定の条件(接触の改善、より効果的な衝突や pH の変化など)を媒体内に作り出すことができ、その結果、反応の平衡状態に、より迅速に、しかし置換されることなく到達します。 。言い換えれば、触媒を使用しないプロセスでも触媒を使用するプロセスでも同じ量の生成物が得られますが、違いはその量が生成されるまでに必要な時間だけです。
触媒は、活性化エネルギーを減少させることで反応を促進する特定の条件(接触の改善、より効果的な衝突や pH の変化など)を媒体内に作り出すことができ、その結果、反応の平衡状態に、より迅速に、しかし置換されることなく到達します。 。言い換えれば、触媒を使用しないプロセスでも触媒を使用するプロセスでも同じ量の生成物が得られますが、違いはその量が生成されるまでに必要な時間だけです。
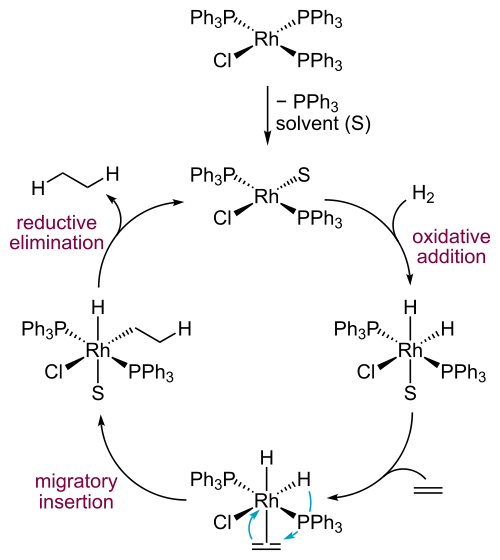
一連の反応における触媒の作用
触媒は 試薬封鎖剤として機能することができ(したがって、気体床または液体床における固体触媒の原理)、触媒が効果的に衝突した後、生成された生成物が放出され、反応物 + 触媒 → 製品 – 触媒という新しいサイクルが始まります。
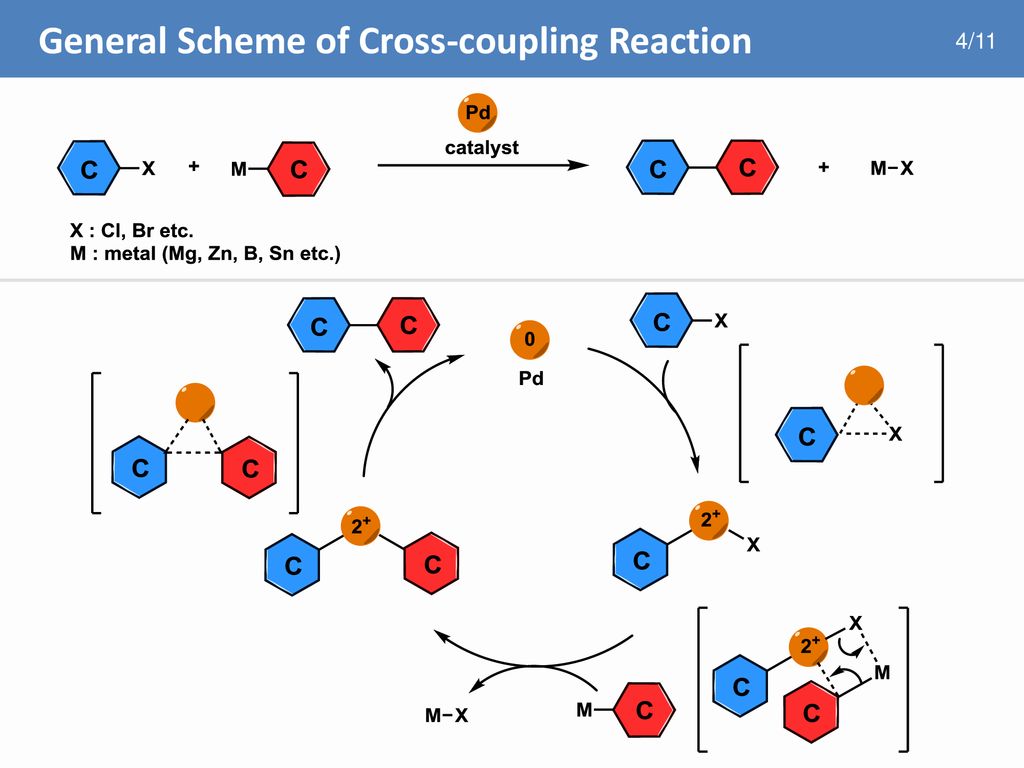
次のスキームは、一般的な反応 A + B → C に対する触媒の作用を示しています。
見てわかるように、反応物 A が触媒に加わります。次に、反応物 B は同じ経路をたどり、活性化された複合体 AB を形成します。即座に生成物 C が形成され、触媒から離れますが、これが遊離すると、再び反応物 A および B に結合して、再び生成物 C が生成されます。このプロセスは、反応物が使い果たされるか、触媒が汚染されるまで継続します。
非常に単純な 触媒サイクルは 、ヨウ化物イオンの作用によって 過酸化水素 (過酸化水素) が水と遊離酸素に分解されることです。
既存のメカニズムは次のとおりであり、ヨウ化物イオンは各一連の反応の最後に常に回収されることに注意してください。
H 2 O 2(aq) + I – (aq) → OI – (aq) + H 2 O (l)
H 2 O 2(aq) + OI – (aq) → I – (aq) + H 2 O 2(l) + O 2(g)
ギャラリー