蒸発 または 気化は 、私たちが日常的に観察する現象であり、衣類を吊り干しするときや、香水の匂いを嗅ぐときでも、水や香水の分子が液相から気相に逃げる 相変化を 観察しています。 。開放的な環境では、このプロセスは、たとえば衣服が乾くまで継続的に発生します。

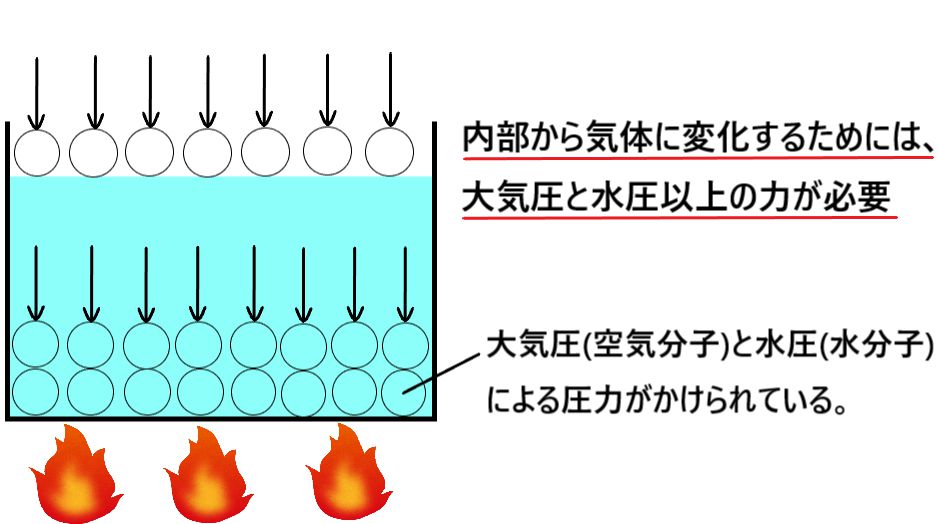
特定の物質の液体が入った密閉容器内では、より大きな運動エネルギーを持つ分子が液体から逃げる蒸発も起こります。生成されたこの蒸気は液体に圧力を及ぼし、2 つの相が熱力学的平衡状態になるとき、この圧力は 蒸気圧 と呼ばれます。
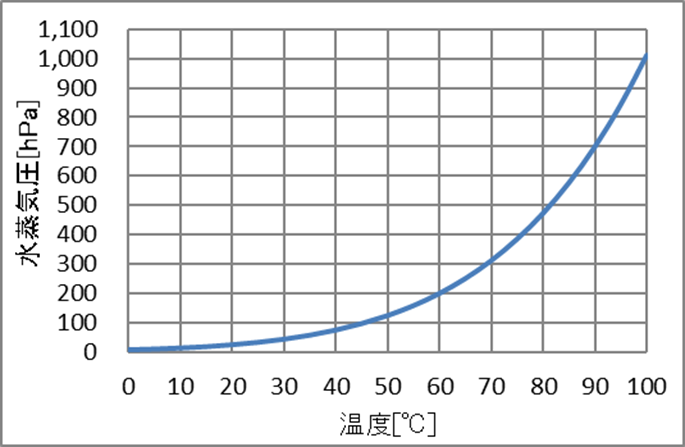
蒸気圧は物質の揮発性の尺度です。蒸気圧が高い物質は揮発性が高く、蒸気圧が低い物質は揮発性が低い物質です。揮発性は物質の化学的性質に依存し、分子を結合させる力、 ファンデルワールス力 と密接に関係しています。 水素結合 などの強い 分子間相互作用 を持つ物質は蒸気圧が低いため、揮発性が低くなります。一方、ロンドン分散力などにより相互作用が弱い物質は蒸気圧が高くなるため、揮発性が高くなります。
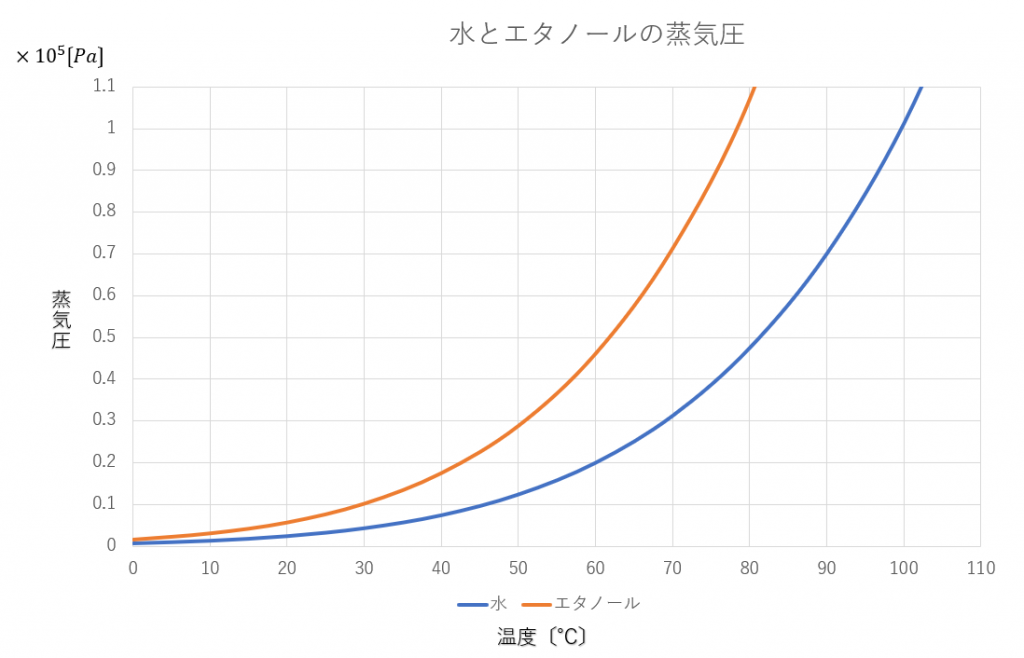
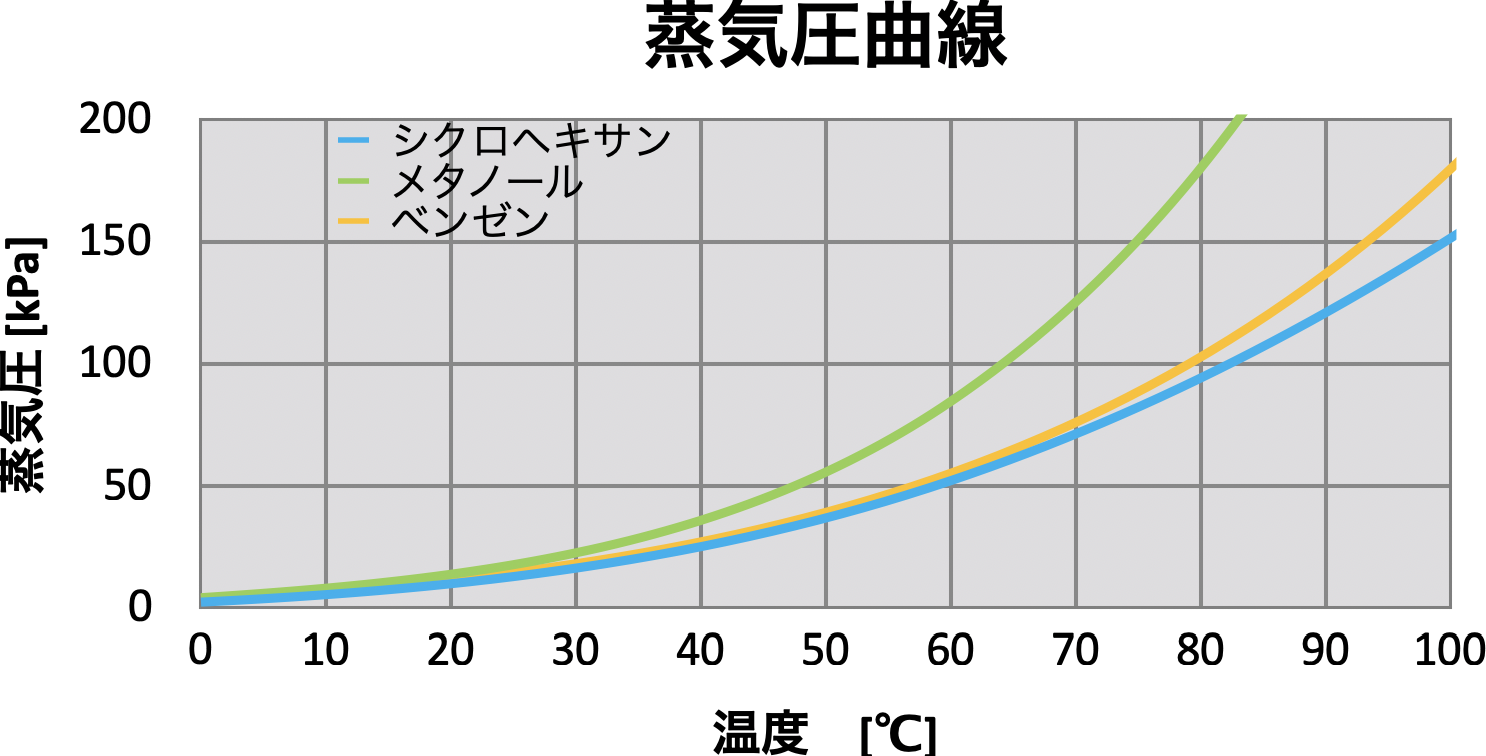
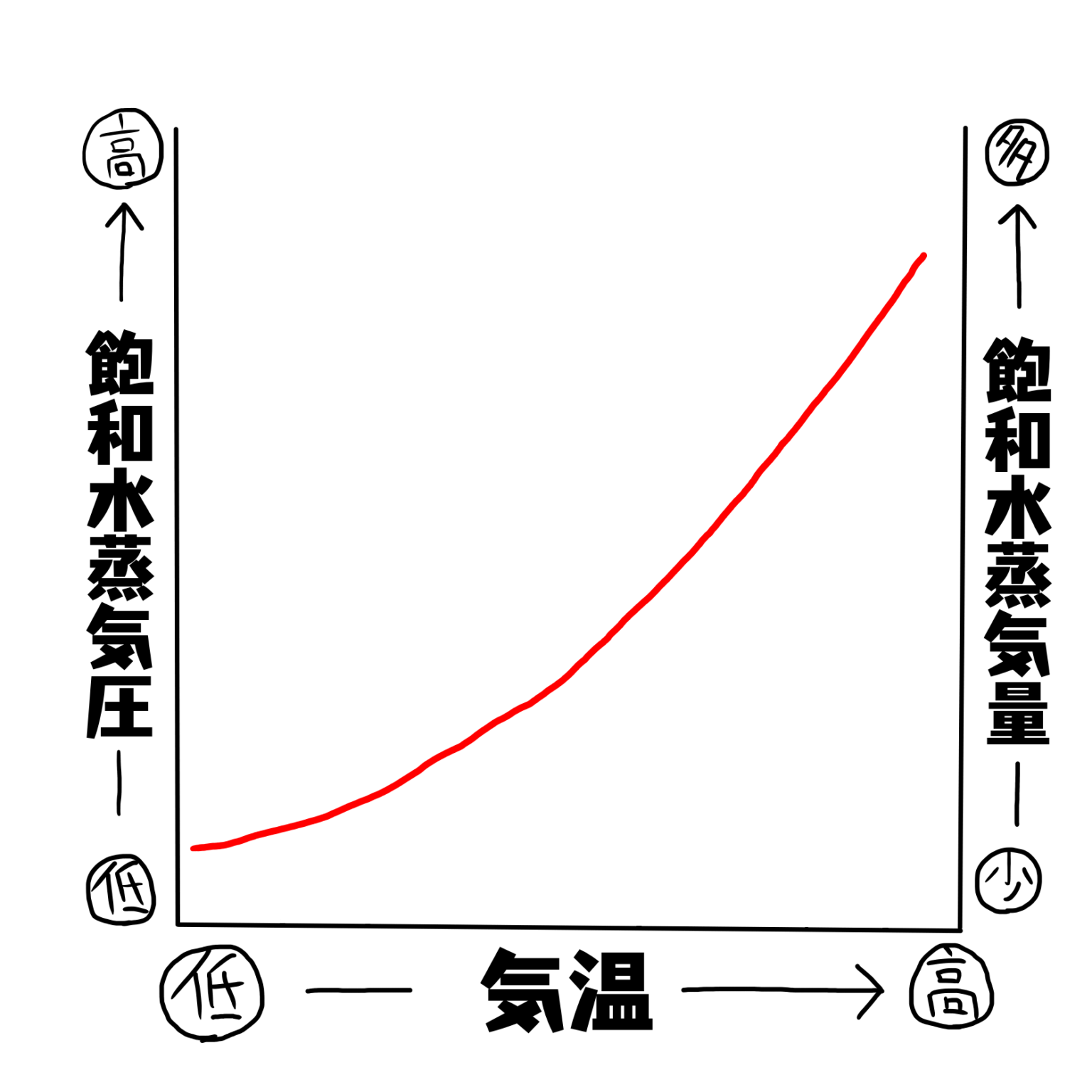
蒸気圧は系の温度に強く依存し、温度が高くなるほど化合物の蒸気圧も高くなります。温度が高くなるほど、より多くの物質が気相に入る傾向があるため、これは相変化の概念と一致しています。さまざまな目的のために、任意の温度における物質の蒸気圧を予測する方法を知ることは興味深いことです。この意味で、いくつかの式が開発されました。そのうちの 1 つは、熱力学的議論から導かれたクラウジウス-クラペイロン方程式です。
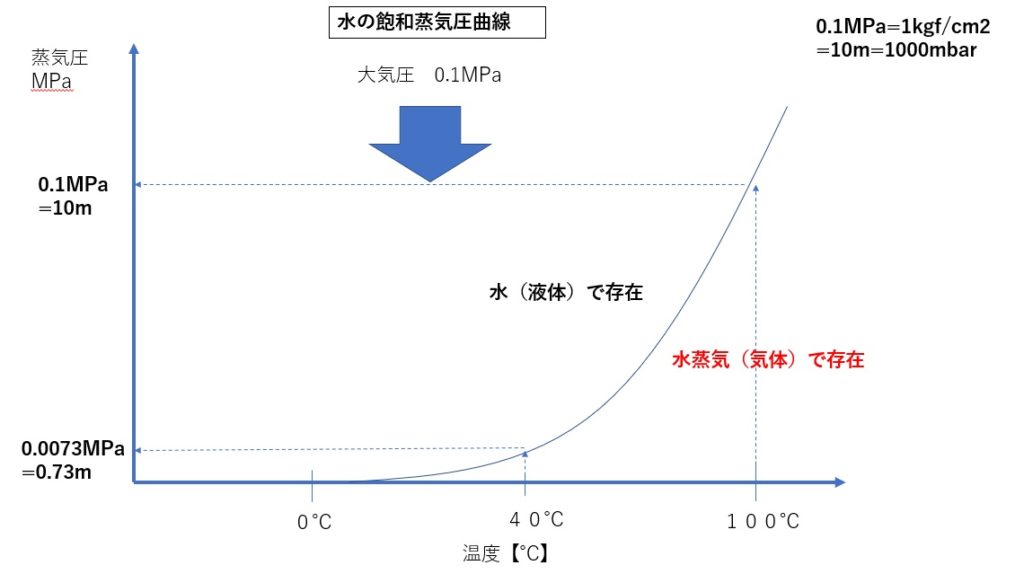
ここで、 は温度における蒸気圧、 は物質の蒸発のエンタルピーです。この方程式は便利ではありますが、常に有効であるとは限らない理想的なモデルに基づいています。このようにして、実験パラメータを調整して、いわゆる Antoine 方程式を取得する 2 番目の式がこれから導き出されます。
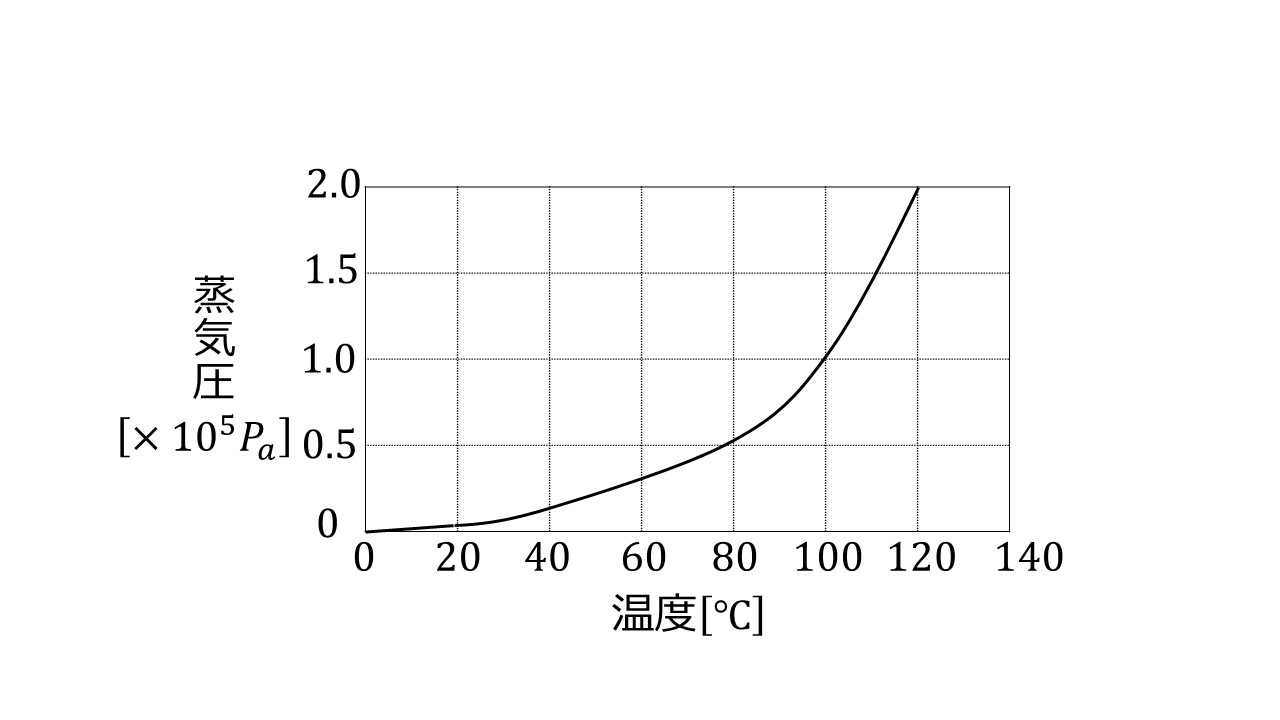
ここで、T は温度、A、B、C は各物質の特定の定数です。
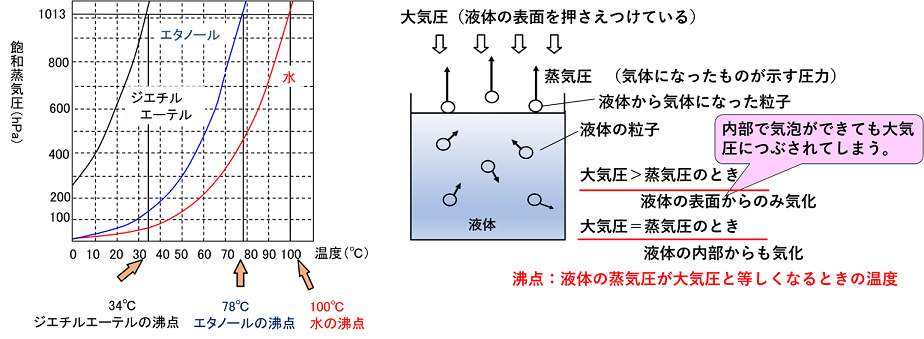
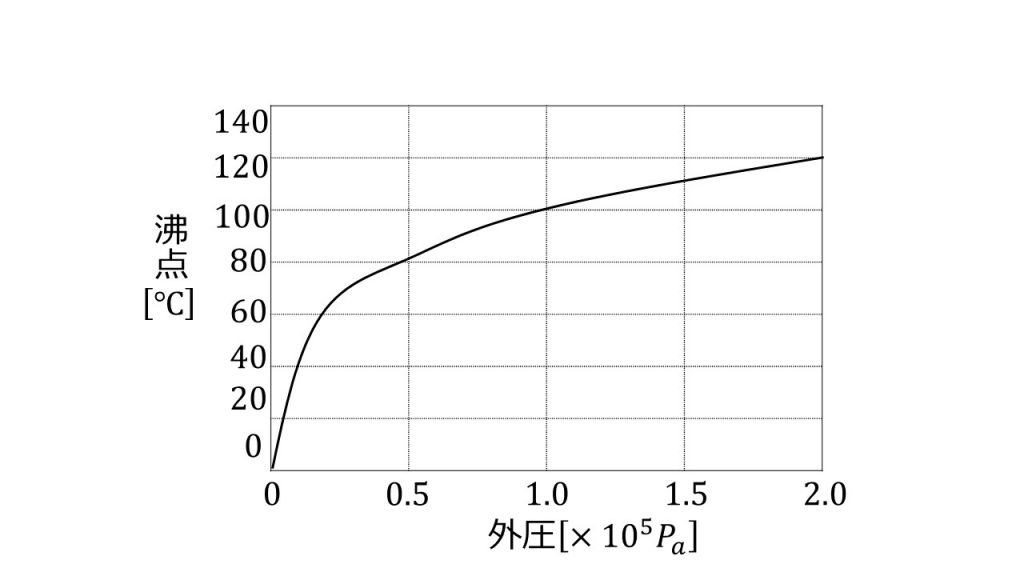
特定の温度では、液体の蒸気圧は外部圧力と等しくなり、これが起こると液体が 沸騰する ことが観察されます。物質の沸騰温度は、その蒸気圧が外部圧力と等しくなる温度になります。必要な圧力と必要なパラメーターを備えた前述の式を使用すると、特定の圧力における任意の物質の沸点を決定することができます。
参照:
アトキンス、P.W.ポーラ、フリオ・デ。物理化学。 8.編リオデジャネイロ: LTC、2008. 2 v. ISBN 9788521616009 (v.1)。
ギャラリー