しばしば 誤って 水素結合と呼ばれる 水素結合は 、分子間相互作用のタイプの 1 つです (他の相互作用には、イオン双極子、双極子双極子、ロンドン力などがあります)。したがって、これを 共有結合 とみなすことはできません。 電気陰性 度の高い原子との結合の安定性。
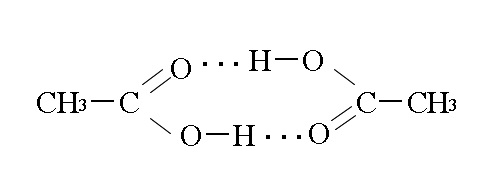
融点の高い液体は、切断するのに多くのエネルギーを必要とする水素結合型の相互作用を示すため、正確に観察できることがよくあります。場合によっては、液体が完全に沸騰した場合でも、このタイプの結合がいくつか気相に残ることがあります。たとえば、一定の質量の 酢酸 では、いくつかの二量体が H3CCOOH の形で共存しています。

水素結合の側面
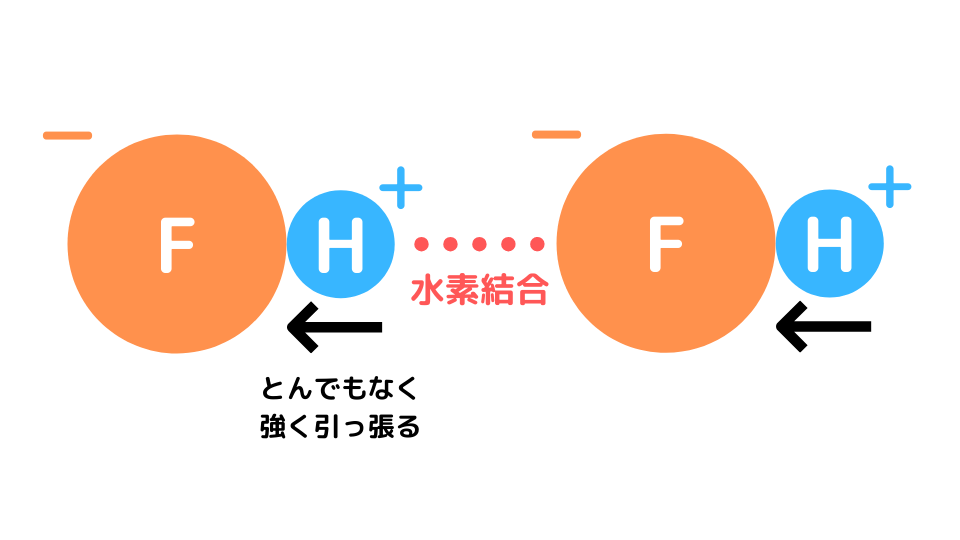
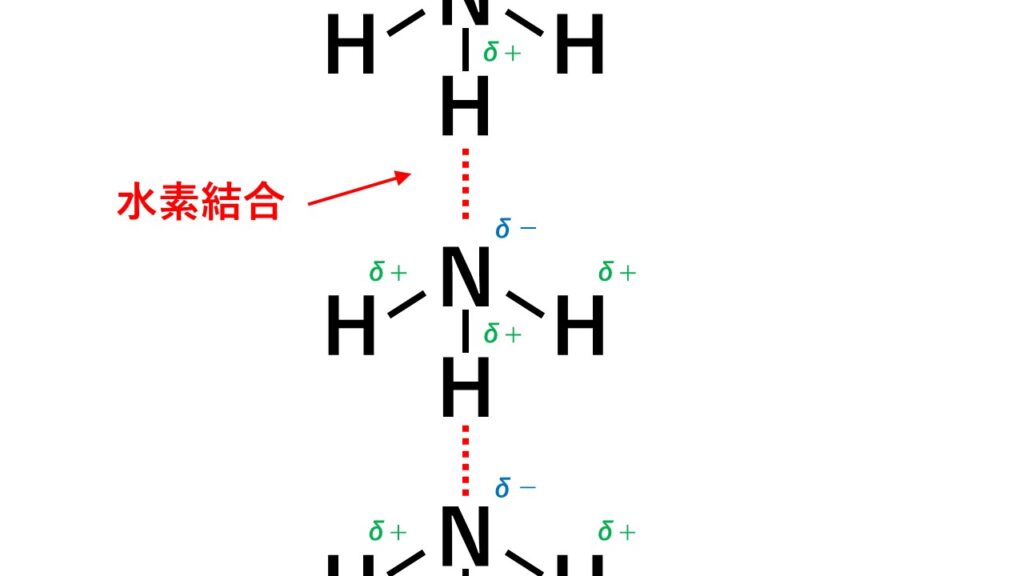
水素は、その部分電荷が正である場合にのみ、他の原子とこの種の結合を形成できます。したがって、電子対( 配位共有結合 )を受け入れることができます。
酢酸の場合、OH 基から水素を取り出すと、共有 電子 対が酸素原子により近い (より電気陰性である) ことがわかります。したがって、水素はこの結合において部分的に正電荷を持ちます。さらに、それは小さな原子であるため、別の分子の酸素原子(3 個ある)の孤立した電子対の 1 つに引き寄せられる可能性があります。
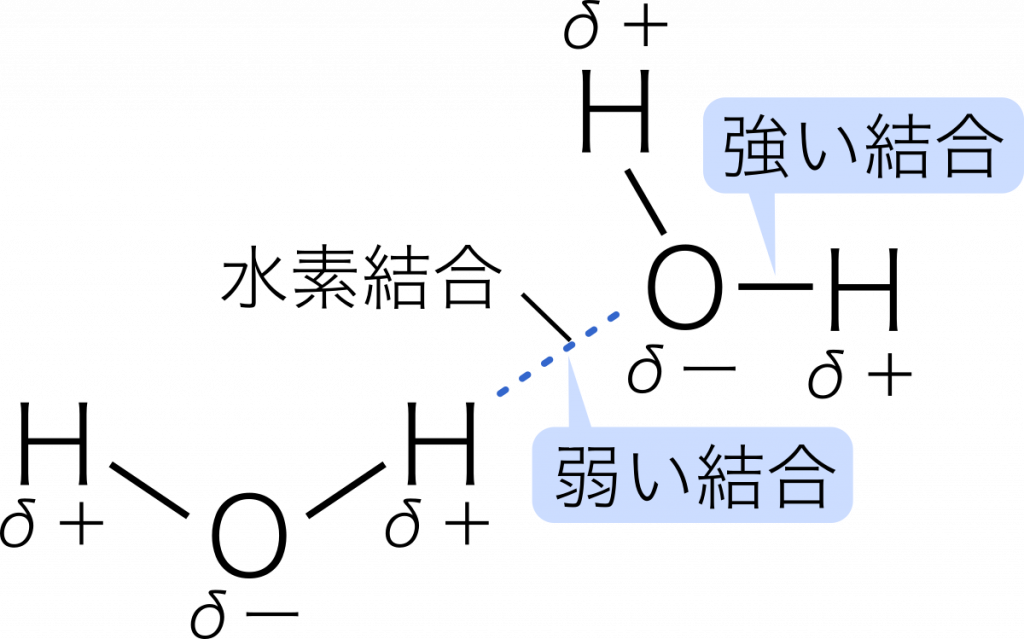
これにより、水素の部分的な正電荷とこの孤立した電子対、つまり水素結合自体によって引き起こされる非常に強い相互作用が生じます。
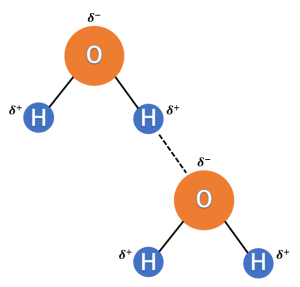
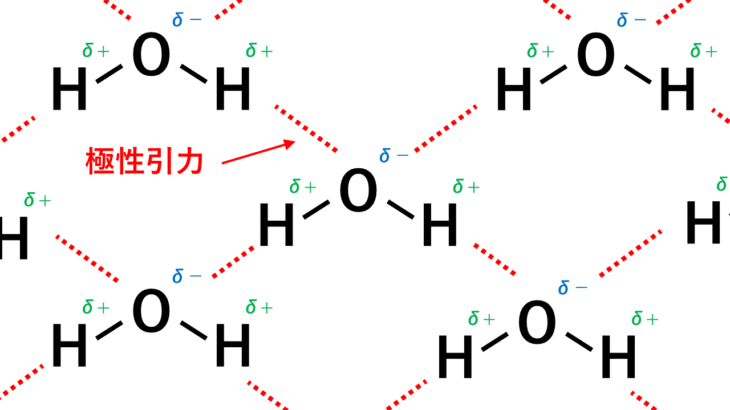
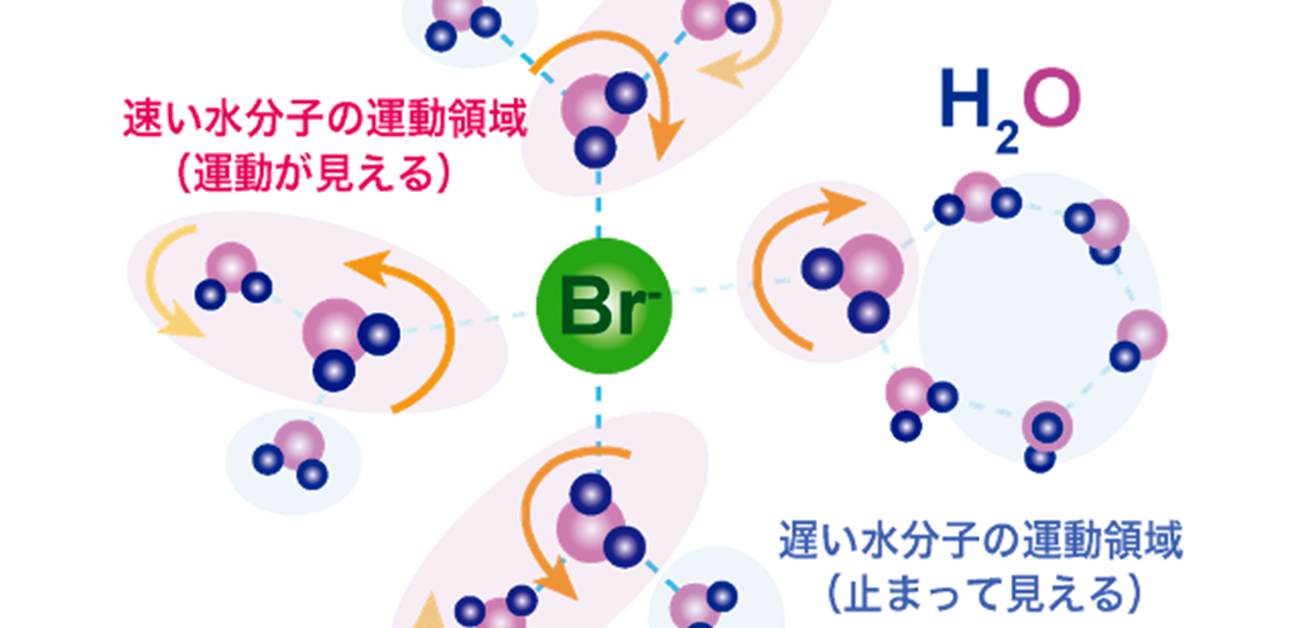
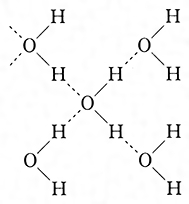
水素相互作用は水中でも起こります。
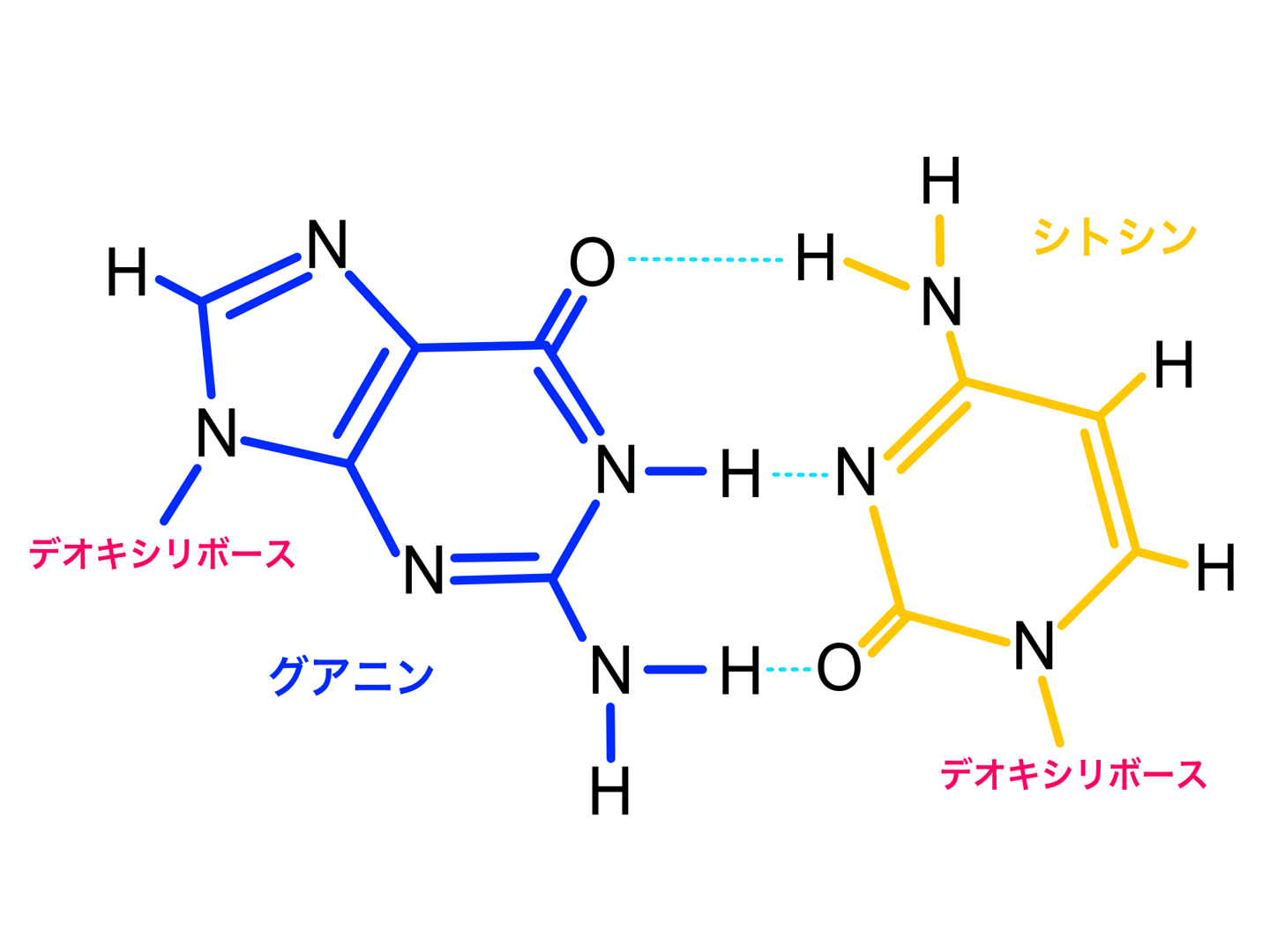
電気陰性度の高い原子間で水素結合が起こることには議論の余地がありません。文献から漏れることが多いのは、そのような相互作用の可能性のある原子として 窒素 、 フッ素 、酸素のみを考慮していることです。さて、電気陰性度が非常に高い他の原子 ( 塩素 など) もこの現象を経験する可能性があります。したがって、可能性の世界を N、F、O グループだけに限定するのは不公平です。
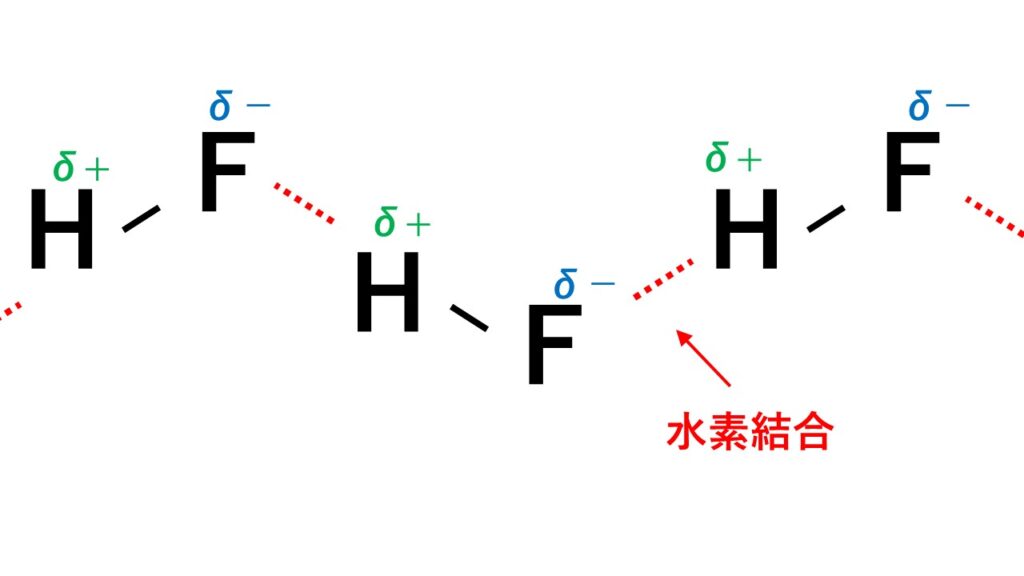
真の水素結合
水素結合は、 水素結合と同義ではありません。この種に共通点があるとしても、状況はまったく異なるからです。水素結合は、3 つの原子 (中心 3 つ、電子 2 つ) に分割された 2 つの電子からなる分子配置を表します。
たとえば、ジボラン (B 2 H 6 ) では、2 つのホウ素原子が、文字通りそれらの間に橋を形成する水素原子の存在によって結合されます。したがって、BH 3 種は強調表示されず、その二量体が強調表示されます。
この例では、各ブリッジからの 2 つの水素電子が 2 つのホウ素原子に分割されます (つまり、2 つの電子と 3 つの原子 – BHB)。
http://sec.sbq.org.br/cd29ra/resumos/T1907-1.pdf
ギャラリー