化学元素ホウ素は 原子番号 5、原子質量 10.811 を持っています。非晶質のときの密度は 2.34 です。最も純粋な結晶状態では、非常に硬く、ほぼ金属のような光沢があり、密度は 3.3 です。 融点 は2,300℃で、穏やかに揮発します。ホウ素は純粋な状態ではあまり応用できませんが、 ホウ酸 や ホウ砂 の形では産業界で広く応用されています。 温度 の上昇とともに 導電率 が増加するため、エレクトロニクス分野では 半導体 として使用されます。ホウ素は金属元素と非金属元素の両方と結合して共有結合化合物を形成できますが、いかなる場合もイオン状態、カチオン (正に荷電したイオン) またはアニオン (負に荷電したイオン) を生じません。
ホウ酸

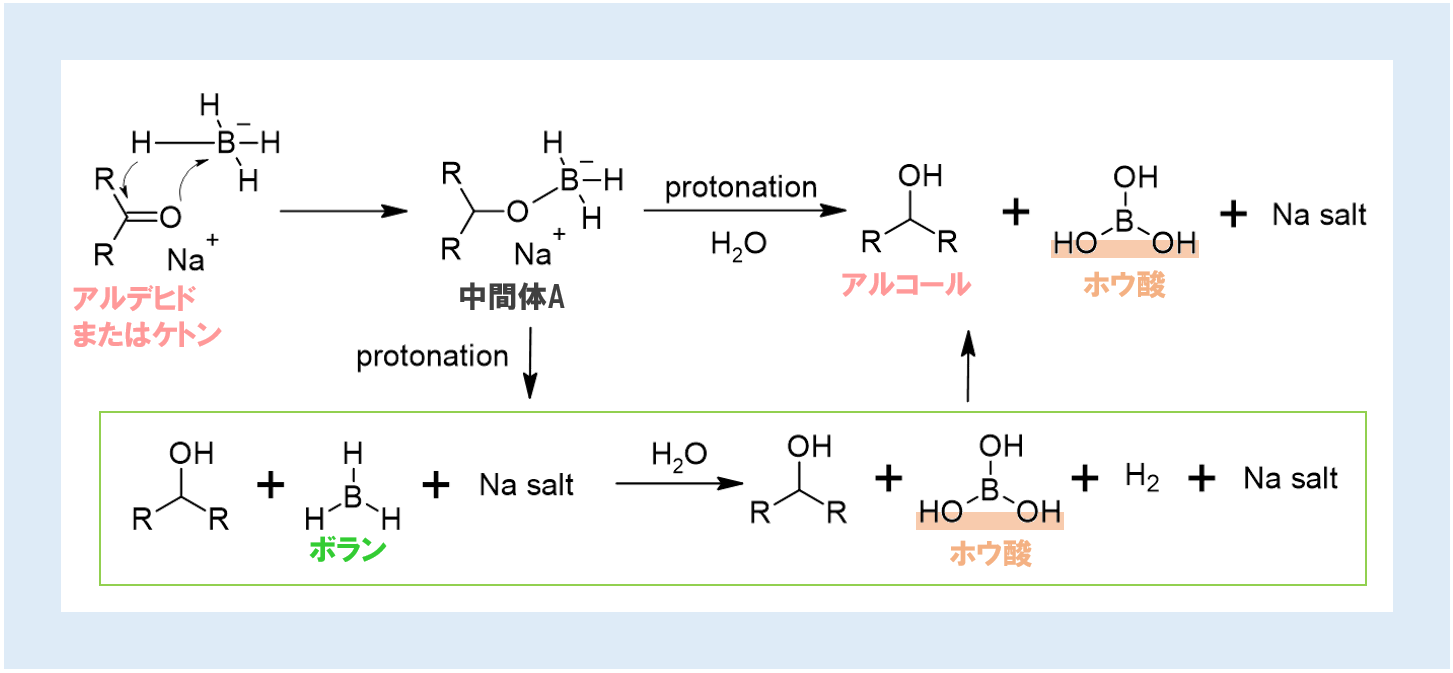
現在、化学元素ホウ素に由来するいくつかの酸がホウ酸として知られており、すべて無水ホウ酸に由来していますが、最も適切なものは H 3 BO 3 、つまりオルトホウ酸であり、過去には以下の縮合によって得られていました。トスカーナのいわゆるマレンマに存在する噴気孔から 90 度から 120 度の温度で噴出する火山蒸気により、少量のこの酸が引きずり込まれます。その後、米国 (カリフォルニア州) と 南アメリカ で天然に産出するホウ酸カルシウムからホウ酸が得られるようになりました。
ホウ酸は非常に 弱い 酸性の 性質を持っており、かつては主に防腐剤として、また一部の食品の保存に医療に使用されていました。この酸の既知の毒性特性により、この行為は現在禁止または禁忌です。ホウ酸はガラスの製造にも使用され、特に熱に耐えるために金属シートを覆うエナメルにも使用されます。
ホウ砂
化学元素ホウ素のもう 1 つの重要な誘導体は、単にホウ砂として知られる四ホウ酸ナトリウム (Na 2 B 4 O 7 ) です。 ホウ砂は自然界ではチンカル (単斜晶系鉱物、水和ホウ酸ナトリウム) の形で存在し、平均 55% のホウ砂 (十水和四ホウ酸ナトリウム、Na 2 B 4 O 7 ・10H 2 O) を含みます。現在、ホウ砂は無色の結晶の形で天然に得られ、冷水にはわずかに溶けますが、熱水にはより溶けやすく、その溶液はアルカリ性です。

ホウ砂は、溶けると一部の金属酸化物を溶解し、特定の色の化合物を形成する特性があり、色によってこれらの金属を識別することを目的とした ホウ砂パール として知られる 分析化学 のテストに使用されます。現在、ホウ砂はエナメルや光学ガラスの製造に大量に使用されています。石鹸と乾性油の製造。キャンドルの芯を硬くする場合。紙、トランプなどのサテン仕上げに。他のアプリケーションの中でも。
参考文献:
サルデッラ、アントニオ。マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
ラッセル、ジョン B. General Chemistry vol.1、サンパウロ: ブラジルのピアソン教育、マクロンブックス、1994 年。
マハン、ブルース・M。ローリー・J・マイヤーズ;化学: 大学コース、Edgard Blucher LTDA、サンパウロ/SP – 2002
ギャラリー