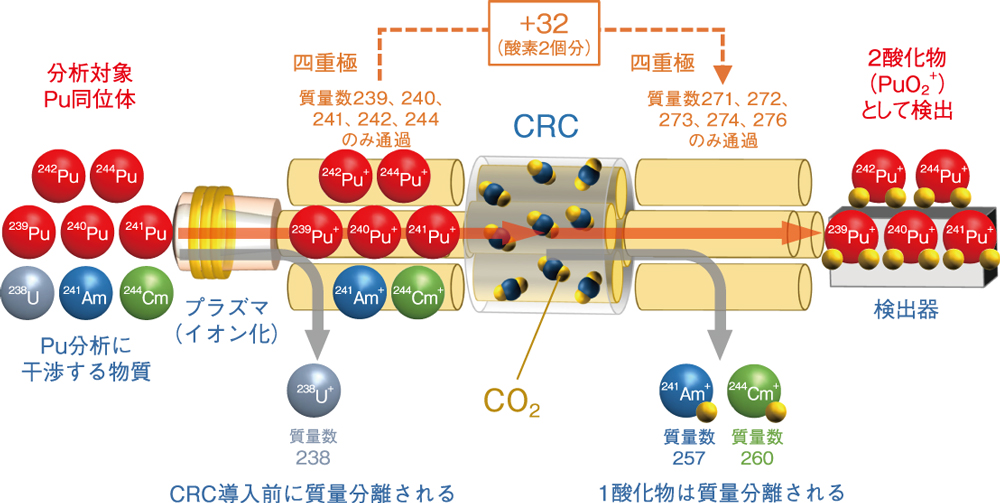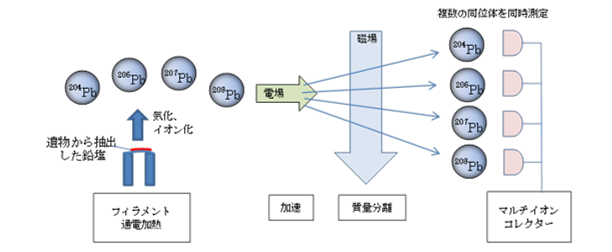
同位体

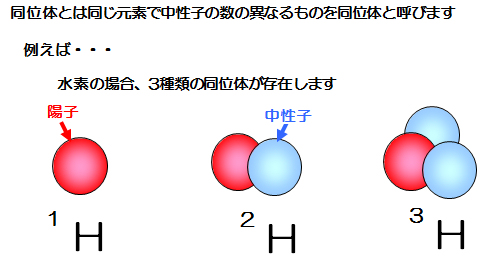
化学元素の 原子は 、原子番号が同じであっても、含まれる 中性子 の数が異なるため、質量数が異なることがあります。この特徴的な 同位体 を持つ原子を原子と呼びます。つまり、それらは同じ数の 陽子 を持っています。いくつかの化学元素には同位体がありますが、3 つの同位体のそれぞれに特別な命名法があるのは 水素 だけです。
| プロチウム | 重水素 | トリチウム | |
| 1H1 | 1D2 | 1T3 | |
| n = 0 | n = 1 | n = 2 | |
| 発生: | 99.985% | 0.015% | 10 -7 % |
同位体を持つ他の元素には水素のような特別な命名法はなく、以下のように質量数のみで識別されます。
|
カーボン12
6C12 n = 6 |
カーボン13
6C13 n = 7 |
カーボン14
6C14 n = 8 |
|
酸素16
8 0 16 n = 8 |
酸素17
8 0 17 n = 9 |
酸素18
8 0 18 n = 10 |
したがって、同位体は、同じ数の陽子と異なる数の質量と中性子を持つ、同じ化学元素の原子であると結論付けることができます。
放射性同位体 は放射性核を持つ原子であり、同位体に変化すると、 アルファ線 、 ベータ線 、または ガンマ線 粒子と呼ばれる放射線の形でエネルギーを放出します。上記の炭素 14 は 炭素 の放射性同位体であり、化石年代測定や地下水研究で広く使用されています。
イソバリア
異なる化学元素の原子は同じ質量数を持つことができますが、含まれる中性子の数が異なるため、原子番号は異なります。この特徴を持つ原子を等圧原子、つまり同じ質量を持つ原子と呼びます。いくつかの例を見てみましょう。
|
カーボン14
6C14 n = 8 |
窒素
7N14 n = 7 |
|
カリウム
19K40 n = 21 |
アルゴン
18 エア 40 n = 22 |
したがって、等圧線は、同じ質量数を持つ異なる化学元素の原子であると結論付けることができます。

等張性
これらは、同じ数の中性子を持つが、原子番号が異なる、異なる化学元素の原子です。この特徴を持つ原子をアイソトーン原子と呼びます。つまり、同じ数の中性子を持っています。いくつかの例を見てみましょう。
|
カーボン14
6C14 n = 8 |
酸素
8 0 16 n = 8 |
|
ボロン
5B11 n = 6 |
炭素
6C12 n = 6 |
したがって、アイソトンは、同じ数の中性子を持つ異なる化学元素の原子であると結論付けることができます。

等電子工学
それらは、同じ数の電子を持つ異なる化学元素の原子です。この特性を持つ原子を等電子原子と呼びます。つまり、同じ数の 電子 を持っています。それらは中性原子、陽イオンまたは陰イオンの場合があります。いくつかの例を見てみましょう。
|
マグネシウムカチオン
12mg 2+ 電子 = 10 |
フッ素アニオン
9F -1 電子 = 10 |
|
カルシウムカチオン
20Ca2 + 電子 = 18 |
リン陰イオン
15P -3 電子 = 18 |
したがって、等電子は、同じ数の電子を持つ異なる化学元素の中性原子またはイオンであると結論付けることができます。
以下の表では、このコンテンツで検討した違いを確認できます。
| 原子の類似性 | 陽子の数 (Z) | 質量数(A) | 中性子の数 (n) | 電子の数 (e) |
| 同位体 | = | ≠ | ≠ | ≠ |
| 等圧線 | ≠ | = | ≠ | ≠ |
| アイソトーン | ≠ | ≠ | = | ≠ |
| アイソエレクトロニクス | ≠ | ≠ | ≠ | = |
参考文献:
BOSQUILHA、G. 化学ミニマニュアル: 理論と実践 。 2. 改訂版サンパウロ:リディール、2003年。
http://adm.online.unip.br/img_ead_dp/21667.PDF
ギャラリー



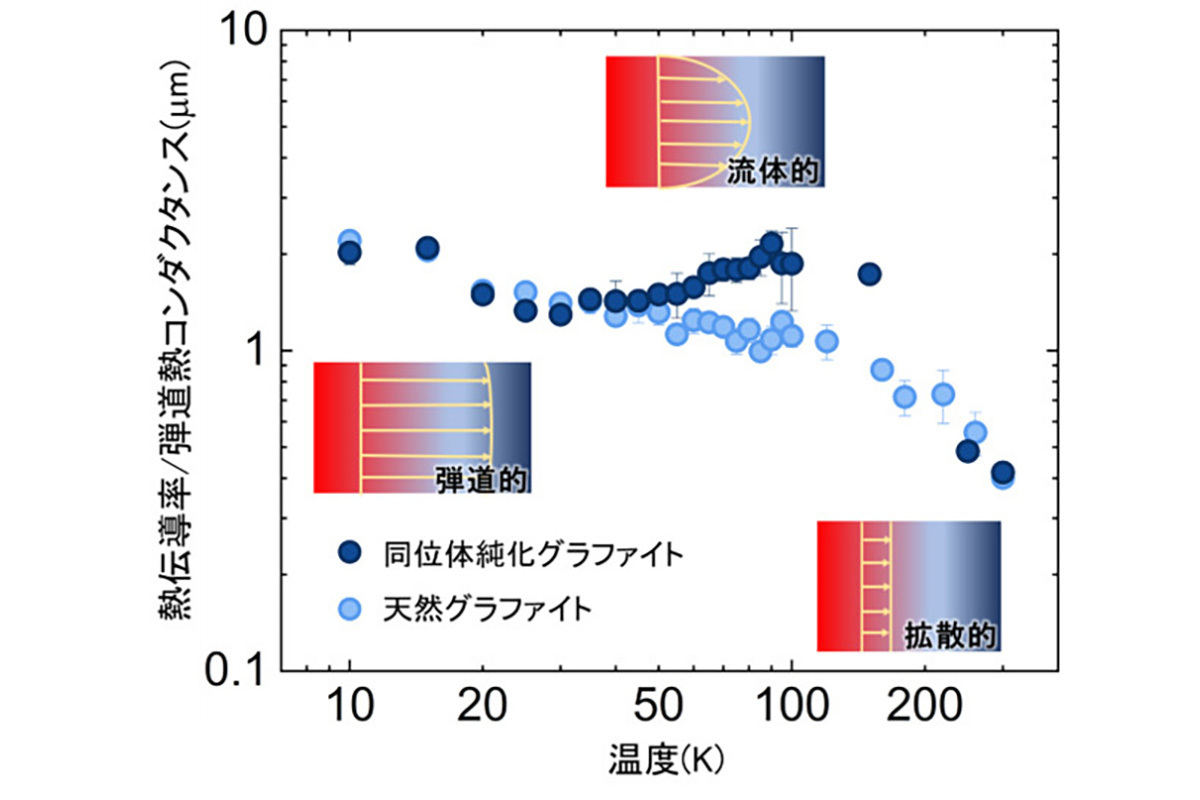

画像1(田中先生).png)