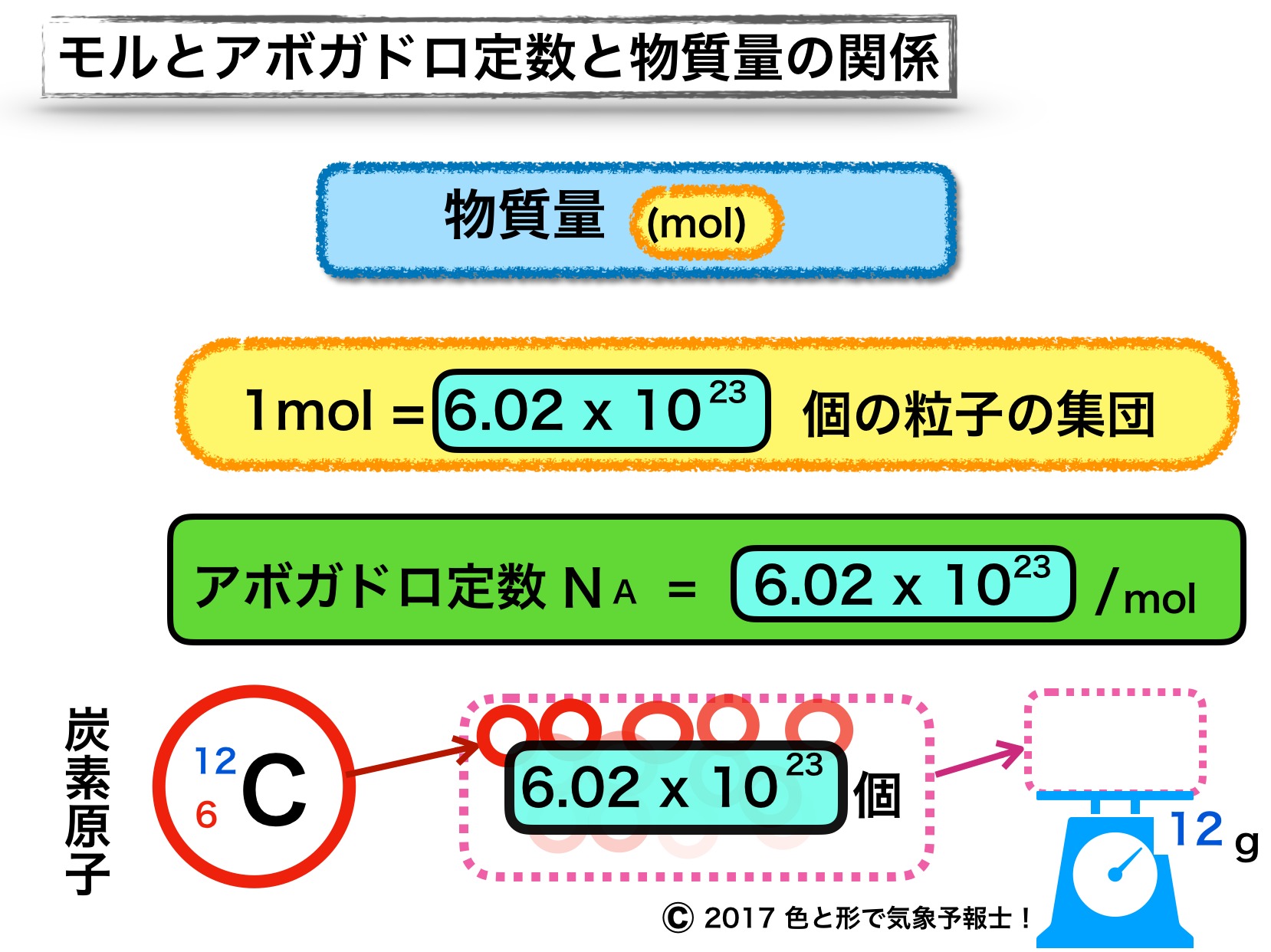
原子質量単位 (u)
この単位は、
12
C
原子
の質量の 1/12 に相当し、小文字の
u
で表されます。
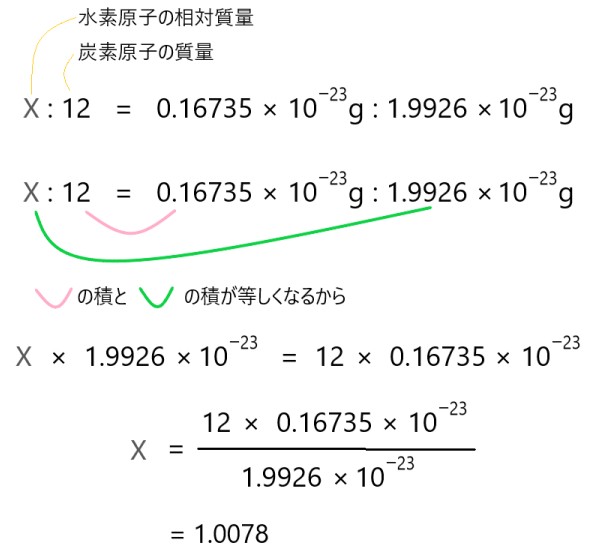
原子質量
原子質量 (MA) は、化学元素の原子が炭素 12 原子の 1/12 よりどれだけ重いかを表します。
たとえば、酸素の原子質量は 16u です。これは、炭素 12 原子の 12 の 1 部分に比べて 16 倍重いためです。

ヘリウム原子は 4u、つまりその質量は 12 C 原子の質量の 1/3 に相当します。
注: 周期表や大学入試では単位の u が省略されることがよくあります。
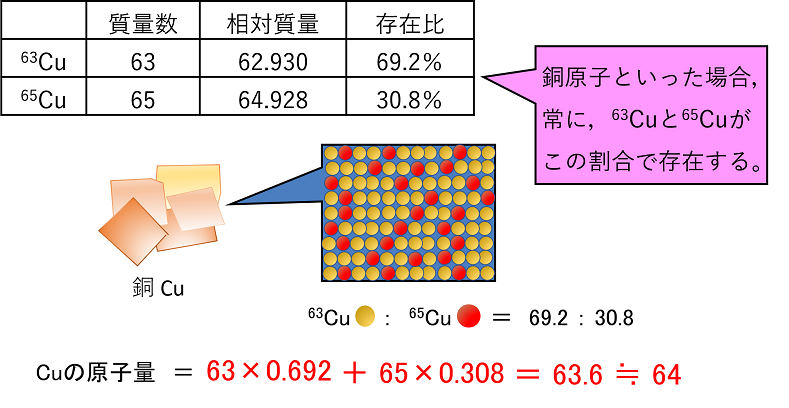
化学元素の原子量
化学元素は複数の
同位体
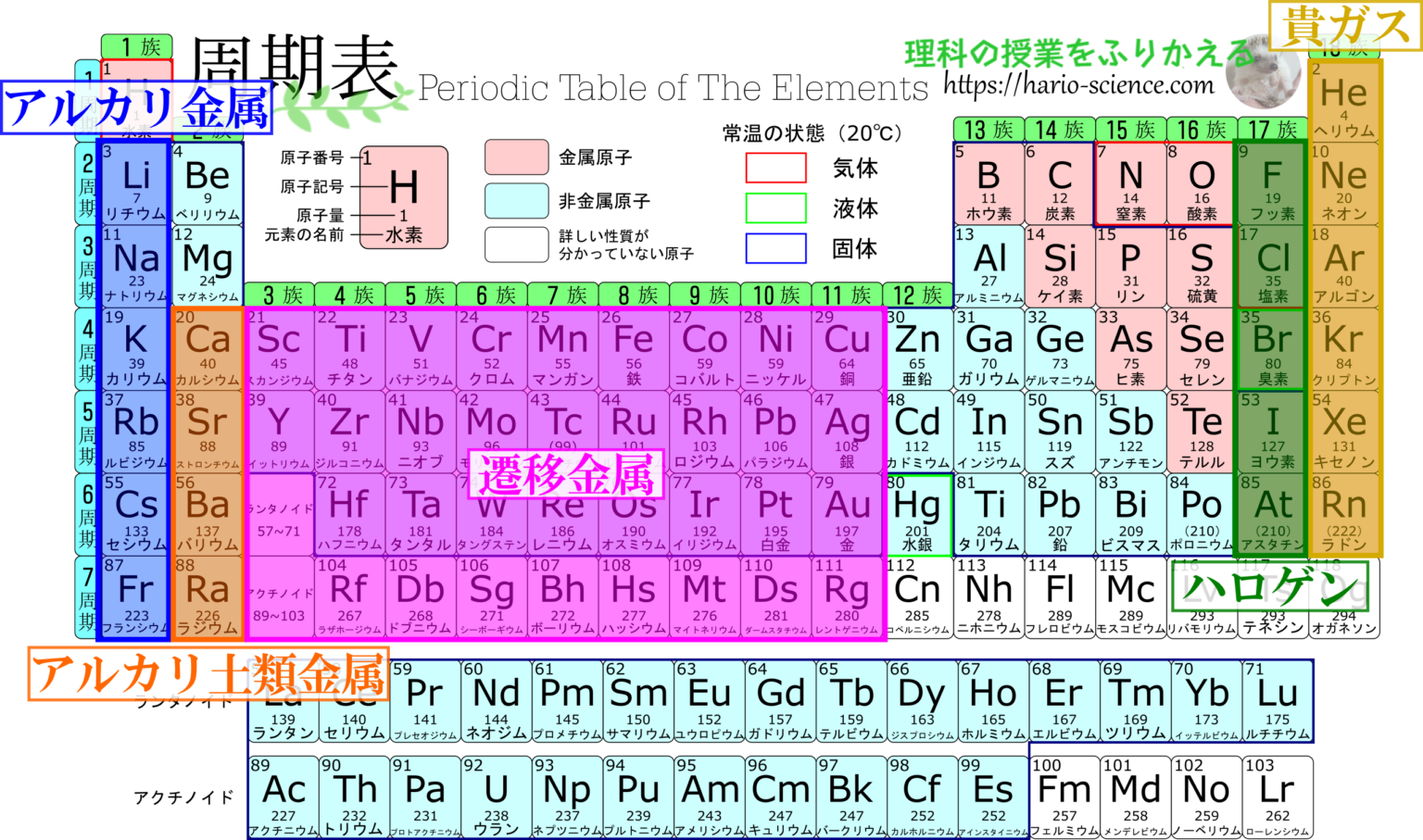
(原子番号は同じだが質量が異なる) を持つことができますが、それらすべてを
周期表
で表すことは現実的ではありません。したがって、これらの表に示されている原子質量は、この化学元素が持つ宇宙に存在するさまざまな安定同位体の質量の
加重平均
です。
たとえば、酸素には 3 つの安定同位体があります。
- 16 O – MA = 16u、宇宙の全酸素原子の 99.7% に相当
- 17 O – MA = 17u、O 原子のわずか 0.03%
- 18O – MA = 18u、存在量 0.2%
加重平均を取ると、次のようになります。

予想通り、酸素原子の 99.7% がこの MA を持っているため、加重平均では 16 に近い値が得られました。
次に、
塩素
の例を見てみましょう。塩素の安定同位体:
- 35 Cl – MA = 35u、塩素原子の 75.4% を表す
- 37 Cl – MA = 37u、塩素原子の 24.6% です
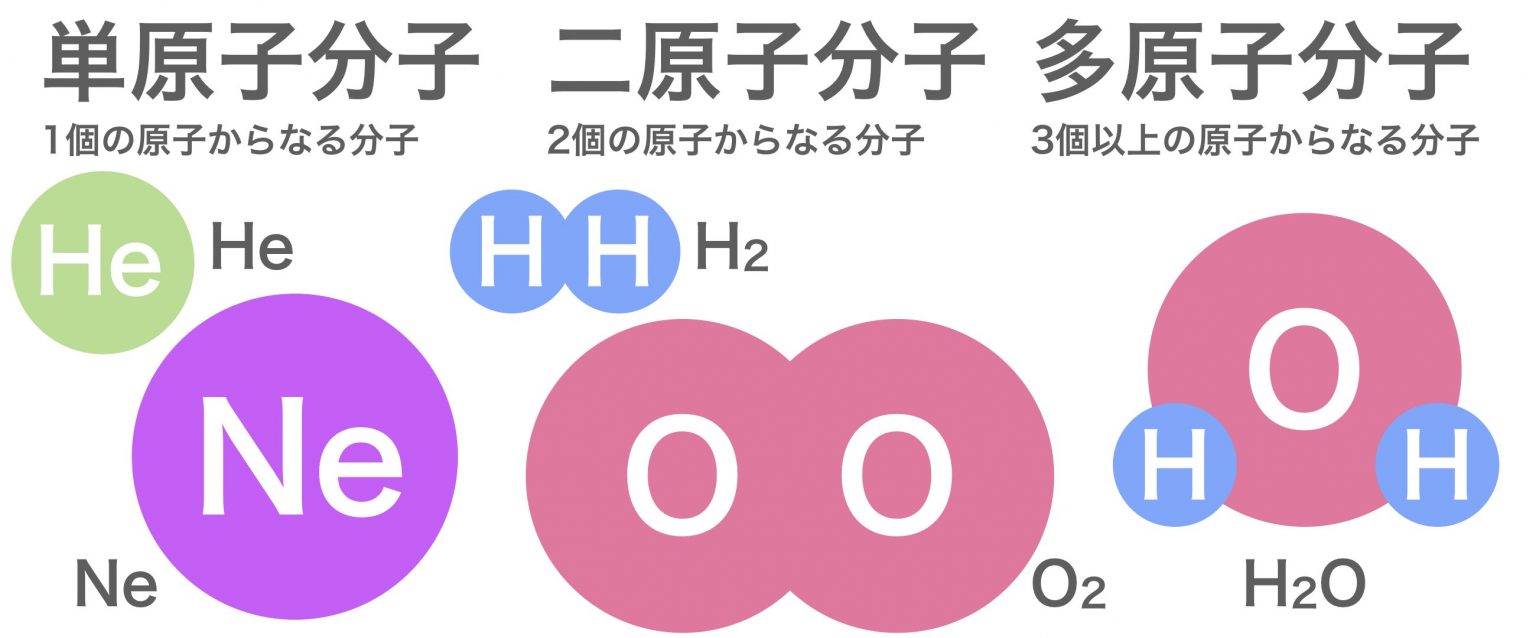
分子量
分子量 (MM) は、
分子
を構成する原子の原子質量の合計です。たとえば、水分子 (H
2
O) には次のものがあります。
- H = 1u、2 つの 水素 = 2u
- O = 16u
- H2O = 2u + 16u = 18u
ギャラリー