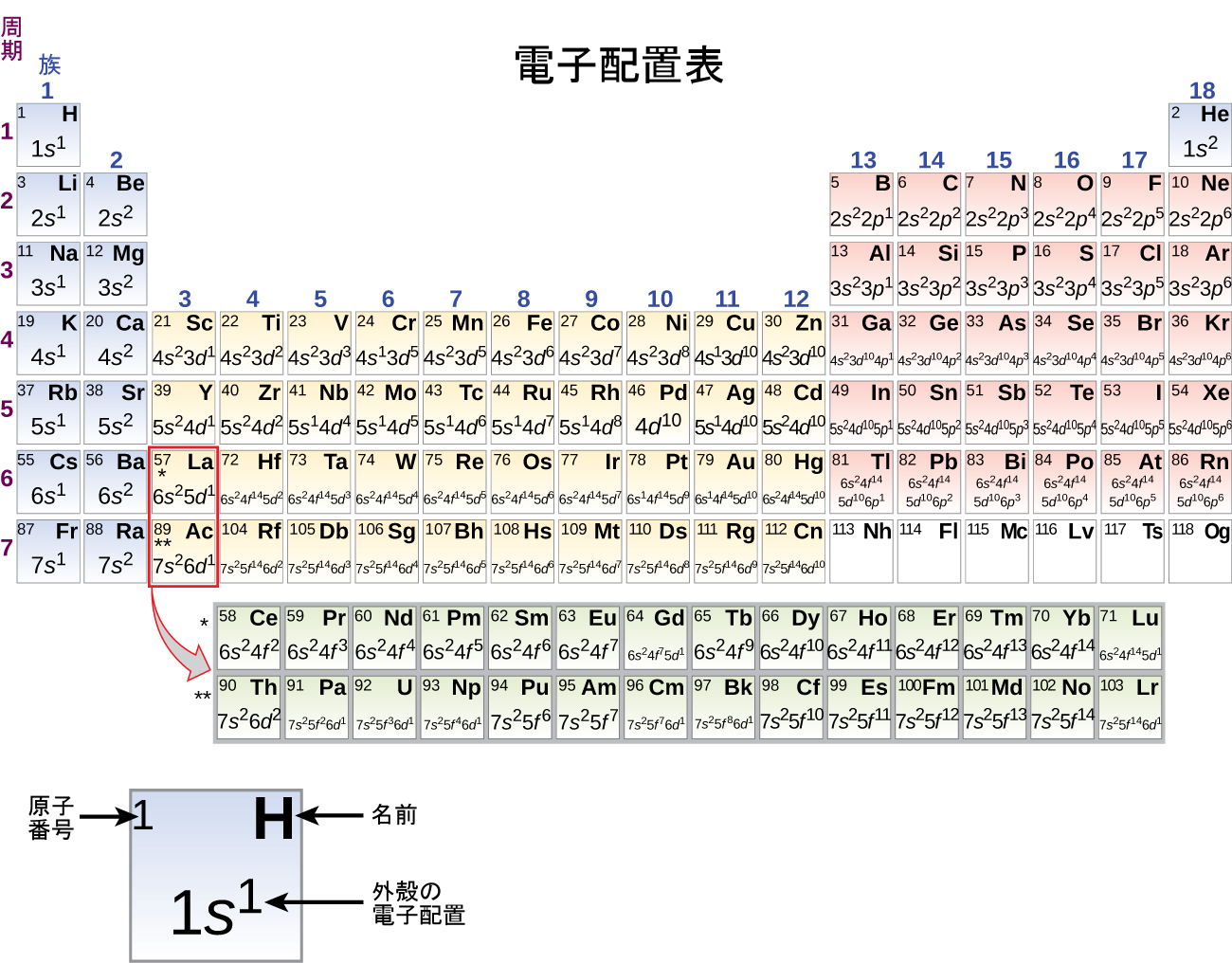
原子 の多くの特性は原子番号に応じて周期的な変化を示すため、 表 で示すことができます。それらの中には、化学的特性としてみなされる 原子半径 、 イオン化エネルギー 、 電子親和力 、電気陰性度 および電気陽性度 、および 密度 、 原子体積 、融点および沸点、金属特性などの物理的性質としてみなされるものがあります。
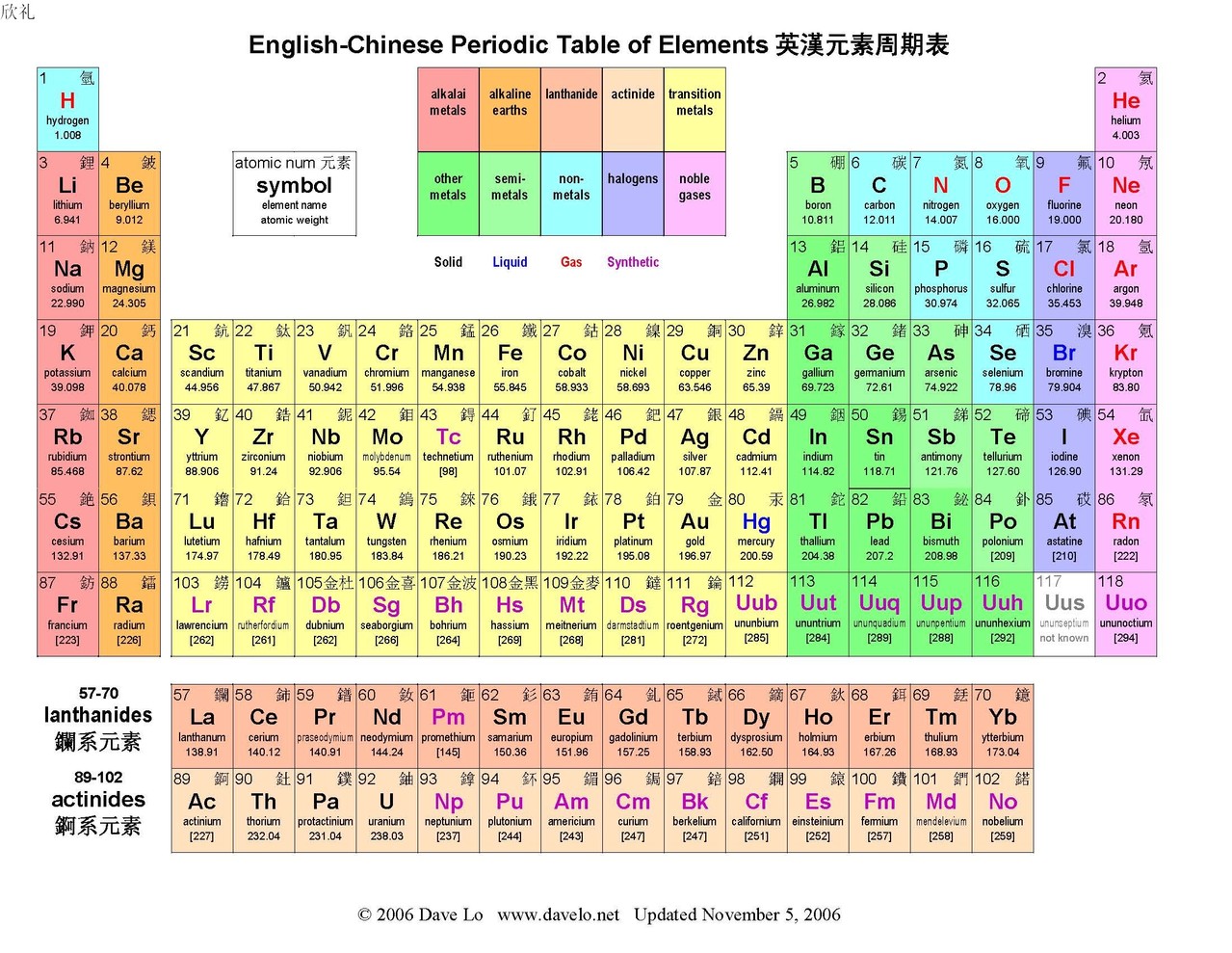
周期表での化学元素の配置は、その特性の変化がより明確になる最も一貫した方法を表しています。したがって、グループ化すると、「類似性」を持つ化学元素が互いに近くに見つかるため、これらの元素はこれらの特性のいくつかに従って分類できます。

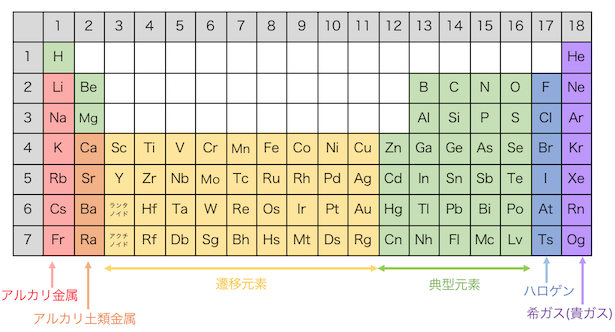
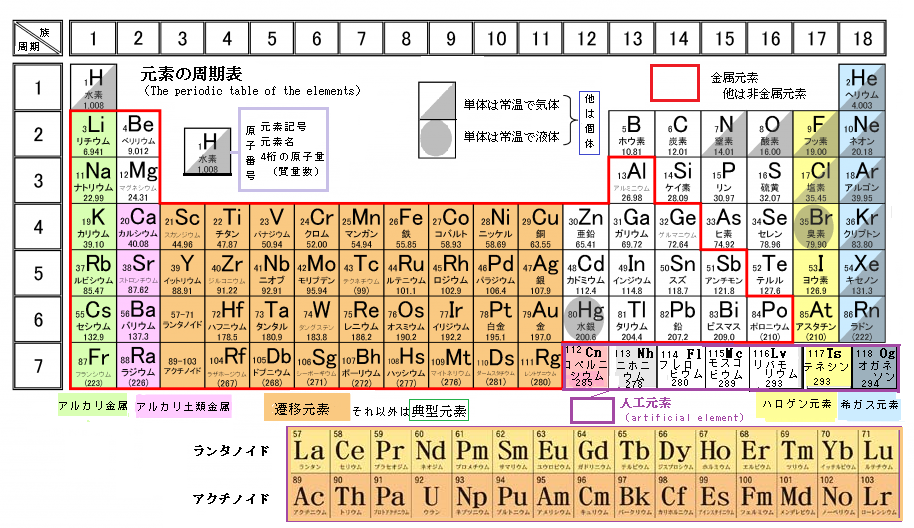
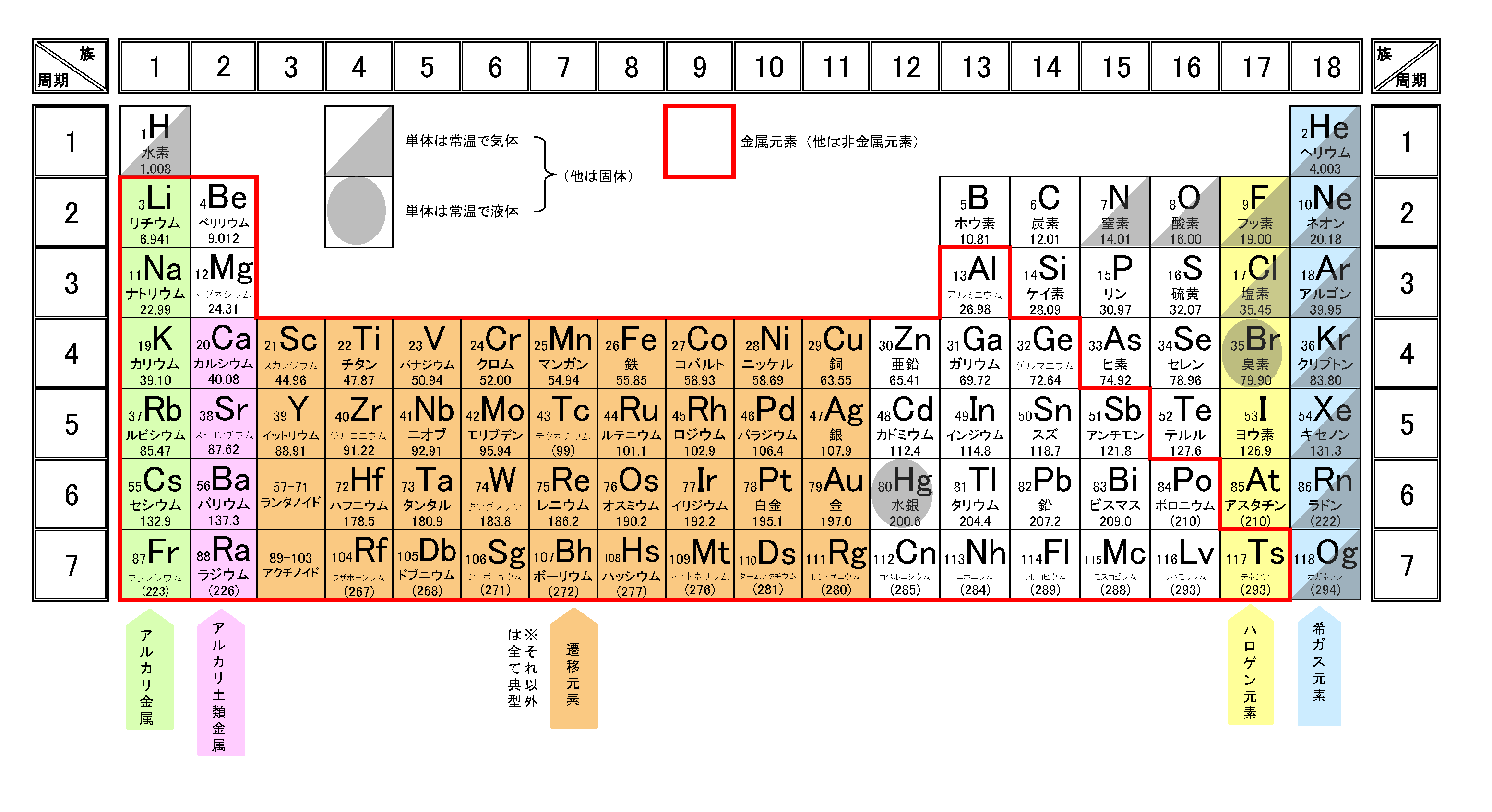
一部の元素族 (周期表の縦線) は、その特性の一部に関連する名前によって特徴付けられます。たとえば、IA 族元素は、その化合物が腐食性、つまり名前が示すように「アルカリ性」であるため、 アルカリ金属 と呼ばれることがよくあります。 IIA 族元素は、鉱物に含まれ、その化合物の一部は腐食性であるため、 アルカリ土類金属 として知られています。 VIIA 族の元素は ハロゲン と呼ばれ、その名前はギリシャ語の「塩形成体」に由来しています。グループ 0 の元素は 希ガス であり、その物理的状態と低い、実質的に存在しない化学反応性に基づいて名前が付けられています。
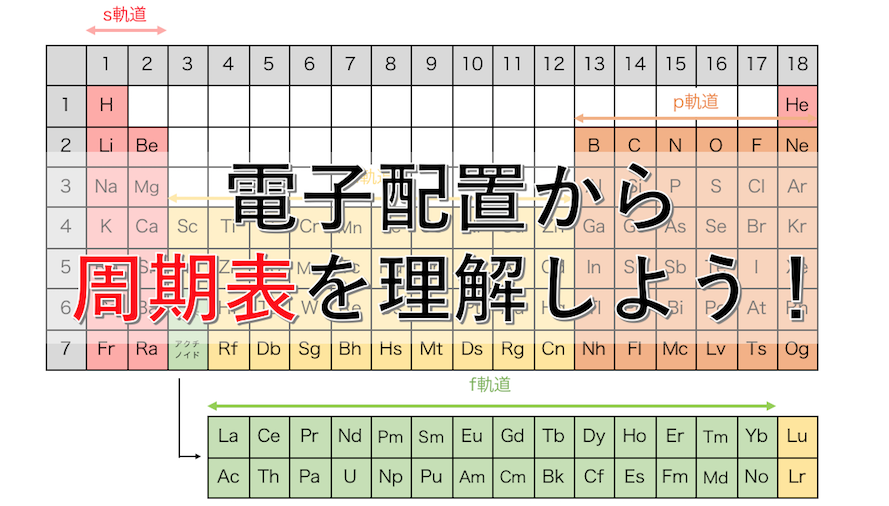
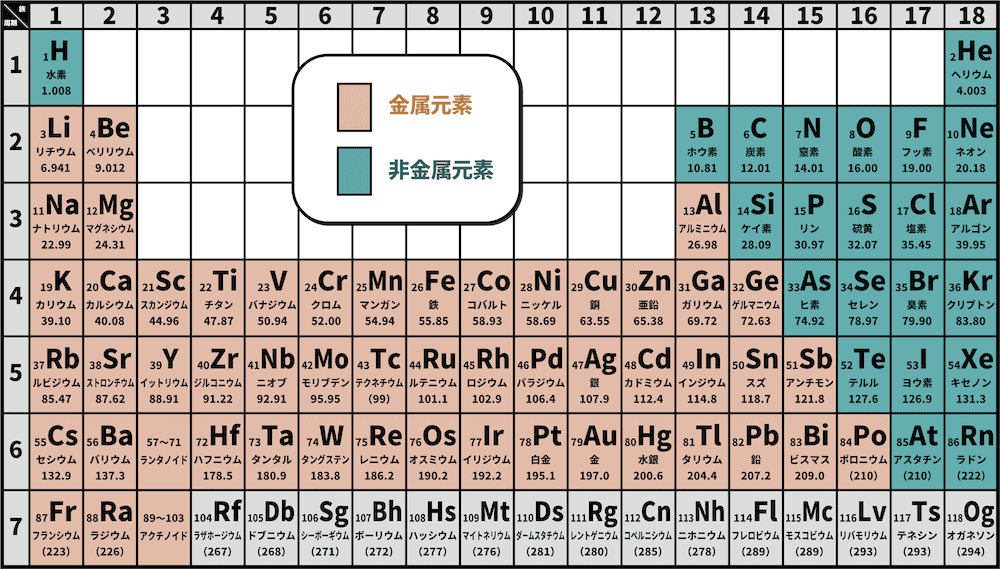
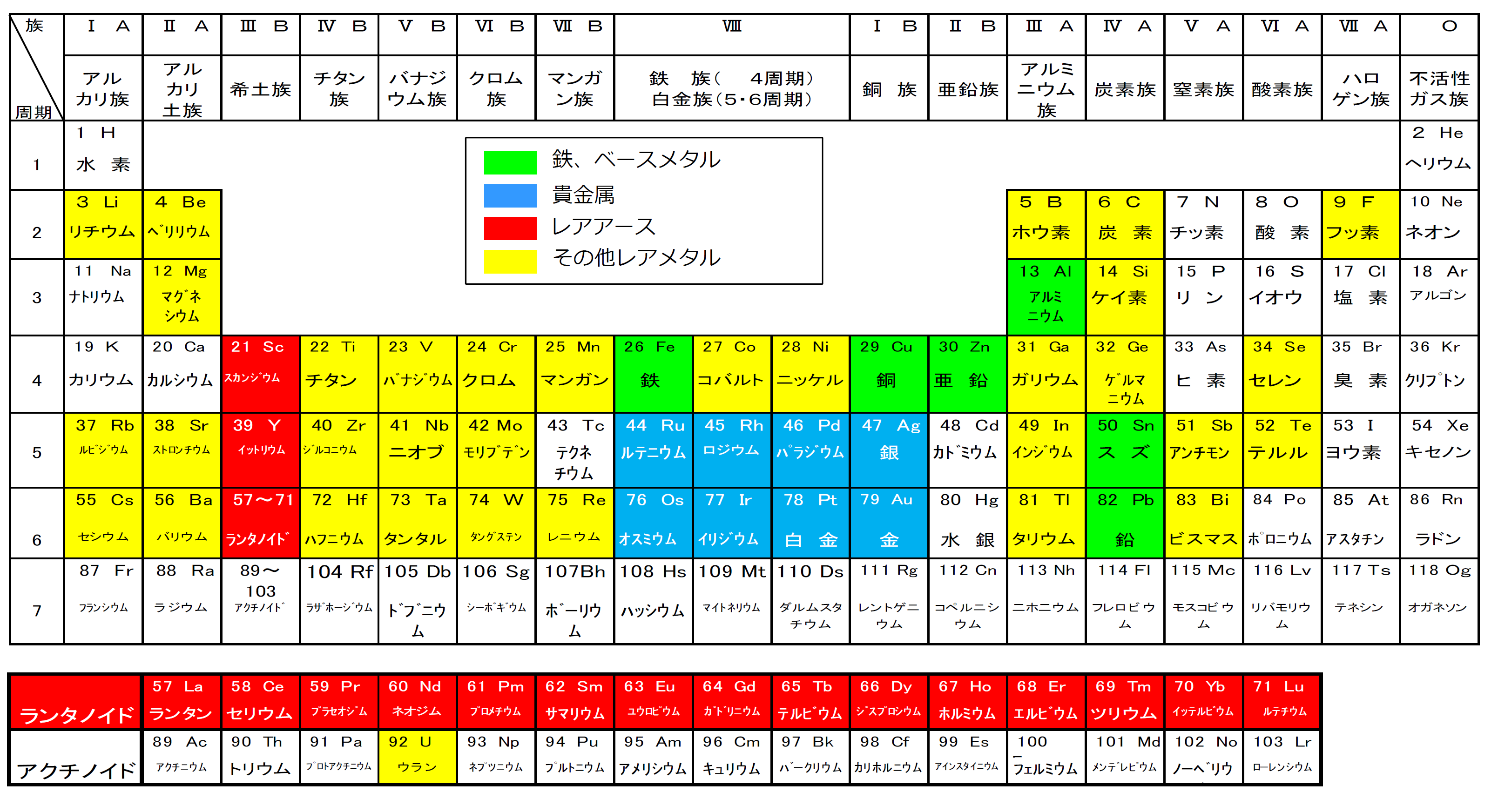
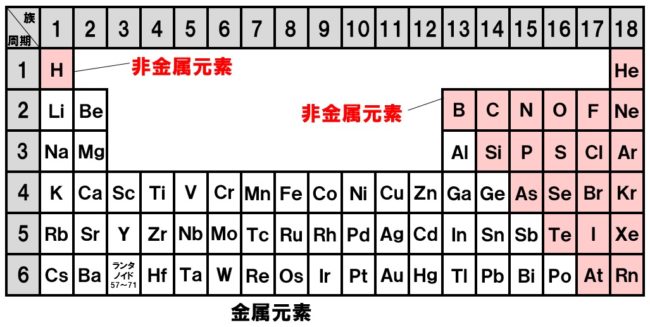
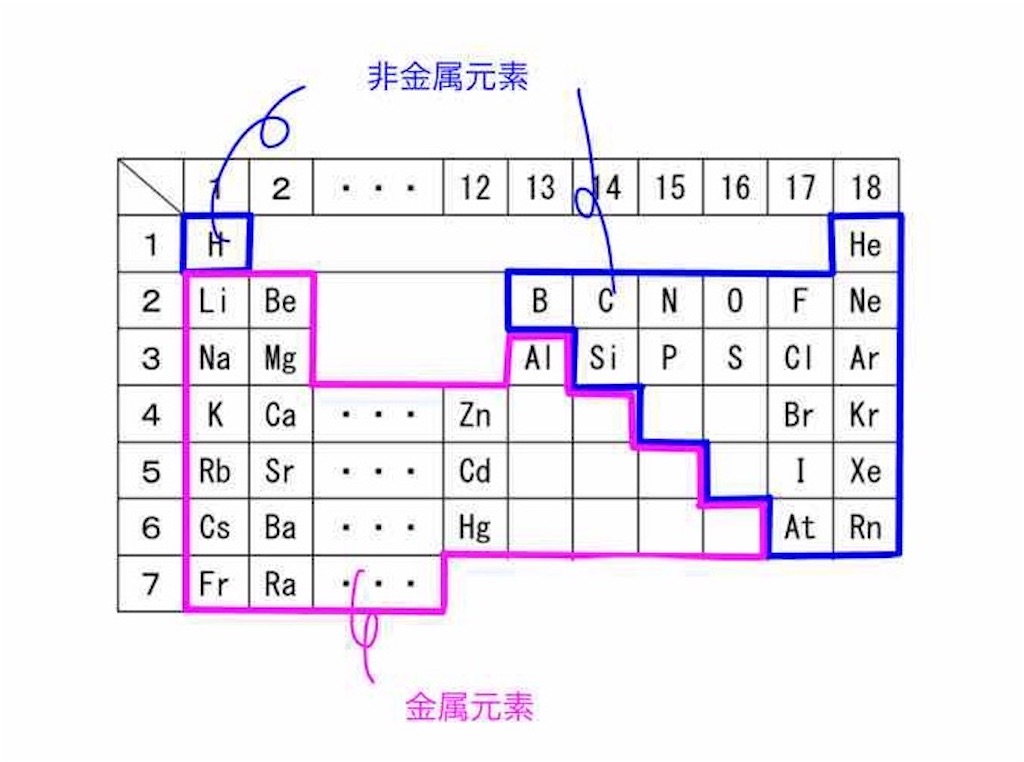
さらに幅広く、元素は 金属 、 半金属 、非金属に分類することもできます。この分類基準は、主にこれらの元素の電気的特性に基づいています。なぜなら、「 私たちが金属的性質と呼ぶものは、実際には、次の一般的な事実に基づいた一連の特性です。つまり、元素はより金属的であり、電子を失う能力が大きくなります 。」 1 .

金属は高い 電気伝導率と熱伝導率 、特徴的な光沢、一般に高い融点、延性、展性を持っています。一方、 非金属または非金属は 、電気と熱の伝導性が悪く、金属特有の光沢がなく、固体の場合は非常に脆いです。半金属または半金属は、金属と非金属の中間の特性を持っています。例えば、電気半導体として工業的に利用されている。

周期表では、元素の大部分は金属であり、これらは左側に位置し、さらに右側にある非金属が不利になります。 2 つのグループの間には、半金属が存在し、2 つのグループ間の一種の区分を形成しています。 「 グループ IA の最上位にある水素は、実際にはこの分類から除外される唯一の元素です。これは、通常の条件下では非金属の挙動を示し、極度の高圧では金属の挙動を示すためです 。」 2 .
参考文献:
1. サルデッラ、アントニオ;マテウス、エデガー。化学コース: 一般化学、アティカ編、サンパウロ/SP – 1995 年。
2. マハン、ブルース・M。ローリー・J・マイヤーズ;化学: 大学コース、Edgard Blucher LTDA、サンパウロ/SP – 2002
ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
ローゼンバーグ、イスラエル・モルカ。一般化学、マウア工科大学、Edgard Blucher LTDA、サンパウロ/SP – 2002 年。
ギャラリー