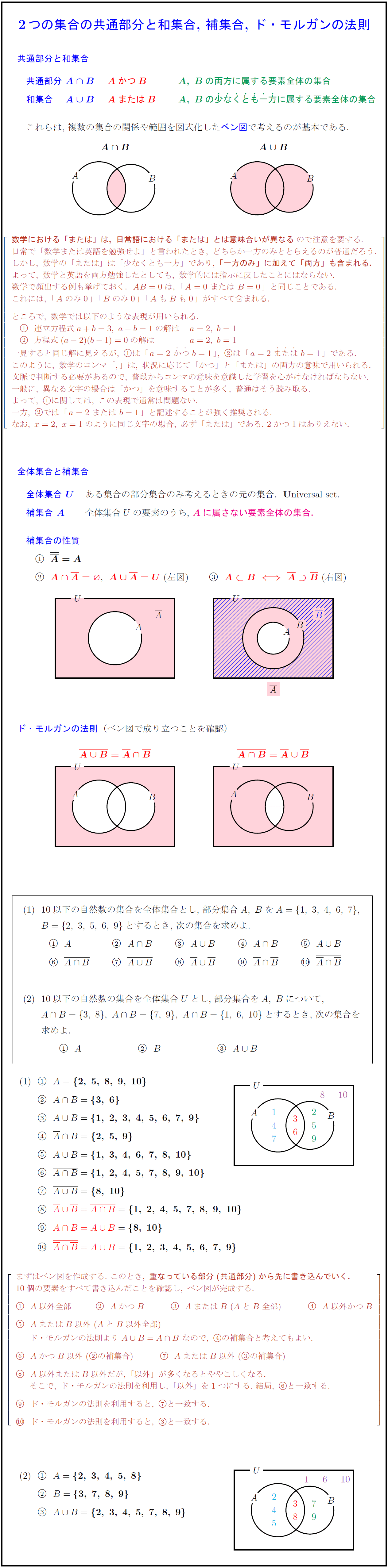
凝集特性は 、分散粒子の数に依存する溶液の特性であり、溶質粒子の性質には依存しません。

水の物理的特性に対する溶質の影響は、いくつかの一般的な状況、または少なくともわかりやすい状況で見ることができます。たとえば、極寒の場所で車のラジエーター内の水が凍結するのを防ぐ方法などです。なぜ砂糖が傷の治りを早めるのか。なぜ肉を保存するために塩を加えるのか。
溶質はイオン性と分子性に分類されます。イオン性溶質は、食塩、NaCl などの イオン結合 を持つ溶質です。この場合、イオンは解離し、溶液中に分散します。分子溶質は 共有結合 を持っており、この場合解離はありませんが、分子は溶液中で孤立して配置されます。分子溶質の例は、糖 (スクロース) C 12 H 22 O 11 です。
結合プロパティは次のように分類されます。

沸騰鏡検査
この現象は、例えば、沸騰寸前のコーヒー水に砂糖を加えると、溶媒との相互作用により沸点が遅れる場合に発生します。言い換えれば、沸騰は沸騰温度の上昇、より具体的には不揮発性溶質粒子の存在による沸騰温度の変動の増加から構成されます。計算に使用される式は次のとおりです。
ΔTe = Te 2 – Te
どこ:
- Te = 溶液の沸点
- Te 2 = 溶媒の沸点

眼圧検査
このプロセスは トノメトリー とも呼ばれ、溶質が関与する溶媒の最大蒸気圧を下げることから構成されます。最大蒸気圧は、凝縮速度と 蒸発 速度が等しくなり、動的平衡に達したときに発生することを覚えておく価値があります。このプロセスは、たとえば水 (溶媒) にヨウ素 (不揮発性溶質) を加えるときに発生します。眼圧検査の計算式は次のとおりです。
Δp = P 2 – P
どこ:
- P = 溶液の 蒸気圧
- P 2 = 溶媒の蒸気圧。

凍結鏡検査
この現象はクライオメトリーとも呼ばれ、ラジエーター内の水の凍結を防ぐことができる理由です。非常に寒い国では、ラジエーター内の水に特別な添加剤を加えて、水の沸点を上げ、 凝固点または凝固点 を下げます。そして、水中のこの添加物の濃度が高くなるほど、凝固温度は低くなります。このプロパティを計算できる式は次のとおりです。
ΔTc = Tc 2 – Tc
どこ:
- Tc = 溶液の凝固温度
- Tc 2 = 溶媒の凝固温度

浸透圧
まず、 浸透 現象を定義する必要があります。これは、溶媒が半透膜を通って最も濃度の低い溶液から最も濃度の高い溶液に通過する現象です。これは、たとえば、調理前に豆を浸したままにするときに発生します。豆の粒が膨らんでいるのがわかります。浸透圧は、溶媒の通過を遮断または妨害するために溶液に加えなければならない圧力です。その計算式は次のとおりです。
Π= MRT
どこ:
- M=モル濃度
- R = 気体定数
- T = ケルビン単位の温度
ギャラリー


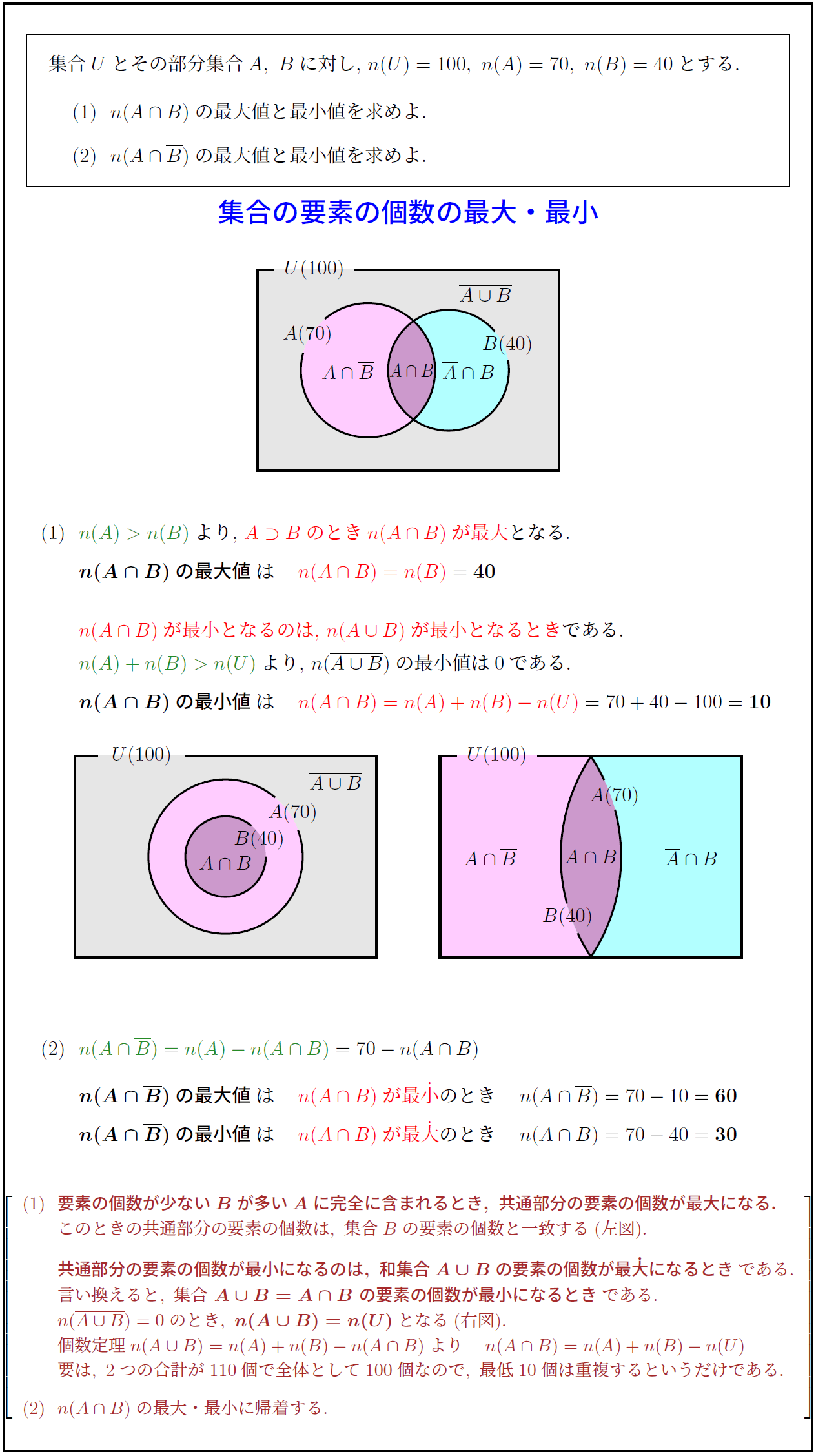

/assets/images/4076660/original/20190905060037.jpg?1568002134)