1862 年、アレクサンドル シャンクルトワ というフランスの 地質学者は 、既知の化学元素を円柱の周りの螺旋線によって原子量の昇順に並べました。この配置は テルリック スクリュー として知られるようになり、テルリックという用語は地球を指します。
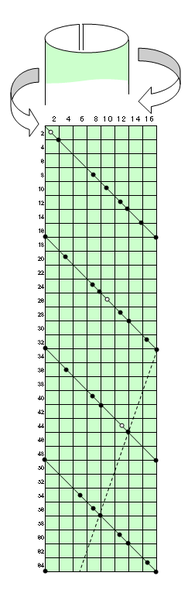
シャンクルトワは、化学元素である 酸素 の原子量に基づいており、当時すでに 16 と確立されていました。 したがって、彼は円柱を使用し、それを 16 の等しいセグメントに分割し、この円柱の表面にらせんをマークして、間に角度を形成しました。それとその軸は45°です。このらせん上に、彼は化学元素を原子量の昇順に配置しました。そして彼は、「 らせんは値が 16 の倍数である距離でジェネレーターを横切り、原子量が 16 単位異なる元素は同じジェネレーターに分類される 」ことに気づきました 。 彼はまた、各母集団の要素のグループには、少なくとも当時一般的で知られていた特性において類似点があることも観察しました。

PERUZZO E CANTO の言葉によれば、「 円柱の周りに 16 の分割が行われ、同様の性質を持つ要素が螺旋の連続的な回転で互いに重なり合っている 」とのこと です 。 Chancourtois は、その特性は配列内で要素が占める位置に直接関係しているだろうと示唆しました。しかし、彼が発見した規則性はすべての要素で観察できなかったため、このアイデアは破棄されました。
たとえば、化学元素の ホウ素 (B)、 ベリリウム (Be)、 リチウム (Li) と元素の アルミニウム (Al)、 マグネシウム (Mg)、 ナトリウム (Na) は同じ母集団に含まれています。それらの特性に類似性が与えられます。しかし、これは一部の元素の間で発生したにもかかわらず、多数の不規則性が発見されたため、当時の科学界ではシャンクルトワの研究がそれほど注目されていなかった。これらの不規則性の中で、元素 Na と Al の特性を例として使用できます。これらの元素は、価数の違いにより多くの特性が異なります。今日私たちが知っている限り、ナトリウムは一価であり、MCl 型の塩素と塩を形成しますが、三価であるアルミニウムは、MCl 3 型の塩素と塩を形成します。

しかし、この主題を探求したテキストに基づくと、彼の研究に対する反論の主な理由は実験の問題だけに集中していたのではなく、おそらく科学を行う方法のための彼の研究の過度の複雑さにあったと結論付けることができます。時代。そして、彼のシステムには純粋な化学元素だけでなく化合物も含まれていたという言及も重要です。

参考文献:
1.
http://www.laifi.com/laifi.php?id_laifi=628&idC=6120#
2. ペルッツォ、フランシスコ・ミラガイア(チトー)。カント、エドゥアルド・レイテ。 Chemistry in the Everyday Approach、現代編、vol.1、サンパウロ/SP- 1998。
アトキンス、ピーター。ロレタ・ジョーンズ。化学の原理: 現代生活と環境への疑問、ポルト アレグレ: ブックマン、2001 年。
フェルトレ、リカルド。化学の基礎、vol.ウーニコ、現代編、サンパウロ/SP – 1990
ギャラリー


















